题目内容
18.1mol下列有机物中与足量的NaHCO3溶液反应.可得2molCO2的是( )| A. |  | B. | HOCH2CH2OH | C. | HOOC-COOH | D. | CH3COOH |
分析 有机物能与碳酸氢钠反应,说明含有羧基,1mol下列有机物中与足量的NaHCO3溶液反应.可得2molCO2,则有机物含有2个羧基,以此解答该题.
解答 解:有机物能与碳酸氢钠反应,说明含有羧基,1mol下列有机物中与足量的NaHCO3溶液反应.可得2molCO2,则有机物含有2个羧基,而羟基与碳酸氢钠不反应,只有C正确.
故选C.
点评 本题考查有机物的结构和性质,为高考常见题型,侧重于学生的分析能力的考查,注意把握有机物的结构特点和官能团的性质,为解答该题的关键,难度不大.

练习册系列答案
相关题目
8.下列描述正确的是( )
| A. | 实验室制取乙酸乙酯的方程式为:CH3COOH+H18O-C2H5$?_{△}^{浓H_{2}SO_{4}}$CH3COOC2H5+H${\;}_{2}^{\;}$18O | |
| B. | 向某溶液中滴加KSCN溶液,溶液呈血红色,证明存在Fe3+而没有Fe2+ | |
| C. | 常温下浓硝酸与铝不反应,可用铝制容器存放浓硝酸 | |
| D. | 沉淀溶解达到平衡时,溶液中溶质的离子浓度不一定相等,但保持不变 |
9.下列物质中碳元素含量最高的是( )
| A. | 甲烷 | B. | 乙烷 | C. | 乙烯 | D. | 苯 |
13.下列说法正确的是( )
| A. | NaCl晶体中每个钠离子与周围6个氯离子形成6个离子键 | |
| B. | 前四周期元素的原子中,未成对电子数最多的是Mn | |
| C. | 金属导电的原因是在外电场作用下金属产生自由电子,电子定向运动 | |
| D. | 岩浆冷却过程中,晶格能高的矿物晶体先结晶 |
3.下列说法中,正确的是( )
| A. | 1 mol氢约含有阿伏伽德罗常数个氢 | |
| B. | 1 molCaCl2含有2 mol Cl- | |
| C. | 1 mol氢气含有6.02×1023个电子 | |
| D. | 1 molH2O含有1 molH2和1 molO |
3.下列各组元素性质递变情况错误的是( )
| A. | Li、Be、B原子最外层电子数依次升高 | |
| B. | P、S、Cl元素最高正化合价依次升高 | |
| C. | B、C、N、O、F原 子半径依次升高 | |
| D. | Li、Na、K的原子半径依次增大 |
20.向20mL1mol/LAl2(SO4)3溶液中,加入30mLKOH溶液,充分反应后,得0.78g沉淀,则KOH溶液的物质的量浓度为( )
| A. | 5mol/L | B. | 3mol/L | C. | 2mol/L | D. | 7mol/L |
1.下列有关化学用语使用正确的是( )
| A. | 符号为${\;}_8^{18}O$的原子常用于文物年代的测定 | |
| B. | CO2分子比例模型: | |
| C. | H2O2的电子式: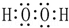 | |
| D. | 结构简式为CH2CH2的分子可发生加成反应 |

 .
.