题目内容
8.下列描述正确的是( )| A. | 实验室制取乙酸乙酯的方程式为:CH3COOH+H18O-C2H5$?_{△}^{浓H_{2}SO_{4}}$CH3COOC2H5+H${\;}_{2}^{\;}$18O | |
| B. | 向某溶液中滴加KSCN溶液,溶液呈血红色,证明存在Fe3+而没有Fe2+ | |
| C. | 常温下浓硝酸与铝不反应,可用铝制容器存放浓硝酸 | |
| D. | 沉淀溶解达到平衡时,溶液中溶质的离子浓度不一定相等,但保持不变 |
分析 A.酯化反应的实质为酸脱羟基醇脱氢,18O应该在乙酸乙酯中;
B.只能证明溶液中含有铁离子,无法证明是否含有亚铁离子;
C.常温下铁、铝能够与浓硫酸、浓硝酸发生钝化现象,发生了反应,不是不反应;
D.沉淀溶解达到平衡时,溶液中各种离子浓度不再变化,不一定相等.
解答 解:A.实验室制取乙酸乙酯时,产物中18O应该在乙酸乙酯中,正确的方程式为:CH3COOH+H18O-C2H5$?_{△}^{浓H_{2}SO_{4}}$CH3CO18OC2H5+H2O,故A错误;
B.向某溶液中滴加KSCN溶液,溶液呈血红色,证明存在Fe3+,而无法证明是否含有Fe2+,可用酸性高锰酸钾溶液检验亚铁离子,故B错误;
C.由于常温下浓硝酸与铝发生反应生成一层致密的氧化膜,即发生钝化现象,可用铝制容器存放浓硝酸,故C错误;
D.沉淀溶解达到平衡时,溶液中各种离子达到饱和状态,溶液中溶质的离子浓度不一定相等,只要外界条件不变,则溶液中各种离子浓度不变,故D正确;
故选D.
点评 本题考查较为综合,涉及难溶物溶解平衡、铝的钝化、酯化反应、常见离子检验等知识,题目难度不大,明确钝化现象的实质为解答结构,注意掌握酯化反应原理、铁离子和亚铁离子的检验方法,试题培养了学生的分析能力及化学实验能力.

练习册系列答案
相关题目
18.常温下,下列各组离子在指定溶液中能大量共存的是( )
| A. | 中性溶液中:Cl-、Mg2+、Al3+、K+ | |
| B. | 1.0mol•L-1的NaAlO2溶液中:Cl-、HCO3-、K+、Ca2+ | |
| C. | 在强碱性环境中:AlO2-、SiO32-、Na+、K+ | |
| D. | 0.1mol•L-1明矾溶液中:NH4+、AlO2-、HCO3-、Na+ |
16.用括号内试剂除去下列各物质中少量杂质,其中不正确的是( )
| A. | 苯中己烯(溴水) | B. | 乙酸乙酯中乙酸(饱和Na2CO3溶液) | ||
| C. | 甲烷中乙烯(溴水) | D. | 苯中苯酚(NaOH溶液) |
3.下列化学用语表示正确的是( )
| A. | 葡萄糖的最简式(实验式):CH2O | B. | 乙烯的结构简式为:CH2CH2 | ||
| C. | 氮气的电子式: | D. | 核内有8个中子的碳原子:86C |
20.设NA为阿伏伽德罗常数的数值,下列说法正确的是( )
| A. | 25℃时,1L pH=12的Ba(OH)2溶液中含有的OH-的数目为0.02NA | |
| B. | 标准状况下,11.2 L乙醇所含的羟基数为0.5NA | |
| C. | 1 mol Fe与1 mol Cl2反应转移电子数一定为3NA | |
| D. | 常温常压下,19g H3O+含有10NA个电子 |
18.1mol下列有机物中与足量的NaHCO3溶液反应.可得2molCO2的是( )
| A. |  | B. | HOCH2CH2OH | C. | HOOC-COOH | D. | CH3COOH |
 一定温度下,在2L的恒容密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如图所示:
一定温度下,在2L的恒容密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如图所示: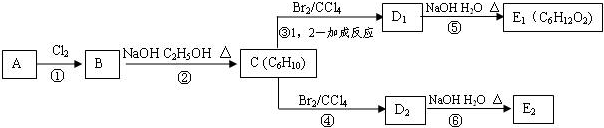
 ;E2含有的含氧官能团的名称为:羟基.
;E2含有的含氧官能团的名称为:羟基.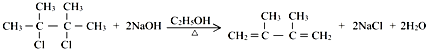 ,反应类型为:消去反应;反应⑥的化学方程式为:
,反应类型为:消去反应;反应⑥的化学方程式为: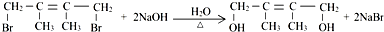 ,反应类型为:水解反应(或取代反应).
,反应类型为:水解反应(或取代反应).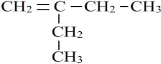 、
、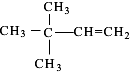 (均不考虑立体异构).
(均不考虑立体异构).