题目内容
7.若NA表示阿伏加德罗常数的值,下列说法正确的是( )| A. | 6.4gCu与足量的硫反应,转移电子数为0.2 NA | |
| B. | 通常情况下,32g O2和O3的混合气体含有的分子总数小于NA | |
| C. | 6.4g CaC2中含有的离子总数目为0.3NA | |
| D. | 标准状况下,将分子总数为NA的NH3和Cl2充分混合后,所得混合气体体积约为22.4L |
分析 A.铜与硫反应生成硫化亚铜;
B.氧气摩尔质量为32g/mol,臭氧摩尔质量为48g/mol;
C.CaC2晶体中含阴离子为C22-,6.4克CaC2为0.1mol;
D.氨气与氯气发生反应,氨气过量:3Cl2+8NH3═6NH4Cl+N2;氨气少量:3Cl2+2NH3═6HCl+N2;
解答 解:A.6.4gCu与足量的硫反应生成0.1mol硫化亚铜,转移电子数为0.1 NA,故A错误;
B.32g O2物质的量为1mol,32gO3的物质的量小于1mol,则32g O2和O3的混合气体含有的分子总数小于NA,故B正确;
C.CaC2晶体中含阴离子为C22-,阳离子为Ca2+,6.4克CaC2为0.1mol,含有离子数目0.2NA,故C错误;
D.氨气与氯气混合反应时,若氨气足量,则生成氮气和氯化氨,气体分子数减小;若氯气足量,则生成氮气和氯化氢,气体分子数增加,故D错误;
故选:B.
点评 本题考查了阿伏伽德罗常数的有关计算,熟练掌握公式的使用和物质的结构是解题关键,注意铜与硫反应生成硫化亚铜,题目难度不大.

练习册系列答案
 世纪百通期末金卷系列答案
世纪百通期末金卷系列答案
相关题目
4.中国科学家屠呦呦因创制了具有国际影响的新型抗疟药-青蒿素和双氢青蒿素,获得2015年诺贝尔生理学或医学奖.青蒿素的结构如图所示,下列关于青蒿素的说法错误的是( )

| A. | 难溶于水,易溶于乙醚 | |
| B. | 可与NaOH溶液发生水解反应 | |
| C. | 其同分异构体不可能有芳香族化合物 | |
| D. | 分子中含有的官能团是过氧键、醚键和酯基 |
18.把过量CO2气体通入下列溶液中,不会变浑浊的是( )
| A. | 澄清石灰水 | B. | 水玻璃 | C. | 苯酚钠 | D. | NaAl(OH)4 |
15.下列关系不正确的是( )
| A. | 原子半径:C>Si | B. | 热稳定性:HF>HBr | C. | 还原性:S2->C1- | D. | 酸性:HNO3>H3PO4 |
16.下列物质依次按照混合物、氧化物、弱电解质和非电解质的顺序排列的一组是( )
| A. | 淀粉、CuO、HClO、Cu | |
| B. | 水玻璃、Na2O•CaO•6SiO2、Na2O、SO3 | |
| C. | KAl(SO4)2•12H2O、KClO3、NH3•H2O、CH3CH2OH | |
| D. | 普通玻璃、H2O、CH3COOH、葡萄糖 |
17.下列相关实验的操作或结论正确的是( )
| A. | 将某气体通入溴水中,溴水颜色褪去,该气体一定是乙烯 | |
| B. | 制硝基苯时温度计水银球在反应液中 | |
| C. | 用酸性高锰酸钾溶液既可鉴别CH4和C2H4,又可除去CH4中的C2H4 | |
| D. | 在提纯鸡蛋中的蛋白质时,可向鸡蛋清溶液中加入浓(NH4)2SO4溶液,然后将所得沉淀滤出,即得较纯的蛋白质 |
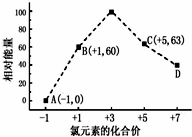 一定条件下,在水溶液中1mol Cl-、ClOX-(x=1,2,3,4)的能量(KJ)相对大小如图所示.回答下列问题:
一定条件下,在水溶液中1mol Cl-、ClOX-(x=1,2,3,4)的能量(KJ)相对大小如图所示.回答下列问题: