题目内容
4.中国科学家屠呦呦因创制了具有国际影响的新型抗疟药-青蒿素和双氢青蒿素,获得2015年诺贝尔生理学或医学奖.青蒿素的结构如图所示,下列关于青蒿素的说法错误的是( )
| A. | 难溶于水,易溶于乙醚 | |
| B. | 可与NaOH溶液发生水解反应 | |
| C. | 其同分异构体不可能有芳香族化合物 | |
| D. | 分子中含有的官能团是过氧键、醚键和酯基 |
分析 A.该分子中没有亲水基,只有憎水基,根据相似相溶原理判断其溶解性;
B.酯基能发生水解反应;
C.有机物含有5个环,1个C=O键,不饱和度为6,苯环的不饱和度是4;
D.该分子中的官能团是酯基、醚键和过氧键.
解答 解:A.该分子中没有亲水基,只有憎水基,根据相似相溶原理知,该物质不易溶于水,易溶于有机溶剂乙醚,故A正确;
B.酯基能发生水解反应,该分子中含有酯基,所以能与NaOH溶液发生水解反应,故B正确;
C.有机物含有5个环,1个C=O键,不饱和度为6,苯环的不饱和度是4,所以该有机物的同分异构体中可能含有苯环,故C错误;
D.根据图知,该分子中的官能团是酯基、醚键和过氧键三种官能团,故D正确;
故选C.
点评 本题考查有机物结构和性质,为高频考点,侧重考查学生分析判断能力,明确官能团的性质是解本题关键,注意不饱和度的计算方法,环的不饱和度是1、双键的不饱和度是1,题目难度不大.

练习册系列答案
相关题目
14.下列实验能达到目的是( )
| A. | 将NH4Cl溶液蒸干灼烧制备NH4Cl固体 | |
| B. | 只滴加氨水鉴别NaCl、AlCl3、MgCl2、Na2SO4四种溶液 | |
| C. | 用可见光束照射以区别溶液和胶体 | |
| D. | 用分液的方法分离酒精和水的混合物 |
15.下列有关化学用语的表示方法中正确的是( )
| A. | H2O2的电子式: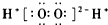 | |
| B. | CO2分子的结构式:O═C═O | |
| C. | 原子核内有8个中子的碳原子:${\;}_8^{14}C$ | |
| D. | 氯化钾的分子式:KCl |
12.下列关于卤素的说法中,正确的是( )
| A. | 单质的密度随核电荷数的增加逐渐减小 | |
| B. | 单质的颜色随核电荷数的增加而逐渐变浅 | |
| C. | 单质的氧化性随核电荷数的增加而逐渐减弱 | |
| D. | 氢化物的稳定性随核电荷数的增加逐渐增强 |
9.烟气中含有SO2等大量有害的物质,烟气除硫的方法有多种,其中石灰石法烟气除硫工艺的主要反应如下:
Ⅰ.CaCO3(s)?CO2(g)+CaO(s)△H=+178.2kJ/mol
Ⅱ.SO2(g)+CaO(s)?CaSO3(s)△H=-402kJ/mol
Ⅲ.2CaSO3(s)+O2(g)+4H2O(l)?2[CaSO4•2H2O](s)△H=-234.2kJ/mol
(1)试写出由石灰石、二氧化硫、氧气和水反应生成生石膏的热化学方程式2CaCO3(s)+O2(g)+2SO2(g)+4H2O(l)?2[CaSO4.2H2O](s)+2CO2(g)△H=-681.8kJ/mol.
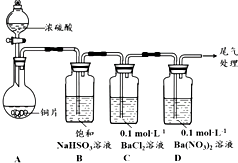
甲乙两同学分别对含+4价硫元素的物质性质进行了探究.
(2)甲用右图装置进行实验(气密性已检验,加热和夹持装置已略去).实验进行一段时间后,C、D中都出现明显的白色沉淀,经检验均为BaSO4.
①A中反应的化学方程式是Cu+2H2SO4(浓)$\frac{\underline{\;\;△\;\;}}{\;}$CuSO4+SO2↑+2H2O.
②为探究SO2在D中所发生的反应,甲进一步实验发现,出现白色沉淀的过程中,D溶液中NO3-浓度几乎不变.甲据此得出结论:D中出现白色沉淀的主要原因是酸性条件下,含+4价硫元素物质(SO2或H2SO3)被O2氧化生成SO42-.
(3)乙用如下实验对含+4价硫元素的物质性质继续进行探究.
①用化学方程式解释实验1中产生现象的原因:2H++SO32-═SO2+H2O,2SO2+O2+2Ba2++2H2O═2BaSO4↓+4H+或2H2SO3+O2+2Ba2+═2BaSO4↓+4H+.
②由实验1、2、3对比,可以得到推论含+4价硫元素物质可被O2和浓HNO3氧化.
③乙通过查阅资料发现,Na+对实验1和2中出现浑浊的时间无影响,于是进一步探究Cl-和NO3-对其的影响:
i.实验2和4对比,乙获得推论:Cl-的存在可以加快溶液中+4价硫元素的氧化;
ii.实验1和4对比,乙获得推论:硝酸根离子减慢+4价硫的化合物的氧化;.
(4)已知,25℃时,BaSO4的Ksp为1×10-10,硫酸钡的溶解度约是2.33×10-4g.
Ⅰ.CaCO3(s)?CO2(g)+CaO(s)△H=+178.2kJ/mol
Ⅱ.SO2(g)+CaO(s)?CaSO3(s)△H=-402kJ/mol
Ⅲ.2CaSO3(s)+O2(g)+4H2O(l)?2[CaSO4•2H2O](s)△H=-234.2kJ/mol
(1)试写出由石灰石、二氧化硫、氧气和水反应生成生石膏的热化学方程式2CaCO3(s)+O2(g)+2SO2(g)+4H2O(l)?2[CaSO4.2H2O](s)+2CO2(g)△H=-681.8kJ/mol.

甲乙两同学分别对含+4价硫元素的物质性质进行了探究.
(2)甲用右图装置进行实验(气密性已检验,加热和夹持装置已略去).实验进行一段时间后,C、D中都出现明显的白色沉淀,经检验均为BaSO4.
①A中反应的化学方程式是Cu+2H2SO4(浓)$\frac{\underline{\;\;△\;\;}}{\;}$CuSO4+SO2↑+2H2O.
②为探究SO2在D中所发生的反应,甲进一步实验发现,出现白色沉淀的过程中,D溶液中NO3-浓度几乎不变.甲据此得出结论:D中出现白色沉淀的主要原因是酸性条件下,含+4价硫元素物质(SO2或H2SO3)被O2氧化生成SO42-.
(3)乙用如下实验对含+4价硫元素的物质性质继续进行探究.
| 序号 | 实验操作 | 实验现象 |
| 1 | 取0.3g 纯净Na2SO3固体,向其中加入10mL2mol•L-1盐酸,再滴入4滴BaCl2溶液 | 产生无色气泡;滴入BaCl2溶液后,开始无现象,4min后,溶液变浑浊 |
| 2 | 取0.3g 纯净Na2SO3固体,向其中加入10mL 2mol•L-1 HNO3,再滴入4滴BaCl2溶液 | 产生无色气泡;滴入BaCl2溶液后,开始无现象,2h后,溶液变浑浊 |
| 3 | 取0.3g 纯净Na2SO3固体,向其中加入10mL 浓HNO3,再滴入4滴BaCl2溶液 | 产生红棕色气体;滴入BaCl2溶液后,溶液立即产生大量白色沉淀 |
②由实验1、2、3对比,可以得到推论含+4价硫元素物质可被O2和浓HNO3氧化.
③乙通过查阅资料发现,Na+对实验1和2中出现浑浊的时间无影响,于是进一步探究Cl-和NO3-对其的影响:
| 序号 | 实验操作 | 实验现象 |
| 4 | 取固体混合物,向其中加入10mL2mol•L-1 HNO3,再滴入4滴BaCl2溶液 | 产生无色气泡;滴入BaCl2溶液后,开始无现象,20min后,溶液变浑浊 |
ii.实验1和4对比,乙获得推论:硝酸根离子减慢+4价硫的化合物的氧化;.
(4)已知,25℃时,BaSO4的Ksp为1×10-10,硫酸钡的溶解度约是2.33×10-4g.
16.下列各组溶液,只用试管和胶头滴管就可以鉴别的是( )
①AlCl3溶液和NaOH溶液
②Ca(HCO3)2溶液和NaOH溶液
③NaAlO2溶液和盐酸
④Al2(SO4)3溶液和氨水
⑤AgNO3溶液和氨水.
①AlCl3溶液和NaOH溶液
②Ca(HCO3)2溶液和NaOH溶液
③NaAlO2溶液和盐酸
④Al2(SO4)3溶液和氨水
⑤AgNO3溶液和氨水.
| A. | ①③⑤ | B. | ①②③ | C. | ②③④ | D. | ③④⑤ |
6.已知弱酸的电离平衡常数如下表:下列选项正确的是( )
| 弱酸 | H2CO3 | 水杨酸(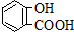 ) ) |
| 电离平衡常数(25℃) | Ka1=4.3×10-7 Ka2=5.6×10-11 | Ka1=1.3×10-3 Ka2=1.1×10-11 |
| A. | 常温下,等浓度、等体积的NaHCO3溶液pH小于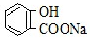 溶液pH 溶液pH | |
| B. | 常温下,等浓度、等体积的Na2CO3溶液和  溶液中所含离子总数前者小于后者 溶液中所含离子总数前者小于后者 | |
| C. |  +2NaHCO3→ +2NaHCO3→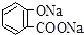 +2H2O+2CO2↑ +2H2O+2CO2↑ | |
| D. |  最多可与2molCO2反应 最多可与2molCO2反应 |
7.若NA表示阿伏加德罗常数的值,下列说法正确的是( )
| A. | 6.4gCu与足量的硫反应,转移电子数为0.2 NA | |
| B. | 通常情况下,32g O2和O3的混合气体含有的分子总数小于NA | |
| C. | 6.4g CaC2中含有的离子总数目为0.3NA | |
| D. | 标准状况下,将分子总数为NA的NH3和Cl2充分混合后,所得混合气体体积约为22.4L |