题目内容
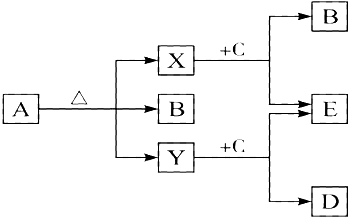
19.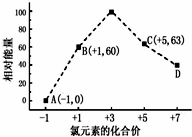 一定条件下,在水溶液中1mol Cl-、ClOX-(x=1,2,3,4)的能量(KJ)相对大小如图所示.回答下列问题:
一定条件下,在水溶液中1mol Cl-、ClOX-(x=1,2,3,4)的能量(KJ)相对大小如图所示.回答下列问题:(1)D是ClO4-(填离子符号).
(2)B→A+C反应的离子方程式为:3ClO-=ClO3-+2Cl-;生成1molC时,放出117KJ的热(填吸收或放出以及具体数值).
分析 (1)由图可知,D中Cl元素的化合价为+7价;
(2)结合Cl元素的化合价可知B→A+C反应为3ClO-=ClO3-+2Cl-,生成1molC时能量变化为3×60kJ-63kJ-0=117kJ,以此来解答.
解答 解:(1)由图可知,D中Cl元素的化合价为+7价,则D为ClO4-,故答案为:ClO4-;
(2)结合Cl元素的化合价可知B→A+C反应为3ClO-=ClO3-+2Cl-,生成1molC时能量变化为3×60kJ-63kJ-0=117kJ,反应物总能量大于生成物总能量,该反应放出117kJ热量,故答案为:3ClO-=ClO3-+2Cl-;放出117.
点评 本题考查含氯微粒及能量变化,为高频考点,把握微粒中元素的化合价及图中能量变化为解答的关键,侧重分析与迁移应用能力的考查,注意图象的分析与应用,题目难度不大.

练习册系列答案
相关题目
16.下列各组溶液,只用试管和胶头滴管就可以鉴别的是( )
①AlCl3溶液和NaOH溶液
②Ca(HCO3)2溶液和NaOH溶液
③NaAlO2溶液和盐酸
④Al2(SO4)3溶液和氨水
⑤AgNO3溶液和氨水.
①AlCl3溶液和NaOH溶液
②Ca(HCO3)2溶液和NaOH溶液
③NaAlO2溶液和盐酸
④Al2(SO4)3溶液和氨水
⑤AgNO3溶液和氨水.
| A. | ①③⑤ | B. | ①②③ | C. | ②③④ | D. | ③④⑤ |
10.关于有机物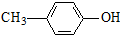 的叙述错误的是( )
的叙述错误的是( )
 的叙述错误的是( )
的叙述错误的是( )| A. | 分子式为C7H10O | B. | 含有羟基 | C. | 能发生加成反应 | D. | 含有苯环结构 |
7.若NA表示阿伏加德罗常数的值,下列说法正确的是( )
| A. | 6.4gCu与足量的硫反应,转移电子数为0.2 NA | |
| B. | 通常情况下,32g O2和O3的混合气体含有的分子总数小于NA | |
| C. | 6.4g CaC2中含有的离子总数目为0.3NA | |
| D. | 标准状况下,将分子总数为NA的NH3和Cl2充分混合后,所得混合气体体积约为22.4L |
4.下表是元素周期表的一部分,请用化学用语回答:
(1)最高价氧化物对应的水化物中酸性最强的是HClO4.
(2)实验室制取②的氢化物的化学方程式2NH4Cl+Ca(OH)2$\frac{\underline{\;\;△\;\;}}{\;}$CaCl2+2NH3↑+2H2O.
(3)④和⑤元素最高价氧化物对应的水化物相互反应的化学方程式NaOH+Al(OH)3=NaAlO2+2H2O.
(4)元素②、⑥与氢元素形成的一种化合物含有的化学键类型有离子键、共价键,其电子式为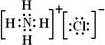 .
.
| 主族 周期 | IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 |
| 二 | ① | ② | ③ | |||||
| 三 | ④ | ⑤ | ⑥ | ⑦ | ||||
| 四 | ⑧ | ⑨ |
(2)实验室制取②的氢化物的化学方程式2NH4Cl+Ca(OH)2$\frac{\underline{\;\;△\;\;}}{\;}$CaCl2+2NH3↑+2H2O.
(3)④和⑤元素最高价氧化物对应的水化物相互反应的化学方程式NaOH+Al(OH)3=NaAlO2+2H2O.
(4)元素②、⑥与氢元素形成的一种化合物含有的化学键类型有离子键、共价键,其电子式为
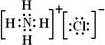 .
.
8.下列关于碱金属某些性质的排列中正确的是( )
| A. | 密度:Li<Na<K<Rb<Cs | B. | 熔点、沸点:Li<Na<K<Rb<Cs | ||
| C. | 原子半径:Li<Na<K<Rb<Cs | D. | 氧化性:Li+<Na+<K+<Rb+<Cs+ |
 ④CH3COOH⑤HOCH2CHO ⑥CH3CH2CH2CH3⑦葡萄糖 ⑧蛋白质⑨淀粉
④CH3COOH⑤HOCH2CHO ⑥CH3CH2CH2CH3⑦葡萄糖 ⑧蛋白质⑨淀粉