题目内容
14.在铁与铜的混合物中,加入一定量的稀硝酸,微热,充分反应后,剩余金属a g,再向其中加入一定量的稀HCl,微热,充分反应后剩余金属b g( )| A. | a可能等于b | B. | a一定大于b | C. | a可能大于b | D. | a一定等于b |
分析 反应后溶液中存在大量的NO3-,加入盐酸,在酸性条件下NO3-与金属继续反应,则剩余金属进一步溶解,以此解答.
解答 解:在Fe,Cu的混合物中加入一定量的稀硝酸并微热,充分反应后剩余金属a克,该金属可能为Fe、Cu或二者的混合物,溶液中一定存在NO3-,加入盐酸,在酸性条件下NO3-与金属继续反应,则剩余金属进一步溶解,则有a一定大于b,
故选B.
点评 本题考查混合物的计算,题目难度不大,注意NO3-在酸性条件下的性质.

练习册系列答案
相关题目
5.如表是A、B、C、D、E五种有机物的有关信息:
回答下列问题:
(1)B具有的性质是②③(填序号).
①无色无味液体 ②有毒 ③不溶于水 ④密度比水大
⑤与酸性KMnO4溶液和溴水反应褪色 ⑥任何条件下不与氢气反应
(2)写出结构简式
ACH2=CH2 CCH3CH2OH DCH3CHO
(3)判断E可能具有的性质是ABCDE(填字母)
A、能使酸性高锰酸钾褪色B、能使溴水褪色C、能与氢氧化钠反应 D、能与钠反应 E、能发生酯化反应.
| A | ①能使溴的四氯化碳溶液褪色;②比例模型为 ;③能与水在一定条件下反应生成C ;③能与水在一定条件下反应生成C |
| B | ①由C、H两种元素组成;②球棍模型为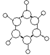 |
| C | ①由C、H、O三种元素组成;②能与Na反应,但不能与NaOH溶液反应;③能与E反应生成相对分子质量为100的酯 |
| D | ①相对分子质量比C少2;②能由C氧化而成 |
| E | ①由C、H、O三种元素组成;②球棍模型为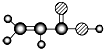 |
(1)B具有的性质是②③(填序号).
①无色无味液体 ②有毒 ③不溶于水 ④密度比水大
⑤与酸性KMnO4溶液和溴水反应褪色 ⑥任何条件下不与氢气反应
(2)写出结构简式
ACH2=CH2 CCH3CH2OH DCH3CHO
(3)判断E可能具有的性质是ABCDE(填字母)
A、能使酸性高锰酸钾褪色B、能使溴水褪色C、能与氢氧化钠反应 D、能与钠反应 E、能发生酯化反应.
2.热化学方程式C(s)+H2O(g)=CO(g)+H2(g)△H=+131.3kJ/mol表示( )
| A. | 碳和水反应吸收131.3kJ 能量 | |
| B. | 1mol 碳和1mol 水反应生成一氧化碳和氢气并吸收131.3kJ 热量 | |
| C. | 1mol 固态碳和1mol 水蒸气反应生成一氧化碳气体和氢气,并吸热131.3kJ | |
| D. | 1 个固态碳原子和1 分子水蒸气反应吸热131.1kJ |
3.下列关于水的叙述错误的是( )
| A. | 自然界中的水都是混合物 | B. | 工业废水可直接排放 | ||
| C. | 水是生命活动不可缺少的物质 | D. | 肥皂水可以区分软水和硬水 |
4.下列物质中既含有共价键又含有离子键的是( )
| A. | C2H6 | B. | HNO3 | C. | Na2O | D. | KOH |
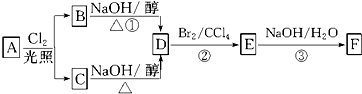
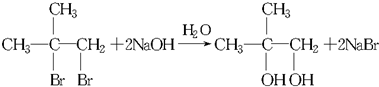 .
.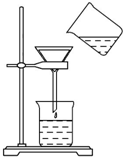 将含有少量氯化钾的硝酸钾固体提纯,某学生进行如图所示实验操作.回答下列问题:
将含有少量氯化钾的硝酸钾固体提纯,某学生进行如图所示实验操作.回答下列问题: