题目内容
3.下列关于水的叙述错误的是( )| A. | 自然界中的水都是混合物 | B. | 工业废水可直接排放 | ||
| C. | 水是生命活动不可缺少的物质 | D. | 肥皂水可以区分软水和硬水 |
分析 可以根据水的组成、性质、水的污染、软水和硬水的鉴别等方面进行分析、判断,从而得出正确的结论.
解答 解:A、自然界中的水都含有可溶性或者不溶性的杂质,都是混合物,故A正确;
B、工业废水含有有毒、有害物质,直接排放会污染水资源和土壤,故B错误;
C、水是生命活动不可缺少的物质,故C正确;
D、区分软水和硬水可用肥皂水,软水遇到肥皂水产生较多泡沫,故D正确;
故选B.
点评 本题难度不大,考查有关水的知识点,有利于学生通过题目对水的有关知识进行归纳总结,掌握基础知识点即可轻松解题.

练习册系列答案
 名校练考卷期末冲刺卷系列答案
名校练考卷期末冲刺卷系列答案
相关题目
13.某饱和一元醛发生银镜反应时可以析出21.6g银,等量的醛完全燃烧可以产生8.96LCO2(标准状况),则该醛为( )
| A. | 乙醛 | B. | 甲醛 | C. | 丙醛 | D. | 丁醛 |
14.在铁与铜的混合物中,加入一定量的稀硝酸,微热,充分反应后,剩余金属a g,再向其中加入一定量的稀HCl,微热,充分反应后剩余金属b g( )
| A. | a可能等于b | B. | a一定大于b | C. | a可能大于b | D. | a一定等于b |
11.把铝粉与Fe3O4的混合物,分为两等份.前一份在高温下恰好完全反应,之后将生成物与足量盐酸充分反应;后一份直接加入足量NaOH溶液充分反应.前后两种情况下生成的气体在同温同压下的体积比是( )
| A. | 1:1 | B. | 3:4 | C. | 9:8 | D. | 4:3 |
18.下列实验中,不能观察到明显变化的是( )
| A. | 把一段打磨过的镁条放入少量冷水中 | |
| B. | 把Cl2通入FeBr2溶液中 | |
| C. | 把绿豆大的钾投入水中 | |
| D. | 把溴水滴加到KI淀粉溶液中 |
8.实现“低碳经济”的一种策略是节约能源.下列制备氢气的方法最节能的是( )
| A. | 电解水:2H2O $\frac{通电}{\;}$2H2↑+O2↑ | |
| B. | 焦炭与水蒸气反应:C+H2O$\frac{\underline{\;高温\;}}{\;}$H2+CO | |
| C. | 太阳光分解水:2H2O$\frac{TiO_{2}}{太阳光}$2H2↑+O2↑ | |
| D. | 天然气与水蒸气反应:CH4+H2O $\frac{高温}{\;}$CO+3H2 |
15.实验室有四瓶失去标签的无色透明液体,它们分别是稀硫酸、NaOH溶液、Na2CO3溶液和酚酞溶液.已知碳酸钠溶液遇酚酞溶液变红.化学小组为了确定每瓶溶液的成分,将它们分别标记为①、②、③、④后进行实验,实验现象记录如下:
根据以上实验现象,回答下列问题:
(1)实验1中,③中发生反应的化学方程式是Na2CO3+H2SO4=Na2SO4+CO2↑+H2O.
(2)溶液①为NaOH,溶液②为酚酞,溶液④为稀H2SO4.
(3)分析解释实验3中的实验现象此空多余.
②中“红色变为无色”的原因:稀硫酸中和NaOH溶液.
③中“先无明显现象,之后有气泡产生”的原因:稀硫酸先与NaOH反应,然后再与Na2CO3溶液反应.
| 实验过程 | 实验现象 |
| 实验1:分别将①、②、③取样于三支试管中,再分别加入溶液④ | ①②无明显变化,③有气泡产生 |
| 实验2:分别将②、③、④取样于三支试管中,再分别加入溶液① | ③、④无明显变化,②溶液变红 |
| 实验3:分别向实验2的三支试管中,继续滴加入足量溶液④ | ④无明显变化,②溶液变红变为无色,③中先无明显现象,之后有气泡产生 |
(1)实验1中,③中发生反应的化学方程式是Na2CO3+H2SO4=Na2SO4+CO2↑+H2O.
(2)溶液①为NaOH,溶液②为酚酞,溶液④为稀H2SO4.
(3)分析解释实验3中的实验现象此空多余.
②中“红色变为无色”的原因:稀硫酸中和NaOH溶液.
③中“先无明显现象,之后有气泡产生”的原因:稀硫酸先与NaOH反应,然后再与Na2CO3溶液反应.
12.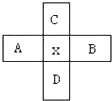 原子序数为x的元素在周期表中位于A、B、C、D四种元素的中间,A、B、C、D四种元素的原子序数之和如图所示,其中不可能的是(La系、Ac系、0族元素除外)( )
原子序数为x的元素在周期表中位于A、B、C、D四种元素的中间,A、B、C、D四种元素的原子序数之和如图所示,其中不可能的是(La系、Ac系、0族元素除外)( )
 原子序数为x的元素在周期表中位于A、B、C、D四种元素的中间,A、B、C、D四种元素的原子序数之和如图所示,其中不可能的是(La系、Ac系、0族元素除外)( )
原子序数为x的元素在周期表中位于A、B、C、D四种元素的中间,A、B、C、D四种元素的原子序数之和如图所示,其中不可能的是(La系、Ac系、0族元素除外)( )| A. | 4x | B. | 4x+6 | C. | 4x+10 | D. | 4x+14 |