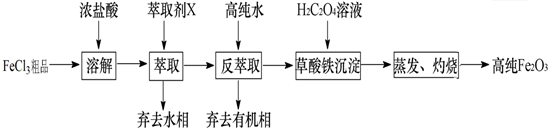
题目内容
3.(I)在一个容积固定不变的密闭容器中进行反应:2X(g)+Y(g)?2Z(g),已知将2molX和1molY充入该容器中,反应在绝热条件下达到平衡时,Z的物质的量为pmol.回答下列问题: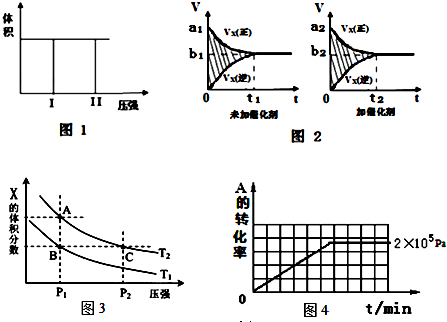
(1)若把2molX和1molY充入该容器时,处于状态I,达到平衡时处于状态II(如图1),则该反应的△H< 0; 熵变△S<0 ( 填:“<,>,=”).该反应在低温(填高温或低温)条件下能自发进行.
该反应的v-t图象如图2中甲图所示.若其他条件不变,仅在反应前加入合适的催化剂,则其v-t图象如图2中乙图所示.以下说法正确的是②③⑤
①a1>a2 ②b1<b2 ③t1>t2 ④右图中阴影部分面积更大⑤两图中阴影部分面积相等
(3)若该反应在容积可变的密闭容器中发生,在温度为T1、T2时,平衡体系中X的体积分数随压强变化曲线如图3所示.下列说法正确的是BD.
A.A、C两点的反应速率:A>C B.A、C两点的气体密度:A<C
C.B、C两点的气体的平均相对分子质量:B<C D.由状态B到A,可以用加热的方法
(II)在容积可变的密闭容器中发生反应:mA(g)+nB(g)?pC(g),在一定温度和不同压强下达到平衡时,分别得到A的物质的量浓度如下表
| 压强p/Pa | 2×105 | 5×105 | 1×106 |
| c(A)/mol•L-1 | 0.08 | 0.20 | 0.44 |
(2)其他条件相同时,在上述三个压强下分别发生该反应.2×105 Pa时,A的转化率随时间变化如图4,请在图4中补充画出压强分别为5×105 Pa 和1×106 Pa时,A的转化率随时间的变化曲线(请在图4上画出曲线并标出相应压强).
分析 (Ⅰ)(1)由图可知状态Ⅱ的压强大于状态Ⅰ压强的2倍,所以平衡逆向移动;根据反应前后气体的变化判断;△H-T△S<0反应自发进行;
(2)加入催化剂,反应速率加快,到达平衡的时间缩短,所以平衡不移动;
(3)A. 根据压强判断A、C两点的反应速率;
B. 压强越大,体积越小,密度越大;
C. B、C两点的X的体积分数相同,则气体物质的量相同,所以气体的平均相对分子质量相同;
D. 由状态B到状态A,压强相同,温度不同;
(Ⅱ)(1)根据压强变化与浓度变化关系分析;反应前后气体的物质的量不变;
(2)2×105与5×105 Pa时A的转化率不变,反应时间缩短,1×106 Pa时,A的转化率减小,反应速率增大时间缩短.
解答 解:(Ⅰ)(1)由图可知状态Ⅱ的压强大于状态Ⅰ压强的2倍,所以平衡逆向移动,反应在绝热条件下进行,逆向进行,说明正反应为放热反应;已知2X(g)+Y(g)?2Z(g),反应后气体的物质的量减少,所以混乱度减小,△S<0,△H-T△S<0反应自发进行,该反应在低温条件下能自发进行,
故答案为:<;<;低温;
(2)加入催化剂,反应速率加快,所以b1<b2,到达平衡的时间缩短,所以t1>t2,平衡不移动,则两图中阴影部分面积相等,
故答案为:②③⑤;
(3)A. 已知压强A点小于C点,压强越大速率越快,所以反应速率A<C,故A错误;
B. 压强越大,体积越小,密度越大,所以气体密度:A<C,故B正确;
C. B、C两点的X的体积分数相同,则气体物质的量相同,所以气体的平均相对分子质量相同,故C错误;
D. 由状态B到状态A,压强相同,温度不同,所以可以通过升温使状态B到状态A,故D正确;
故答案为:BD;
(Ⅱ)(1)由表格数据可知当压强从2×105Pa增大为5×105Pa时,压强增大2.5倍,体积变为$\frac{1}{2.5}$倍,浓度由0.08增大为0.20mol•L-1,也增大2.5倍,所以增大压强平衡不移动,由(1)可知,增大压强平衡不移动,所以反应前后气体的物质的量不变,所以当反应达到平衡状态时,体系中共有amol气体,再向体系中加入bmolB,当重新达到平衡时,体系中气体总物质的量是a+b,故答案为:不;a+b;
(2)2×105与5×105 Pa时A的转化率不变,反应时间缩短,1×106 Pa时,平衡逆移,A的转化率减小,反应速率增大,时间缩短,依此作图为: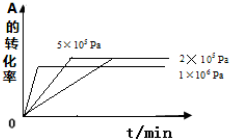 ,故答案为:
,故答案为: .
.
点评 本题考查了平衡常数、平衡移动、平衡图象等,综合性较强,难度中等,注意对图象和表格数据的分析是解题的关键,考查了学生分析图象提取图象信息的能力.

| A. | CuSO4溶液 | B. | Na2CO3溶液 | C. | Fe(OH)3胶体 | D. | Ba(OH)2溶液 |
| A. | 向Na2SiO3溶液中通入过量CO2:SiO32-+2CO2+2H2O═2HCO3-+H2SiO3↓ | |
| B. | 少量SO2通入漂白粉溶液中:SO2+H2O+Ca2++2ClO-═CaSO3↓+2HClO | |
| C. | 用稀HNO3溶解FeS固体:FeS+2H+═Fe2++H2S↑ | |
| D. | 向NH4HCO3溶液中加入足量Ba(OH)2溶液:2HCO3-+Ba2++2OH-═BaCO3↓+CO32-+2H2O |
 冬青油又叫水杨酸甲酯,是一种重要的有机合成原料.某化学小组用水杨酸(
冬青油又叫水杨酸甲酯,是一种重要的有机合成原料.某化学小组用水杨酸(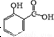 )和甲醇在酸性催化剂催化下合成水杨酸甲酯并计算其产率.
)和甲醇在酸性催化剂催化下合成水杨酸甲酯并计算其产率.实验步骤:
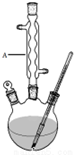
Ⅰ.如图,在三颈烧瓶中加入13.8g (0.1mol)水杨酸和24g(30mL,0.75mol)甲醇,向混合物中加入约10mL甲苯(甲苯与水形成的共沸物,沸点为85℃,该实验中加入甲苯,易将水蒸出),再小心地加入5mL浓硫酸,摇动混匀,加入1~2粒沸石,组装好实验装置,在85~95℃下恒温加热反应1.5小时:
Ⅱ.待装置冷却后,分离出甲醇,然后转移至分液漏斗,依次用少量水、5%NaHCO3溶液和水洗涤;分出的产物加入少量无水MgSO4固体,过滤得到粗酯;
Ⅲ.将粗酯进行蒸馏,收集221℃~224℃的馏分,得水杨酸甲酯9.12g.
常用物理常数:
| 名称 | 分子量 | 颜色状态 | 相对密度 | 熔点(℃) | 沸点(℃) |
| 水杨酸甲酯 | 152 | 无色液体 | 1.18 | -8.6 | 224 |
| 水杨酸 | 138 | 白色晶体 | 1.44 | 158 | 210 |
| 甲醇 | 32 | 无色液体 | 0.792 | -97 | 64.7 |
(1)仪器A的名称是球形冷凝管,加入沸石的作用是防止暴沸.若加热后发现未加沸石,应采取的正确方法是停止加热,待冷却后加入.
(2)制备水杨酸甲酯时,最合适的加热方法是水浴加热.
(3)实验中加入甲苯对合成水杨酸甲酯的作用是加入甲苯易将水蒸出,使平衡向右移动,从而提高反应的产率.
(4)反应结束后,分离出甲醇采用的方法是蒸馏(或水洗分液).
(5)实验中加入无水硫酸镁的作用是除水或干燥.本实验的产率为60%(保留两位有效数字).
 化学兴趣小组的同学用0.100 0 mol/L 盐酸标准溶液测定某烧碱样品的纯度(杂质不与盐酸反应).实验步骤如下:
化学兴趣小组的同学用0.100 0 mol/L 盐酸标准溶液测定某烧碱样品的纯度(杂质不与盐酸反应).实验步骤如下:(1)配制待测液:用分析天平准确称取烧碱样品2.500 g,全部溶于水配制成500 mL溶液.配制溶液需用的玻璃仪器除了烧杯、胶头滴管外,还需要500mL容量瓶、量筒.
(2)滴定:
①用碱式滴定管量取20.00mL所配溶液放在锥形瓶中,滴加几滴指示剂,待测.滴定管在装入反应液之前应进行的操作有检查滴定管是否漏水,洗净并用待盛装的溶液润洗滴定管2~3次.
②用浓度为0.100 0mol/L的盐酸标准溶液进行滴定.开始滴定前的一步操作是调节液面于“0”刻度或“0”刻度以下.
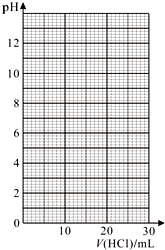
③滴定过程中用pH计测定锥形瓶中溶液的pH,临近滴定终点时每滴一滴测一次pH.滴定过程中,测得锥形瓶中溶液的pH变化如下表:
| V(HCl)/mL | 0.00 | 12.00 | 18.00 | 22.00 | 23.00 | 23.96 |
| pH | 13.1 | 12.6 | 12.2 | 11.7 | 11.4 | 9.9 |
| V(HCl)/mL | 24.00 | 24.04 | 25.00 | 26.00 | 30.00 | |
| pH | 7.0 | 4.0 | 2.7 | 2.4 | 1.9 |
①在坐标图中绘出上述中和滴定曲线.
②所测样品中NaOH的质量百分含量为96%.
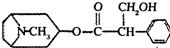
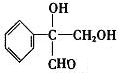 或
或 ;
;