题目内容
17. 下列关于物质的分离提纯不正确的是( )
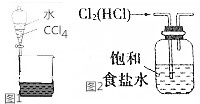
下列关于物质的分离提纯不正确的是( )| A. | 用如图1所示装置分离CCl4和水 | |
| B. | 除去苯中的少量苯酚,加入适量浓溴水,过滤 | |
| C. | 实验室用如图2所示装置除去Cl2中的少量HCl | |
| D. | 除去O2中混有得得少量SO2,可将混合气体依次通过盛有酸性KMnO4溶液、浓硫酸的洗气瓶 |
分析 A.CCl4和水分层;
B.溴、三溴苯酚均易溶于苯;
C.HCl极易溶于水,食盐水抑制氯气的溶解;
D.SO2与高锰酸钾反应,氧气不能,且浓硫酸可干燥氧气.
解答 解:A.CCl4和水分层,则图中分液漏斗分液可分离,故A正确;
B.溴、三溴苯酚均易溶于苯,不能除杂,应选NaOH溶液、分液,故B错误;
C.HCl极易溶于水,食盐水抑制氯气的溶解,且导管长进短出可除杂,故C正确;
D.SO2与高锰酸钾反应,氧气不能,且浓硫酸可干燥氧气,则将混合气体依次通过盛有酸性KMnO4溶液、浓硫酸的洗气瓶可除杂,故D正确;
故选B.
点评 本题考查混合物分离提纯,为高频考点,把握物质的性质、性质差异、发生的反应及混合物分离方法为解答的关键,侧重分析与应用能力的考查,注意有机物性质的应用,题目难度不大.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
7.下列排列顺序正确的是( )
| A. | 稳定性:NH3<PH3<AsH3 | B. | 酸性:H2SO4>H3PO4>H2SiO3 | ||
| C. | 还原性:S 2-<Br -<Fe 2+ | D. | 电负性:Cl>P>S |
8.下列说法不正确的是( )
| A. | pH=13的NaOH溶液与pH=1的醋酸溶液等体积混合后所得溶液的pH>7 | |
| B. | 将等体积pH=4的盐酸和醋酸稀释成pH=5的溶液,醋酸所需加入的水量多 | |
| C. | 常温下,向氨水中逐滴滴入盐酸至溶液的pH=7,则混合液中:c(NH4+)=c(Cl-) | |
| D. | 0.2 mol•L-1的NaHCO3溶液中:c(Na+)>c(HCO3-)>c(OH-)>c(H+) |
5.能区别NaCl,MgCl2,AlCl3,FeCl3,NH4Cl溶液的一种试剂是( )
| A. | H2SO4溶液 | B. | AgNO3溶液 | C. | NaOH溶液 | D. | 氨水 |
3.(1)下表中有三组物质,每组均有甲、乙、丙三种物质(酸、碱、盐均为溶液).
根据该表回答问题:
第Ⅲ组中有一种物质与第Ⅰ组中的所有物质反应,这种物质是H2SO4.
第Ⅱ组物质中,跟第Ⅰ组所有物质都不能发生反应的是NaOH.
(2)双氧水H2O2可作为矿业废液消毒剂,可以消除采矿业废液中的氰化物(如KCN)化学方程式为:KCN+H2O2+H2O═KHCO3+A↑(已配平)①生成物A的化学式为NH3;②反应中被氧化的元素为C;③该反应中的氧化剂是H2O2.
(3)写出下列物质在水溶液里的电离方程式:硫酸铁Fe2(SO4)3=2Fe3++3SO42-,氯酸钾KClO3=K++ClO3-,NaHSO4在熔融状态下的电离方程式是NaHSO4=Na++HSO4-.
(4)下列说法中正确的是BD.
A.NaHSO4属于酸 B.NaHSO4属于酸式盐
C.NaHSO4溶液属于电解质 D.NaHSO4溶液能与Zn反应生成氢气
(5)Fe(OH)3胶体的制备方法在沸腾的蒸馏水中加入饱和氯化铁溶液,当溶液变为红褐色时立即停止加热.
| 第Ⅰ组 | 第Ⅱ组 | 第Ⅲ组 | |
| 甲 | BaCl2 | HCl | Cu(NO3)2 |
| 乙 | Fe2O3 | K2SO4 | H2SO4 |
| 丙 | Fe | NaOH | MgCl2 |
第Ⅲ组中有一种物质与第Ⅰ组中的所有物质反应,这种物质是H2SO4.
第Ⅱ组物质中,跟第Ⅰ组所有物质都不能发生反应的是NaOH.
(2)双氧水H2O2可作为矿业废液消毒剂,可以消除采矿业废液中的氰化物(如KCN)化学方程式为:KCN+H2O2+H2O═KHCO3+A↑(已配平)①生成物A的化学式为NH3;②反应中被氧化的元素为C;③该反应中的氧化剂是H2O2.
(3)写出下列物质在水溶液里的电离方程式:硫酸铁Fe2(SO4)3=2Fe3++3SO42-,氯酸钾KClO3=K++ClO3-,NaHSO4在熔融状态下的电离方程式是NaHSO4=Na++HSO4-.
(4)下列说法中正确的是BD.
A.NaHSO4属于酸 B.NaHSO4属于酸式盐
C.NaHSO4溶液属于电解质 D.NaHSO4溶液能与Zn反应生成氢气
(5)Fe(OH)3胶体的制备方法在沸腾的蒸馏水中加入饱和氯化铁溶液,当溶液变为红褐色时立即停止加热.
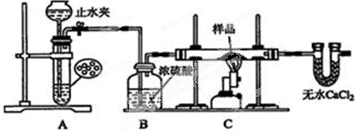
 .
.