题目内容
7.下列排列顺序正确的是( )| A. | 稳定性:NH3<PH3<AsH3 | B. | 酸性:H2SO4>H3PO4>H2SiO3 | ||
| C. | 还原性:S 2-<Br -<Fe 2+ | D. | 电负性:Cl>P>S |
分析 A.非金属性越强,对应氢化物的稳定性越强;
B.非金属性越强,最高价氧化物对应水合物的酸性越强;
C.对应粒子氧化物越强,其还原性越弱;
D.同一周期的元素,原子序数越大,电负性越强.
解答 解:A.同一主族元素,原子序数越大,非金属性越强,对应氢化物的稳定性越弱,则稳定性:NH3>PH3>AsH3,故A错误;
B.同一周期的元素,原子序数越大,非金属性越强,最高价氧化物对应水合物的酸性越强,则酸性:H2SO4>H3PO4>H2SiO3,故B正确;
C.氧化性:S<Fe3+<Br2,则对应离子的还原性:S2->Fe2+>Br-,故C错误;
D.Cl、P、S位于同一周期,原子序数逐渐增大,电负性逐渐增强,则电负性:Cl>S>P,故D错误;
故选B.
点评 本题考查了原子结构与元素周期律的应用,题目难度不大,明确元素周期律内容为解答关键,注意熟练掌握原子结构与元素周期律、元素周期表的关系,试题培养了学生的灵活应用能力.

练习册系列答案
 第1卷单元月考期中期末系列答案
第1卷单元月考期中期末系列答案
相关题目
9.设NA为阿伏加德罗常数的值,下列说法正确的是( )
| A. | 常温下,14g CO和N2的混合物含的原子数为NA | |
| B. | 1mol Fe发生氧化反应失去的电子数一定是3NA | |
| C. | 0.1mol•L-1 NaCl溶液中含的Cl-数是0.1NA | |
| D. | 0.1mol H2SO4与1L 0.1mol•L-1 NaOH溶液反应,生成的H2O分子数是0.2NA |
2.在下列四组物质的水溶液中,仅用一种化学品不能完成组内各种溶液的鉴别的是( )
| A. | Na2CO3、NaCl、AgNO3 | B. | Na2SO4、NaOH、HCl | ||
| C. | Na2SO4、NaNO3、NaOH | D. | Na2SO4、BaCl2、CuSO4 |
12.NA为阿伏伽德罗常数的值.下列说法正确的是( )
| A. | 2.4g镁在空气中完全燃烧生成MgO和Mg3N2,转移的电子数为0.8NA | |
| B. | 标准状况下,5.6L二氧化碳气体中含有的氧原子数为0.5NA | |
| C. | 8.7gMnO2与40mL 10mol/L的浓盐酸充分反应,生成的氯气分子数为0.1NA | |
| D. | 0.1L0.5mol/LCH3COOH溶液中含有的氢离子数为0.05NA |
16.下列各组物质相互混合,既有气体生成又有沉淀生成的是( )
①金属钠投入到CuSO4溶液中
②过量的NaOH溶液和明矾溶液
③NaAlO2溶液和NaHCO3溶液混合
④过量的Na2O2投入FeCl2溶液
⑤金属钠投入NH4Cl溶液中.
①金属钠投入到CuSO4溶液中
②过量的NaOH溶液和明矾溶液
③NaAlO2溶液和NaHCO3溶液混合
④过量的Na2O2投入FeCl2溶液
⑤金属钠投入NH4Cl溶液中.
| A. | ①④ | B. | ②③ | C. | ②③ | D. | ①⑤ |
17.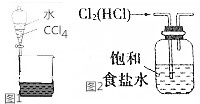 下列关于物质的分离提纯不正确的是( )
下列关于物质的分离提纯不正确的是( )
 下列关于物质的分离提纯不正确的是( )
下列关于物质的分离提纯不正确的是( )| A. | 用如图1所示装置分离CCl4和水 | |
| B. | 除去苯中的少量苯酚,加入适量浓溴水,过滤 | |
| C. | 实验室用如图2所示装置除去Cl2中的少量HCl | |
| D. | 除去O2中混有得得少量SO2,可将混合气体依次通过盛有酸性KMnO4溶液、浓硫酸的洗气瓶 |
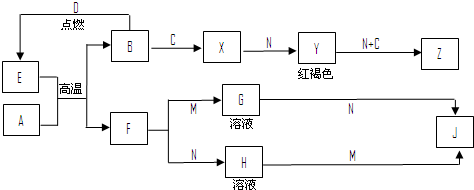
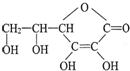 人体内的铁是以Fe2+ 和Fe3+的形式存在.正二价铁离子易被吸收,给贫血者补充铁时,应给予含Fe2+的亚铁盐,如硫酸亚铁.服用维生素C,可使食物中的Fe3+还原成Fe2+,有利于人体吸收.
人体内的铁是以Fe2+ 和Fe3+的形式存在.正二价铁离子易被吸收,给贫血者补充铁时,应给予含Fe2+的亚铁盐,如硫酸亚铁.服用维生素C,可使食物中的Fe3+还原成Fe2+,有利于人体吸收.