题目内容
18. Ⅰ.氢能的存储是氢能应用的主要瓶颈,配位氢化物、富氢载体化合物是目前所采用的主要储氢材料.
Ⅰ.氢能的存储是氢能应用的主要瓶颈,配位氢化物、富氢载体化合物是目前所采用的主要储氢材料.(1)Ti(BH4)2是一种过渡元素硼氢化物储氢材料.在基态Ti2+中,电子占据的最高能层符号为M,该能层具有的原子轨道数为9;
(2)液氨是富氢物质,是氢能的理想载体,利用N2+3H2?2NH3实现储氢和输氢.下列说法正确的是cd(填序号);
a.NH3分子中氮原子的轨道杂化方式为sp2杂化
b.NH4+与PH4+、CH4、BH4-、C1O4-互为等电子体
c.相同压强时,NH3的沸点比PH3的沸点高 d.[Cu(NH3)4]2+中N原子是配位原子
Ⅱ.卤族元素的单质和化合物很多,我们可以利用所学物质结构与性质的相关知识去认识和理解它们.
(3)ClO2-中心氯原子的杂化轨道类型为sp3,写出一个ClO2-的等电子体Cl2O或OF2.
(4)已知高碘酸有两种形式,化学式分别为H5IO6和HIO4,前者为五元酸,后者为一元酸.请比较二者酸性强弱:H5IO6<HIO4.(填“>”、“<”或“=”)
(5)碘在水中的溶解度虽然小,但在碘化钾溶液中溶解度却明显增大这是由于溶液中发生下列反应I-+I2=I3-.与KI3类似的,还有CsICl2等.已知CsICl2不稳定,受热易分解,倾向于生成晶格能更大的物质,则它按下列A式发生.
A.CsICl2=CsCl+ICl B.CsICl2=CsI+Cl2
III.氯化钠是生活中的常用调味品,也是结构化学中研究离子晶体时常用的代表物,其晶胞结构如图所示;
(6)设氯化钠晶体中Na+与跟它最近邻的Cl-之间的距离为r,则与该Na+次近邻的Cl-的个数为8,该Na+与跟它次近邻的Cl-之间的距离$\sqrt{3}$r;
(7)已知在氯化钠晶体中Na+的半径为a pm,Cl-的半径为b pm,它们在晶体中是紧密接触的,则在氯化钠晶体中离子的空间利用率为$\frac{2π}{3}×\frac{({a}^{3}+{b}^{3})}{(a+b)^{3}}×100%$.
分析 (1)写出Ti2+核外电子排布式,判断其最高能层和该能层下的原子轨道数;
(2)a.根据价层电子对互斥理论确定杂化方式;
b.等电子体为原子数相等和价电子数相等的原子团;
c.分子间存在氢键的熔沸点高;
d.提供孤电子对的原子是配原子;
(3)根据价层电子对互斥理论确定其杂化类型;等电子体是具有相同的价电子数和相同原子数的微粒;
(4)根据含氧酸中,酸的元数取决于羟基氢的个数,含非羟基氧原子个数越多,酸性越强;
(5)离子晶体的晶格能与离子半径成反比,与离子所带电荷成正比;
(6)根据NaCl晶体结构判断:Na+位于顶点与它次近邻的Cl-位于晶胞的体心位置,据此判断次近邻的Cl-数目和距离;
(7)NaCl晶胞为面心立方密堆积,则晶胞的边长为(2a+2b)pm,计算出Na+和Cl-所占体积和晶胞体积,从而计算出空间利用率.
解答 解:(1)基态Ti2+价电子排布式为:3d2,最高能层为M层,该能层下含有1个3s轨道、3个3p轨道和5个3d轨道,共有9个原子轨道,
故答案为:M;9;
(2)a.NH3分子中N原子含有3个共用电子对和一个孤电子对,所以其价层电子对是4,采用sp3杂化,故a错误;
b.等电子体为原子数相等和价电子数相等的原子团,NH+4与PH+4、CH4、BH-4均含有5个原子团,且价电子均为8,为等电子体,而ClO-4价电子数为32,不属于等电子体,故b错误;
c.分子间存在氢键的熔沸点高,相同压强时,氨气中含有氢键,PH3中不含氢键,所以NH3沸点比PH3高,故c正确;
d.提供孤电子对的原子是配原子,[Cu(NH3)4]2+离子中,N原子提供孤对电子,N原子为配原子,故d正确;
故答案为:cd;
(3)ClO2-中心氯原子的价层电子对个数n=$\frac{7+1}{2}$=4,属于sp3杂化;等电子体具有相同的电子数目和原子数目的微粒,所以与ClO2-互为等电子体的分子为Cl2O、OF2等;
故答案为:sp3;Cl2O或OF2;
(4)H5IO6(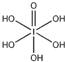 )中含有5个羟基氢,为五元酸,含非羟基氧原子1个,HIO4为一元酸,含有1个羟基氢,含非羟基氧原子3个,所以酸性:H5IO6<HIO4,
)中含有5个羟基氢,为五元酸,含非羟基氧原子1个,HIO4为一元酸,含有1个羟基氢,含非羟基氧原子3个,所以酸性:H5IO6<HIO4,
故答案为:<;
(5)离子晶体中离子电荷越多,半径越小离子键越强,离子晶体的晶格能越大,已知已知CsICl2不稳定,受热易分解,倾向于生成晶格能更大的物质,所以发生的反应为CsICl2=CsCl+ICl,
故答案为:A;
(6)Na+位于顶点,被8个晶胞共有,即Na+与跟它次近邻的Cl-个数为8;Na+与跟它次近邻的Cl-之间的距离为晶胞体对角线的一半,距离为$\sqrt{3}$r,
故答案为:8;$\sqrt{3}$r;
(7)晶胞中共含有4个Na+和4个Cl-,体积为:$\frac{4}{3}$π(a3+b3)×4,晶胞的边长为a+b,晶胞体积为(2a+2b)3,氯化钠晶体中离子的空间利用率为:$\frac{\frac{4}{3}π({a}^{3}+{b}^{3})×4}{(2a+2b)^{3}}$=$\frac{2π}{3}×\frac{({a}^{3}+{b}^{3})}{(a+b)^{3}}×100%$,
故答案为:$\frac{2π}{3}×\frac{({a}^{3}+{b}^{3})}{(a+b)^{3}}×100%$.
点评 本题考查物质结构和性质,涉及核外电子排布、杂化方式的判断等知识点,题目难度中等.明确常见晶胞结构类型、杂化原理的熟练应用为解答关键.

| A. | C3H6 | B. | C2H6O | C. | C6H6 | D. | CH2Cl2 |
| 时间/s | 0 | 20 | 40 | 60 | 80 | 100 |
| n(A)/mol | 0.40 | - | 0.20 | - | - | 0.10 |
| n(B)/mol | 0.00 | 0.24 | - | 0.52 | 0.60 | 0.60 |
| A. | 0~40 s的平均反应速率v(B)=0.01 mol•L-1•s-1 | |
| B. | 80 s时容器中混合气体的密度小于40 s时混合气体的密度 | |
| C. | 其他条件不变,加入合适的催化剂,0~80 s时间段内v(A)>0.001 875 mol•L-1•s-1 | |
| D. | 反应达到最大限度后,增加A的浓度,B的生成速率不变 |
| A. | 硅 | B. | 磷 | C. | 硫 | D. | 氯 |
| A. | 单质钠放入水中:Na+H2O═Na++OH-+H2↑ | |
| B. | 二氧化硅溶于NaOH溶液:SiO2+2OH-═SiO32-+H2O | |
| C. | 向氯化铝溶液中加入过量氨水:Al3++4NH3•H2O═AlO2-+4NH4++2H2O | |
| D. | 碳酸氢铵溶液与足量的NaOH溶液混合后加热:NH4++OH-$\frac{\underline{\;\;△\;\;}}{\;}$NH3↑+H2O |
| A. | 标准状况下,33.6L氟化氢中含有氟原子的数目为1.5NA | |
| B. | 常温常压下,7.0g由乙烯与丙烯组成的混合物中含有氢原子的数目为NA | |
| C. | 1mol Al3+含有的核外电子数为3NA | |
| D. | 某密闭容器装有0.1mol N2和0.3mol H2,在一定条件下充分反应,转移电子的数目为0.6NA |
 .
.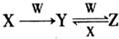 已知A、B、C、D、E是原子序数依次增大的五种短周期元素,A、C同主族,A与B、A与E形成共价化合物,A与B形成化合物的水溶液呈碱性,E元素的最高正化合价与最低负化合价的代数和为6,D是同周期中离子半径最小的元素.
已知A、B、C、D、E是原子序数依次增大的五种短周期元素,A、C同主族,A与B、A与E形成共价化合物,A与B形成化合物的水溶液呈碱性,E元素的最高正化合价与最低负化合价的代数和为6,D是同周期中离子半径最小的元素.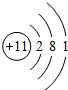 ,用电子式写出C和E形成化合物的过程
,用电子式写出C和E形成化合物的过程 ,用电子式写出A和B形成化合物的过程
,用电子式写出A和B形成化合物的过程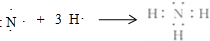 .
.
 .
.