题目内容
8.设NA为阿伏加德罗常数的值,下列叙述正确的是( )| A. | 标准状况下,33.6L氟化氢中含有氟原子的数目为1.5NA | |
| B. | 常温常压下,7.0g由乙烯与丙烯组成的混合物中含有氢原子的数目为NA | |
| C. | 1mol Al3+含有的核外电子数为3NA | |
| D. | 某密闭容器装有0.1mol N2和0.3mol H2,在一定条件下充分反应,转移电子的数目为0.6NA |
分析 A.气体摩尔体积使用对象为气体;
B.乙烯与丙烯的最简式相同为CH2,根据n=$\frac{m}{M}$计算最简式的物质的量,H原子物质的量是最简式的2倍,再根据N=nNA计算;
C.1个铝离子核外有10个电子;
D.氮气与氢气合成氨气为可逆反应,可逆反应不能进行到底;
解答 解:A.标况下,HF为液体,不能使用气体摩尔体积,故A错误;
B.乙烯与丙烯的最简式相同为CH2,最简式的物质的量为$\frac{7g}{14g/mol}$=0.5mol,故H原子物质的量为1mol,含有H原子数目为NA,故B正确;
C.1mol Al3+含有的核外电子数为10NA,故C错误;
D.氮气与氢气合成氨气为可逆反应,可逆反应不能进行到底,所以0.1mol N2和0.3mol H2,在一定条件下充分反应,转移电子的数目小于0.6NA,故D错误;
故选:B.
点评 本题考查阿伏加德罗常数的有关计算和判断,掌握好以物质的量为中心的各化学量与阿伏加德罗常数的关系,明确标况下气体摩尔体积的使用条件是解题关键,注意可逆反应不能进行到底的特点,题目难度不大.

练习册系列答案
相关题目
19.短周期主族元素X、Y、Z、W原子序数依次增大,X最外层电子数是次外层2倍,Y是非金属性最强的元素,Z原子半径在同周期元素中最大,W可与Z形成离子化合物Z2W.下列说法正确的是( )
| A. | 简单离子半径:W>Z>Y | |
| B. | X与W能形成共价化合物 | |
| C. | Y与Z组成的化合物溶于水呈酸性 | |
| D. | 元素X、Y、W的最高化合价均与其族序数相等 |
16.芳樟醇常用于合成香精,香叶醇存在于香茅油、香叶油、香草油、玫瑰油等物质中,有玫瑰花和橙花香气.它们的结构简式如下: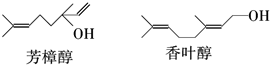
已知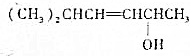 的键线式结构为
的键线式结构为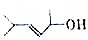 下列说法不正确的是( )
下列说法不正确的是( )

已知
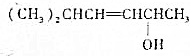 的键线式结构为
的键线式结构为 下列说法不正确的是( )
下列说法不正确的是( )| A. | 两种醇都能与溴水反应 | |
| B. | 两种醇互为同分异构体 | |
| C. | 两种醇与氧气在铜催化的条件下,均可被氧化为相应的醛 | |
| D. | 两种醇在浓H2S04存在下加热,均可与乙酸发生酯化反应 |
3.一定量的盐酸和过量锌粉反应时,为了减缓反应速率,且不影响生成氢气的总量,可以向盐酸中加入适量的( )
| A. | NaOH固体 | B. | 水 | C. | CuSO4固体 | D. | 氯化钠溶液 |
13.下列有关实验原理或操作叙述正确的是( )
| A. | 用干燥洁净的玻璃棒蘸取NaClO溶液,滴到表面皿上的pH试纸上测pH | |
| B. | 不慎将浓碱溶液沾到皮肤上,要立即用大量水冲洗,然后涂上2%~5%的硼酸溶液 | |
| C. | 取金属钠时,要先用镊子夹取,再用小刀切下所需量,剩余钠不能放回原试剂瓶中 | |
| D. | 用NaOH标准溶液滴定盐酸,滴定管尖嘴部分若在滴定前无气泡,滴定终点时出现气泡,测定结果将偏大 |
2.为探究外界条件对H2 (g)+I2 (g)?2HI (g)△H>0 反应速率的影响,设计下表所示实验
(1)完成上表中的空格.
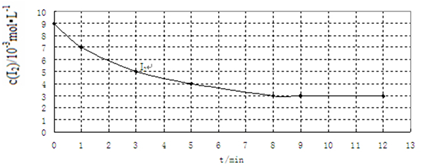
(2)实验Ⅰ中,I2的物质的量浓度(c)随时间(t)的变化如图所示.根据图中数据回答下列问题:
①在0~5min内反应的平均速率ν(I2)=1×10-3mol•L-1•min-1.
②在给出的坐标图中画出实验Ⅱ、Ⅲ中I2的物质的量浓度(c)随时间(t)变化的曲线,并进行必要的标注.
③该同学想用此反应研究压强对化学平衡移动的影响,请问能否达到实验目的?请说明原因.不能(填“能”、不能”),原因是该反应前后气体计量数相等,平衡不受压强的影响.
| 实验 编号 | 实验目的 | 温度/℃ | 催化剂 质量/g | 反应物初始浓度 /10-3mol•L-1 | |
| H2 | I2 | ||||
| Ⅰ | 为以下实验作参照 | 457 | 0 | 7 | 9 |
| Ⅱ | 420 | 7 | 9 | ||
| Ⅲ | 探究催化剂对该反应速率的影响 | 10 | 7 | 9 | |
(2)实验Ⅰ中,I2的物质的量浓度(c)随时间(t)的变化如图所示.根据图中数据回答下列问题:
①在0~5min内反应的平均速率ν(I2)=1×10-3mol•L-1•min-1.
②在给出的坐标图中画出实验Ⅱ、Ⅲ中I2的物质的量浓度(c)随时间(t)变化的曲线,并进行必要的标注.
③该同学想用此反应研究压强对化学平衡移动的影响,请问能否达到实验目的?请说明原因.不能(填“能”、不能”),原因是该反应前后气体计量数相等,平衡不受压强的影响.

19.下列卤代烃在NaOH醇溶液中加热不发生消去反应的是( )
①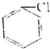 ②
② ③(CH3)3CCH2Cl ④CHCl-CHBr2⑤
③(CH3)3CCH2Cl ④CHCl-CHBr2⑤ ⑥CH3Cl.
⑥CH3Cl.
①
 ②
② ③(CH3)3CCH2Cl ④CHCl-CHBr2⑤
③(CH3)3CCH2Cl ④CHCl-CHBr2⑤ ⑥CH3Cl.
⑥CH3Cl.| A. | ②③⑤ | B. | ①③⑥ | C. | 全部 | D. | ②④ |
 Ⅰ.氢能的存储是氢能应用的主要瓶颈,配位氢化物、富氢载体化合物是目前所采用的主要储氢材料.
Ⅰ.氢能的存储是氢能应用的主要瓶颈,配位氢化物、富氢载体化合物是目前所采用的主要储氢材料.