题目内容
17.硫酸、亚硫酸和氢硫酸是含硫的三种酸.下列说法不正确的是( )| A. | 若向Na2S溶液中通入SO2则产生淡黄色沉淀 | |
| B. | 这三种酸都是二元酸,都能与氢氧化钠反应生成酸式盐和正盐 | |
| C. | 这三种酸的水溶液久置空气中都会变质 | |
| D. | 向氢硫酸、亚硫酸溶液中滴加氯水都会发生氧化还原反应 |
分析 A.Na2S与SO2反应生成硫沉淀;
B.根据酸能电离出的氢离子的数目判断;
C.硫酸在空气中不会变质:
D.-2的S的化合物、+4价的S的化合物均能被氯气氧化.
解答 解:A.Na2S与SO2反应生成硫沉淀,其反应为2Na2S+3SO2=3S↓+2Na2SO3,则向Na2S溶液中通入SO2会产生淡黄色沉淀,故A正确;
B.硫酸、亚硫酸和氢硫酸均能电离出2个氢离子,属于二元酸,都能与氢氧化钠反应生成酸式盐和正盐,故B正确;
C.亚硫酸和氢硫酸均能被空气中的氧气氧化,硫酸与空气中成分不反应,即在空气中不会变质,故C错误;
D.氢硫酸与氯水反应会生成S沉淀,亚硫酸溶液中滴加氯水,亚硫酸会被氧化为硫酸,所以向氢硫酸、亚硫酸溶液中滴加氯水都会发生氧化还原反应,故D正确.
故选C.
点评 本题考查了硫的化合物的性质、氧化还原反应,题目难度不大,注意把握不同化合价的硫的化合物的性质以及氧化还原反应的分析方法.

练习册系列答案
相关题目
8.某温度时,使用一对石墨电极电解饱和Na2SO4溶液,当转移2mol电子时停止电解,析出Na2SO4•10H2O晶体m g,所有数据都在相同温度下测得,下列叙述正确的是( )
| A. | 电解后溶液质量减少(m+36)g | |
| B. | 原溶液中Na2SO4的质量分数为$\frac{71m}{161(m+18)}$ | |
| C. | 若其它条件不变,将石墨电极替换为铜电极,则阴极析出2mol H2 | |
| D. | 若其它条件不变,将石墨电极替换为铜电极,则析出Na2SO4•10H2O晶体仍为m g |
12.为制取含HClO浓度较高的溶液,下列图示装置和原理均正确,且能达到实验目的是( )
| A. | 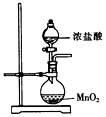 制取氯气 | B. | 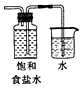 制取氯水 | C. | 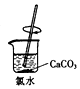 提高HClO浓度 | D. | 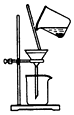 过滤 |
2.下列说法正确的是( )
| A. | 向NaHSO4溶液加入Ba(OH)2溶液至中性:H++SO42-+Ba2++OH-═BaSO4↓+H2O | |
| B. | 100 g含氢元素质量分数为12%的乙烯和乙醛(C2H4O)的混合物中,所含氧原子数目NA | |
| C. | 实验室制氯气的化学方程式:KClO3+6H37Cl(浓)═KCl+337Cl2↑+3H2O | |
| D. | 2.0 L 0.5 mo1/L NaAlO2溶液中含有氧原子的数目为 2NA |
9.下列由相关实验现象所推出的结论正确的是( )
| A. | 纯碱溶液和烧碱溶液均呈碱性,说明二者均属于碱 | |
| B. | Cl2、SO2均能使品红溶液褪色,说明二者均有氧化性 | |
| C. | 某酸与Na2CO3反应生成CO2,说明该酸一定是强酸 | |
| D. | 某溶液中滴加KSCN溶液后,溶液不变色,滴加氯水后溶液显红色,该溶液中一定含Fe2+ |
6.Zn-ZnSO4-PbSO4-Pb电池装置如图,下列说法错误的是( )
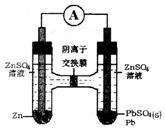

| A. | SO42-从右向左迁移 | |
| B. | 电池的正极反应为:Pb2++2e-═Pb | |
| C. | 左边ZnSO4浓度增大,右边ZnSO4浓度不变 | |
| D. | 若有6.5g锌溶解,有0.1 molSO42-通过离子交换膜 |
7.下列试剂需要保存在棕色试剂瓶中的是( )
| A. | 浓硫酸 | B. | 液溴 | C. | 酒精 | D. | 澄清石灰水 |
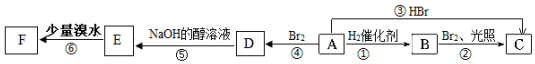
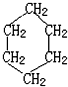 (结构简式).
(结构简式).