题目内容
2.下列说法正确的是( )| A. | 向NaHSO4溶液加入Ba(OH)2溶液至中性:H++SO42-+Ba2++OH-═BaSO4↓+H2O | |
| B. | 100 g含氢元素质量分数为12%的乙烯和乙醛(C2H4O)的混合物中,所含氧原子数目NA | |
| C. | 实验室制氯气的化学方程式:KClO3+6H37Cl(浓)═KCl+337Cl2↑+3H2O | |
| D. | 2.0 L 0.5 mo1/L NaAlO2溶液中含有氧原子的数目为 2NA |
分析 A.反应后溶液呈中性,硫酸氢钠与氢氧化钡按照物质的量2:1反应;
B.混合物C、H原子的物质的量之比为1:2,据此可计算出C的质量分数,然后计算出氧元素的质量分数,结合总质量计算出含有O的物质的量及数目;
C.氯化钾中的Cl原子来自浓盐酸,氯气分子中有1个Cl原子来自氯酸钾;
D.偏铝酸钠溶液中水分子也含有氧原子.
解答 解:A.向NaHSO4溶液加入Ba(OH)2溶液至中性,氢离子与氢氧根离子恰好完全反应,正确的离子方程式为2H++SO42-+Ba2++2OH-═BaSO4↓+2H2O,故A错误;
B.C2H4、C2H4O组成的混合物中,C、H原子数目之比为1:2,则C、H元素质量之比为12:2=6:1,混合物中氢元素质量分数为12%,则混合物中C元素质量分数=12%×6=72%,混合物中氧元素质量分数=1-72%-12%=16%,100g该混合物中含有O的物质的量为$\frac{100g×16%}{16g/mol}$=1mol,所含氧原子数目NA,故B正确;
C.KClO3中Cl元素被还原生成0价氯气,KCl中氯原子来自浓盐酸,正确的化学方程式为2KClO3+12H37Cl(浓)═2K37Cl+Cl2↑+537Cl2↑+6H2O,故C错误;
D.NaAlO2溶液中,溶剂水分子也含有O原子,无法计算混合液中含有氧原子的物质的量及数目,故D错误;
故选B.
点评 本题考查离子方程式、化学方程式的正误判断、物质的量的计算等知识,为高考的高频题,题目难度中等,注意掌握离子方程式、化学方程式的书写原则,C为易错点,明确发生反应的实质为解答关键.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
12.下列物质由于发生反应,既能使溴水褪色,又能使酸性KMnO4溶液褪色的是( )
| A. | 异丁烷 | B. | 1-戊烯 | C. | 苯 | D. | 甲苯 |
13.已知反应A+B=C+D为放热反应,对该反应的下列说法中正确的是( )
| A. | A的能量一定高于C | |
| B. | 该反应为放热反应,故不必加热就一定能发生 | |
| C. | B的能量一定高于D | |
| D. | A和B的总能量一定高于C和D的总能量 |
10.碳是构成地球生命的重要元素.下列说法正确的是( )
| A. | 自然界中不存在游离态的碳 | B. | 碳的化合物数量众多,分布极广 | ||
| C. | 向空气中排放二氧化碳会形成酸雨 | D. | 煤、石油、天然气属于可再生碳资源 |
17.硫酸、亚硫酸和氢硫酸是含硫的三种酸.下列说法不正确的是( )
| A. | 若向Na2S溶液中通入SO2则产生淡黄色沉淀 | |
| B. | 这三种酸都是二元酸,都能与氢氧化钠反应生成酸式盐和正盐 | |
| C. | 这三种酸的水溶液久置空气中都会变质 | |
| D. | 向氢硫酸、亚硫酸溶液中滴加氯水都会发生氧化还原反应 |
7.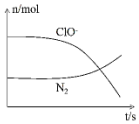 某离子反应涉及到H2O、ClO-、NH4+、OH-、N2、Cl-等微粒,其中N2、ClO-的物质的量随时间变化的曲线如图所示,下列说法正确的是( )
某离子反应涉及到H2O、ClO-、NH4+、OH-、N2、Cl-等微粒,其中N2、ClO-的物质的量随时间变化的曲线如图所示,下列说法正确的是( )
 某离子反应涉及到H2O、ClO-、NH4+、OH-、N2、Cl-等微粒,其中N2、ClO-的物质的量随时间变化的曲线如图所示,下列说法正确的是( )
某离子反应涉及到H2O、ClO-、NH4+、OH-、N2、Cl-等微粒,其中N2、ClO-的物质的量随时间变化的曲线如图所示,下列说法正确的是( )| A. | 该反应中Cl-为氧化产物 | B. | 消耗1 mol还原剂,转移6 mol电子 | ||
| C. | 反应后溶液的酸性减弱 | D. | NH4+被ClO-氧化成N2 |
14.下列离子方程式不正确的是( )
| A. | 乙醛与银氨溶液反应:CH3CHO+2[Ag(NH3)2]OH $\stackrel{△}{→}$CH3COO-+NH4++2Ag↓+3NH3+H2O | |
| B. | 醋酸溶液与新制氢氧化铜反应:2CH3COOH+Cu(OH)2→Cu2++2CH3COO-+2H2O | |
| C. | 苯酚钠溶液中通入少量二氧化碳:2C6H5O-+CO2+H2O→2C6H5OH+CO32- | |
| D. | 溴乙烷水解生成乙醇:CH3CH2Br+OH-$→_{△}^{H_{2}O}$CH3CH2OH+Br- |
11.为实现实验目的,选用的装置、实验操作均正确的是( )
| 实验目的 | 实验步骤和装置 | |
| A | 探究温度对反应速率的影响 | 不同温度下,分别取同体积0.1mol•L-1KI溶液,向其中匀先加入淀粉溶液3滴,再各加入0.1mol•L-1硫酸5滴,并同时记录溶液出现蓝色的时间 |
| B | 配制100mL1.0mol•L-1NaOH溶液 | 向100mL容量瓶中加入4.0gNaOH固体,加水到刻度线 |
| C | 验证牺牲阳极的阴极保护法 | 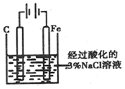 往铁电极附近滴加铁氯化钾溶液 |
| D | 比较H2O2和Fe3+的氧化性 | 将盐酸酸化的双氧水滴入Fe(NO3)2溶液中 |
| A. | A | B. | B | C. | C | D. | D |
12.等量的铁粉分别与足量的盐酸、水蒸气在一定的条件下充分反应,则在相同的条件下,产生氢气的物质的量之比是( )
| A. | 1:1 | B. | 3:4 | C. | 2:3 | D. | 4:3 |