题目内容
8. (1)将0.3mol的气态高能燃料乙硼烷(B2H6)在氧气中燃烧,生成固态三氧化二硼和液态水,放出649.5kJ热量,则乙硼烷的燃烧热的热化学方程式为B2H6(g)+3O2(g)=B2O3(s)+3H2O(l)△H=-2165kJ•mol-1.
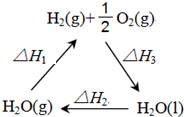
(1)将0.3mol的气态高能燃料乙硼烷(B2H6)在氧气中燃烧,生成固态三氧化二硼和液态水,放出649.5kJ热量,则乙硼烷的燃烧热的热化学方程式为B2H6(g)+3O2(g)=B2O3(s)+3H2O(l)△H=-2165kJ•mol-1.(2)盖斯定律认为:不管化学过程是一步完成或分为数步完成,这个过程的热效应是相同的.某化学过程如图所示,△H1、△H2、△H3三者之间的关系式为△H1+△H2+△H3=0.
分析 (1)0.3molB2H6气体在氧气中燃烧生成固态三氧化二硼和液态水,放出649.5kJ热量,则1molB2H6完全反应放出2165 kJ热量,据此书写热化学反应方程式;
(2)化学反应的反应热只与反应的始态(各反应物)和终态(各生成物)有关,而与反应的途径无关,即如果一个反应可以分步进行,则各分步反应的反应热之和与该反应一步完成时的反应热是相同的,将水蒸气既作为起态和始态,所以各反应热和为零,由此分析解答.
解答 解:(1)0.3molB2H6气体在氧气中燃烧生成固态三氧化二硼和液态水,放出649.5kJ热量,则1molB2H6完全反应放出2165 kJ热量,则该热化学反应方程式为B2H6(g)+3O2(g)=B2O3(s)+3H2O(l)△H=-2165 kJ•mol-1 ,
故答案为:B2H6(g)+3O2(g)=B2O3(s)+3H2O(l)△H=-2165 kJ•mol-1 ;
(2)化学反应的反应热只与反应的始态(各反应物)和终态(各生成物)有关,而与反应的途径无关.即如果一个反应可以分步进行,则各分步反应的反应热之和与该反应一步完成时的反应热是相同的,将水蒸气既作为起态和始态,所以各反应热和为零,故答案为:△H1+△H2+△H3=0.
点评 本题是一个利用盖斯定律解题的一个典型题目,化学反应的反应热只与反应的始态(各反应物)和终态(各生成物)有关,而与反应的途径无关,比较容易.

练习册系列答案
相关题目
19.下列说法中,正确的是( )
| A. | 液氯不导电是非电解质,氯水能导电是强电解质 | |
| B. | 在常温常压下,11.2升氯气所含的原子数目为NA | |
| C. | 氯气可以使湿润的有色布条褪色,但实际起漂白作用的物质是次氯酸而不是氯气 | |
| D. | 1mol氯气参加反应,转移的电子数一定为NA |
16.在由水电离出的c(H+)=1×10-12的溶液中可能大量共存的离子组是( )
| A. | NH4+、K+、CO32-、Cl- | B. | Fe3+、K+、SCN-、NO3- | ||
| C. | Al3+、Cu2+、S2-、Cl- | D. | NH4+、Cu2+、Cl-、NO3- |
3.设NA为阿伏加德罗常数的值,下列说法正确的是( )
| A. | 标准状况下,22.4 L HF中含有原子数为2NA | |
| B. | 7.8 g Na2 0z中阴离子数目为0.2NA | |
| C. | 1 L 1 mol.L-1 KNO3溶液中O原子数为3NA | |
| D. | 常温常压下,44 g CO2和N2O的混合物中含有的质子数为22NA |
13.下列晶体熔化时,化学键没有被破坏的是( )
| A. | 碘化钾 | B. | 氯化钠 | C. | 金刚石 | D. | 干冰 |
20.在催化剂作用下,H2O2发生分解,其反应能量随反应的进程变化如图,下列说法正确的是( )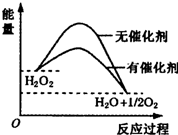

| A. | H2O2分解反应的△H>0 | |
| B. | 催化剂的加入使反应的热效应减小 | |
| C. | 催化剂的加入提高了H2O2的分解率 | |
| D. | 催化剂通过改变反应历程、降低反应的活化能来提高H2O2分解速率 |
17.设NA为阿伏加德罗常数的值.下列说法正确的是( )
| A. | 1 L 0.1mol•L-1的氨水含有0.1NA个OH- | |
| B. | 1 L 1 mol•L-1的NaClO溶液中含有ClO-的数目为NA | |
| C. | 在电解精炼粗铜的过程中,当阴极析出32g铜时转移电子数为NA | |
| D. | 25℃时,pH=13的Ba(OH)2溶液中含有OH-的数目为0.1NA |
18.下列有关氨的说法正确的是( )
| A. | 氨是弱电解质,铵盐是强电解质 | |
| B. | 液氨是纯净物,氨水是混合物 | |
| C. | 氨气遇浓盐酸、浓硫酸、浓硝酸都能产生白烟 | |
| D. | 氨气易液化,所以可用来做喷泉实验 |