题目内容
17.设NA为阿伏加德罗常数的值.下列说法正确的是( )| A. | 1 L 0.1mol•L-1的氨水含有0.1NA个OH- | |
| B. | 1 L 1 mol•L-1的NaClO溶液中含有ClO-的数目为NA | |
| C. | 在电解精炼粗铜的过程中,当阴极析出32g铜时转移电子数为NA | |
| D. | 25℃时,pH=13的Ba(OH)2溶液中含有OH-的数目为0.1NA |
分析 A.一水合氨为弱电解质;
B.次氯酸根离子为弱酸根离子,水溶液中部分水解;
C.32g铜的物质的量为0.5mol,得到0.5mol铜需要转移1mol电子;
D.溶液体积未知.
解答 解:A.一水合氨为弱电解质,部分电离,所以1 L 0.1mol•L-1的氨水含有小于0.1NA个OH-,故A错误;
B.次氯酸根离子为弱酸根离子,水溶液中部分水解,所以1 L 1 mol•L-1的NaClO溶液中含有ClO-的数目小于NA,故B错误;
C.32g铜的物质的量为0.5mol,生成0.5mol铜需要得到1mol电子,根据电子守恒,转移电子数为NA,故C正确;
D.溶液体积未知,无法计算氢氧根离子数目,故D错误;
故选:C.
点评 本题考查阿伏加德罗常数的有关计算和判断,注意掌握好以物质的量为中心的各化学量与阿伏加德罗常数的关系,明确电解法精炼铜原理是解题关键,题目难度中等.

练习册系列答案
 举一反三同步巧讲精练系列答案
举一反三同步巧讲精练系列答案 口算与应用题卡系列答案
口算与应用题卡系列答案
相关题目
7.进行化学实验必须注意安全,下列说法不正确的是( )
| A. | 不慎将少量酸溅到眼中,应立即用水洗,边洗边眨眼睛 | |
| B. | 不慎将浓碱溶液沾到皮肤上,要立即用大量水冲洗,然后涂上硼酸溶液 | |
| C. | 配制稀硫酸时,可先在量筒中加入一定体积的水,再在搅拌下慢慢加入浓硫酸 | |
| D. | 酒精着火时,可用湿抹布将其扑灭 |
12.若NA表示阿伏加德罗的数值,下列说法中正确的是( )
| A. | 1molNa作为还原剂可得到的电子数为NA | |
| B. | 标准状况下,22.4L水中所含的水分子数为NA | |
| C. | 常温常压下,4g氦气含有的氦原子数为NA | |
| D. | 1mol Fe与足量的Cl2充分反应电子转移数为2NA |
2.下列有关实验现象或结论的描述不正确的是( )
| A. | 铅蓄电池充电时,阳极的反应为:PbSO4+2H2O+2e-═PbO2+SO42-+4H+ | |
| B. | FeCl2溶液与K3[Fe(CN)6]溶液混合后得到特征蓝色沉淀,利用此反应可检验Fe2+ | |
| C. | 常温下将5mL 0.1 mol/LNa2S2O3溶液、5mL 0.01 mol/LNa2S2O3溶液分别与5mL 0.1 mol/LH2SO4溶液混合并搅拌,通过记录溶液中出现浑浊的时间,可确定浓度对化学反应速率的影响 | |
| D. | 处理含有Hg2+离子的废水可加入硫化钠,使Hg2+离子转化为HgS沉淀 |
9.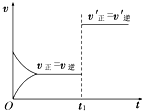 对可逆反应:2A(g)+B(s)?3C(s)+2D(g);△H>0.如图所示为正逆反应速率(v)与时间(t)关系的示意图,如果在t1时刻改变以下条件:
对可逆反应:2A(g)+B(s)?3C(s)+2D(g);△H>0.如图所示为正逆反应速率(v)与时间(t)关系的示意图,如果在t1时刻改变以下条件:
①加入A;
②加入催化剂;
③加压;
④升温;
⑤减少C
符合图示的条件是( )
 对可逆反应:2A(g)+B(s)?3C(s)+2D(g);△H>0.如图所示为正逆反应速率(v)与时间(t)关系的示意图,如果在t1时刻改变以下条件:
对可逆反应:2A(g)+B(s)?3C(s)+2D(g);△H>0.如图所示为正逆反应速率(v)与时间(t)关系的示意图,如果在t1时刻改变以下条件:①加入A;
②加入催化剂;
③加压;
④升温;
⑤减少C
符合图示的条件是( )
| A. | ②③ | B. | ①② | C. | ③④ | D. | ④⑤ |
6.硫酸亚铁铵是一种重要的化工原料,以下各组溶液中加入该盐后,选项中各离子数目均没有明显减少的是( )
| A. | Na+ H+ Cl- NO3- | B. | Na+ Mg2+ Cl- SO42- | ||
| C. | K+ Ba2+ OH- I- | D. | K+ OH- Br- Cl- |
7.下列说法正确的是( )
| A. | 氧化钠可用于呼吸面具中作为氧气的来源 | |
| B. | 氧化还原反应的实质是元素化合价是否变化 | |
| C. | 铁制容器可以贮运稀硝酸 | |
| D. | 雷电为自然界固氮提供了条件 |
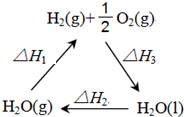 (1)将0.3mol的气态高能燃料乙硼烷(B2H6)在氧气中燃烧,生成固态三氧化二硼和液态水,放出649.5kJ热量,则乙硼烷的燃烧热的热化学方程式为B2H6(g)+3O2(g)=B2O3(s)+3H2O(l)△H=-2165kJ•mol-1.
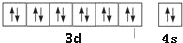
(1)将0.3mol的气态高能燃料乙硼烷(B2H6)在氧气中燃烧,生成固态三氧化二硼和液态水,放出649.5kJ热量,则乙硼烷的燃烧热的热化学方程式为B2H6(g)+3O2(g)=B2O3(s)+3H2O(l)△H=-2165kJ•mol-1.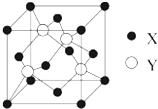 元素X位于第四周期,其基态原子的内层轨道全部排满电子,且最外层电子数为2.元素Y基态原子的3p轨道上有4个电子.元素Z的原子最外层电子数是其内层的3倍.
元素X位于第四周期,其基态原子的内层轨道全部排满电子,且最外层电子数为2.元素Y基态原子的3p轨道上有4个电子.元素Z的原子最外层电子数是其内层的3倍.