题目内容
7.下列化学用语表示正确的是( )| A. | CO2分子的球棍模型: | |
| B. | COCl2的电子式: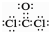 | |
| C. | 质子数为6、质量数为14的原子:${\;}_{6}^{14}$N | |
| D. | 熔融状态下硫酸氢钾的电离方程式:KHSO4(熔融)→K++H++SO4- |
分析 A、根据球棍模型主要体现的是分子的空间结构和成键类型;
B、COCl2中含有碳氧双键,各原子满足最外层8电子;
C、质子数为6是碳原子;
D、熔融状态下硫酸氢钾电离氢原子不电离.
解答 解:A、因CO2分子是直线形分子,不是V形分子,故A错误;
B、COCl2中含有碳氧双键,根据电子式书写方法书写正确,故B正确;
C、元素符号的左下角为6,质子数为6的是碳,而不是氮元素,故C错误;
D、熔融状态下硫酸氢钾的电离方程式:KHSO4$\frac{\underline{\;熔融\;}}{\;}$K++HSO4-,故D错误;
故选B.
点评 本题考查球棍模型、电子式、元素、电离方程式等,难度不大,注意不同化学用语的书写要求.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
17.学生做如下实验:第一步,在淀粉KI溶液中,滴入少量NaClO溶液,并加入少量稀硫酸,溶液立即变蓝;第二步,在上述蓝色溶液中,滴加足量的Na2SO3溶液,蓝色逐渐消失.下列叙述中该同学对实验原理的解释和所得结论不正确的是( )
| A. | 氧化性:ClO->I2>SO42- | |
| B. | 蓝色消失的原因是Na2SO3溶液反应生成SO2具有漂白性 | |
| C. | 淀粉KI溶液变蓝是因为I-被ClO-氧化为I2,I2遇淀粉变蓝 | |
| D. | 若将Na2SO3溶液加入溴水,溴水褪色 |
19.有如下转化关系:
甲+强酸→盐+气体+H2O,则甲不可能是( )
甲+强酸→盐+气体+H2O,则甲不可能是( )
| A. | Na2O2 | B. | Cu | C. | Fe | D. | Si |
13.下列说法中错误的是( )
| A. | 原子及其离子的核外电子层数等于该元素所在的周期数 | |
| B. | 元素周期表中从IIIB族到IIB族 10个纵行的元素都是金属元素 | |
| C. | 除氦外的稀有气体原子的最外层电子数都是8 | |
| D. | 同一元素的各种同位素的物理性质、化学性质均相同 |
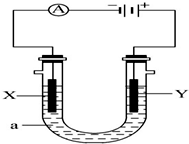 电解原理在化学工业中有广泛应用.如图表示一个电解池,X、Y都是惰性电极,a是饱和NaCl溶液,实验开始时,同时在两边各滴入几滴酚酞溶液,请回答以下问题:
电解原理在化学工业中有广泛应用.如图表示一个电解池,X、Y都是惰性电极,a是饱和NaCl溶液,实验开始时,同时在两边各滴入几滴酚酞溶液,请回答以下问题: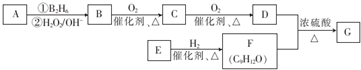
 ;该反应的反应类型为取代反应或酯化反应
;该反应的反应类型为取代反应或酯化反应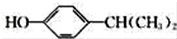 .
.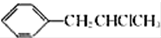 为原料也可合成F,请参考题目中的相关信息写出相应的合成路线图(反应条件中的试剂写在箭头上方,其他写在箭头下方):
为原料也可合成F,请参考题目中的相关信息写出相应的合成路线图(反应条件中的试剂写在箭头上方,其他写在箭头下方):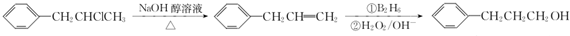 .
.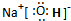 ,所含有的化学键有离子键、极性共价键;它属于离子化合物(填“离子”或“共价”).
,所含有的化学键有离子键、极性共价键;它属于离子化合物(填“离子”或“共价”).