题目内容
固体粉末X中可能含有FeO、Fe2O3、MnO2、K2S、K2SO3、KAlO2、MgCl2、K2SO4、K2CO3、NaNO2中的若干种.为确定该固体粉末的成分,现取X进行连续实验,实验过程及产物如下:
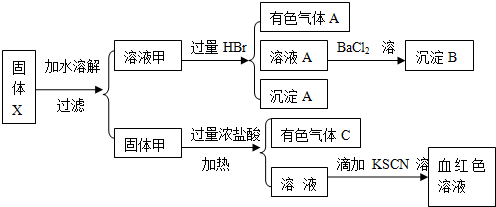
根据上述实验,以下说法正确的是( )

根据上述实验,以下说法正确的是( )
| A、原混合物中一定含有Fe2O3 |
| B、气体A一定均为纯净物 |
| C、气体C是纯净的氯气 |
| D、溶液甲中一定含有K2S、K2SO3、NaNO2、K2SO4可能含有KAlO2、K2CO3 |
考点:物质的检验和鉴别的实验方案设计
专题:实验设计题
分析:有色气体A应为NO2,可能含有CO2气体,说明一定含有NaNO2,固体甲与浓盐酸反应生成有色气体C,C应为Cl2,则应含有MnO2,沉淀A应为S,说明含有K2S、K2SO3,则一定不含有MgCl2,溶液A和氯化钡反应得到沉淀,沉淀为硫酸钡沉淀,则原溶液含K2SO4,溶液加KSCN溶液呈血红色,说明含有Fe3+,则固体中可能含有FeO、Fe2O3,Fe2+可被氯气氧化生成Fe3+,以此解答该题.
解答:
解:有色气体A应为NO2,可能含有CO2气体,说明一定含有NaNO2,固体甲与浓盐酸反应生成有色气体C,C应为Cl2,则应含有MnO2,沉淀A应为S,说明含有K2S、K2SO3,则一定不含有MgCl2,溶液A和氯化钡反应得到沉淀,沉淀为硫酸钡沉淀,则原溶液含K2SO4,溶液加KSCN溶液呈血红色,说明含有Fe3+,则固体中可能含有FeO、Fe2O3,Fe2+可被氯气氧化生成Fe3+,
A.溶液B加KSCN溶液呈血红色,说明含有Fe3+,则固体中可能含有FeO、Fe2O3,Fe2+可被氯气氧化生成Fe3+,故A错误;
B.有色气体A应为NO2,可能含有CO2气体,故B错误;
C.而浓盐酸易挥发,生成的氯气中一定含有HCl气体,故C错误;
D.有以上分析可知溶液甲中一定含有K2S、K2SO3、NaNO2、K2SO4,一定没有MgCl2,可能含有K2CO3,也可能含有KAlO2,加入过量氢溴酸生成AlBr3,与以上物质不反应,不能确定,故D正确;
故选D.
A.溶液B加KSCN溶液呈血红色,说明含有Fe3+,则固体中可能含有FeO、Fe2O3,Fe2+可被氯气氧化生成Fe3+,故A错误;
B.有色气体A应为NO2,可能含有CO2气体,故B错误;
C.而浓盐酸易挥发,生成的氯气中一定含有HCl气体,故C错误;
D.有以上分析可知溶液甲中一定含有K2S、K2SO3、NaNO2、K2SO4,一定没有MgCl2,可能含有K2CO3,也可能含有KAlO2,加入过量氢溴酸生成AlBr3,与以上物质不反应,不能确定,故D正确;
故选D.
点评:本题考查物质的检验和鉴别的实验方案的设计,侧重于元素化合物知识的综合运用,题目难度中等,注意把握反应的现象,根据现象结合物质的性质进行判断,易错点为A,注意体会.

练习册系列答案
相关题目
将40℃的饱和石灰水冷却至10℃;或加入少量CaO,但温度仍保持40℃,在这两种情况下均未改变的是( )
| A、Ca(OH)2的溶解度、溶剂的质量 |
| B、溶液中溶质的质量分数 |
| C、溶液的质量、水的电离平衡 |
| D、溶液中Ca2+的数目 |
下列原理或用途不正确的是( )
| A、酒精消毒是对蛋白的变性作用 |
| B、天然皮革是变性蛋白质 |
| C、误食重金属盐会使人中毒,可以服用鸡蛋清帮助解毒 |
| D、坏血病患者应该多吃的食物是鱼肉和猪肉 |

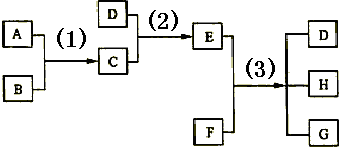
 如图是某化学课外活动小组设计的乙醇与氢卤酸反应的实验装置图.在烧瓶A中放一些新制的无水硫酸铜粉末,并加入约20mL无水乙醇;锥形瓶B中盛放浓盐酸;分液漏斗C和广口瓶D中分别盛浓硫酸;干燥管F中填满碱石灰;烧杯作水浴器.当打开分液漏斗的活塞后,由于浓硫酸流入B中,则D中导管口有气泡产生.此时水浴加热,发生化学反应.过几分钟,无水硫酸铜粉末由无色变为蓝色,生成的气体从F顶端逸出.试回答:
如图是某化学课外活动小组设计的乙醇与氢卤酸反应的实验装置图.在烧瓶A中放一些新制的无水硫酸铜粉末,并加入约20mL无水乙醇;锥形瓶B中盛放浓盐酸;分液漏斗C和广口瓶D中分别盛浓硫酸;干燥管F中填满碱石灰;烧杯作水浴器.当打开分液漏斗的活塞后,由于浓硫酸流入B中,则D中导管口有气泡产生.此时水浴加热,发生化学反应.过几分钟,无水硫酸铜粉末由无色变为蓝色,生成的气体从F顶端逸出.试回答: