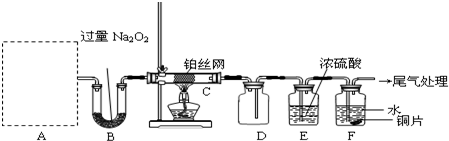
题目内容
已知A、B、C、D均为气体且A的密度小于同条件下B的密度,E、F为固体,G是氯化钙,反应(3)是实验室制取D的方法.它们之间的转换关系如下图所示:
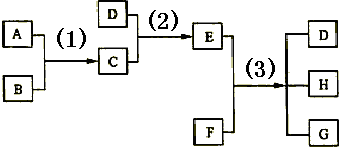
(1)D的化学式 是 ,E的化学式 是 .
(2)A和B反应生成C的化学方程式是 ,A在B中燃烧的现象是 .
(3)E和F反应生成D、H和G的化学方程式是 .

(1)D的化学式 是
(2)A和B反应生成C的化学方程式是
(3)E和F反应生成D、H和G的化学方程式是
考点:无机物的推断
专题:推断题
分析:E、F为固体,G是氯化钙,反应(3)是实验室制取D的方法,通常为氯化铵与氢氧化钙制备氨气的反应,D为NH3,H为H2O,E由气体C、D反应生成,应为NH4Cl,则F为Ca(OH)2,因D为NH3,则C为HCl,A的密度小于同条件下B的密度,则A为H2,B为Cl2,以此解答该题.
解答:
解:E、F为固体,G是氯化钙,反应(3)是实验室制取D的方法,通常为氯化铵与氢氧化钙制备氨气的反应,D为NH3,H为H2O,E由气体C、D反应生成,应为NH4Cl,则F为Ca(OH)2,因D为NH3,则C为HCl,A的密度小于同条件下B的密度,则A为H2,B为Cl2,
(1)由以上分析可知D为NH3,E为NH4Cl,故答案为:NH3;NH4Cl;
(2)A为H2,B为Cl2,二者在点燃条件下反应生成HCl,方程式为H2+Cl2
2HCl,可观察到苍白色火焰,因HCl易溶于水,可观察到瓶口有白雾,
故答案为:H2+Cl2
2HCl; 苍白色火焰,瓶口有白雾;
(3)E和F反应生成D、H和G的反应为实验室用氯化铵和氢氧化钙制备氨气的反应,方程式为2NH4Cl+Ca(OH)2
2NH3↑+2H2O+CaCl2,
故答案为:2NH4Cl+Ca(OH)2
2NH3↑+2H2O+CaCl2.
(1)由以上分析可知D为NH3,E为NH4Cl,故答案为:NH3;NH4Cl;
(2)A为H2,B为Cl2,二者在点燃条件下反应生成HCl,方程式为H2+Cl2
| ||
故答案为:H2+Cl2
| ||
(3)E和F反应生成D、H和G的反应为实验室用氯化铵和氢氧化钙制备氨气的反应,方程式为2NH4Cl+Ca(OH)2
| ||
故答案为:2NH4Cl+Ca(OH)2
| ||
点评:本题考查无机物的推断,为高考常见题型,侧重于学生的分析能力,多角度考查元素化合物知识的理解和运用,注意从反应(3)作为该题的突破口,难度不大.

练习册系列答案
相关题目
两种气态烃的混合气体0.1mol,完全燃烧得0.16mol CO2和3.6g水,下列说法正确的是( )
| A、混合气体中一定有甲烷 |
| B、混合气体中一定是甲烷和乙烯 |
| C、混合气体中一定有乙烷 |
| D、混合气体中一定有乙炔(CH≡CH) |
固体粉末X中可能含有FeO、Fe2O3、MnO2、K2S、K2SO3、KAlO2、MgCl2、K2SO4、K2CO3、NaNO2中的若干种.为确定该固体粉末的成分,现取X进行连续实验,实验过程及产物如下:
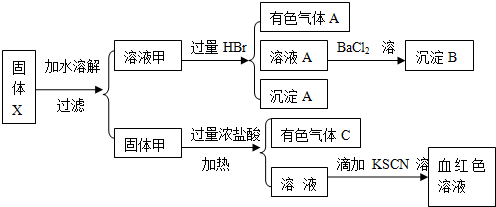
根据上述实验,以下说法正确的是( )

根据上述实验,以下说法正确的是( )
| A、原混合物中一定含有Fe2O3 |
| B、气体A一定均为纯净物 |
| C、气体C是纯净的氯气 |
| D、溶液甲中一定含有K2S、K2SO3、NaNO2、K2SO4可能含有KAlO2、K2CO3 |
只用氢氧化钠溶液不能除去下列各组物质中的杂质(括号中是杂质)的是( )
| A、Mg(Al2O3) |
| B、MgCl2(AlCl3) |
| C、Mg(Al) |
| D、MgO(Al2O3) |
下列对沉淀溶解平衡的描述正确的是( )
| A、反应开始时,溶液中各离子浓度相等 |
| B、达到平衡时,沉淀的速率和溶解的速率相等 |
| C、达到平衡时,溶液中溶质的离子浓度相等,且保持不变 |
| D、达到平衡时,如果再加入难溶性的该沉淀物,将促进溶解 |

 某纯碱样品中含有少量氯化钠杂质,现用如图所示装置来测定纯碱样品中碳酸钠的质量分数(铁架台、铁夹等在图中均已略去).实验步骤如下:
某纯碱样品中含有少量氯化钠杂质,现用如图所示装置来测定纯碱样品中碳酸钠的质量分数(铁架台、铁夹等在图中均已略去).实验步骤如下: