题目内容
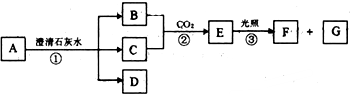
中化学A-G均为中学化学中常见的物质.常温下,A是黄绿色气体,C是无色无味的液体,G是无色无味气体,他们的转化关系如图所示(部分反应中的产物已略去)
(1)写出A的化学式是 ;
(2)①②③三个反应中不属于氧化还原反应的是 ;
(3)写出反应①的离子方程式 .

(1)写出A的化学式是
(2)①②③三个反应中不属于氧化还原反应的是
(3)写出反应①的离子方程式
考点:无机物的推断
专题:推断题
分析:常温下,A是黄绿色气体,能与澄清石灰水反应,则A为氯气,C是无色无味的液体,能与B在二氧化碳的作用下反应生成光照易分解的物质,则D为氯化钙,B、C为水和次氯酸钙,E为次氯酸,G是无色无味气体,G为氧气,F为盐酸,以此解答.
解答:
解:常温下,A是黄绿色气体,能与澄清石灰水反应,则A为氯气,C是无色无味的液体,能与B在二氧化碳的作用下反应生成光照易分解的物质,则D为氯化钙,B、C为水和次氯酸钙,E为次氯酸,G是无色无味气体,G为氧气,F为盐酸,
(1)由以上分析知A为氯气,故答案为:Cl2;
(2)反应①是氯气与氢氧化钙的反应,氯元素化合价变化,属于氧化还原反应,反应②是二氧化碳、次氯酸钙溶液反应,属于置换反应,不属于氧化还原反应,反应③是次氯酸分解,属于氧化还原反应,故答案为:②;
(3)反应①是氯气与氢氧化钙的反应,离子方程式为Cl2+2OH-=Cl-+ClO-+H2O,故答案为:Cl2+2OH-=Cl-+ClO-+H2O.
(1)由以上分析知A为氯气,故答案为:Cl2;
(2)反应①是氯气与氢氧化钙的反应,氯元素化合价变化,属于氧化还原反应,反应②是二氧化碳、次氯酸钙溶液反应,属于置换反应,不属于氧化还原反应,反应③是次氯酸分解,属于氧化还原反应,故答案为:②;
(3)反应①是氯气与氢氧化钙的反应,离子方程式为Cl2+2OH-=Cl-+ClO-+H2O,故答案为:Cl2+2OH-=Cl-+ClO-+H2O.
点评:本题考查了有关氯气的推断问题,注意根据黄绿色气体判断氯气,根据E见光分解判断次氯酸,题目难度不大.

练习册系列答案
 金钥匙试卷系列答案
金钥匙试卷系列答案
相关题目
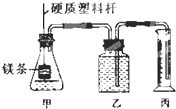 某研究性学习小组为证明在相同条件下,同浓度同体积强弱不同的一元酸与同一种金属反应时,生成氢气的速率不同,同时测定该温度和压强下的气体摩尔体积,设计组装了两套如图所示的简易实验装置.
某研究性学习小组为证明在相同条件下,同浓度同体积强弱不同的一元酸与同一种金属反应时,生成氢气的速率不同,同时测定该温度和压强下的气体摩尔体积,设计组装了两套如图所示的简易实验装置.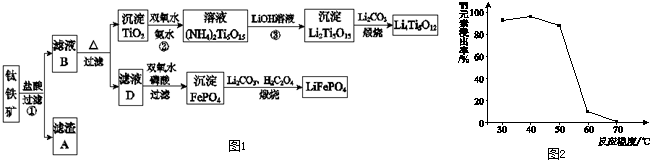
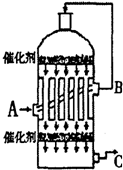 硫酸是工业生产中最为重要的产品之一,在化学工业的很多领域都要用到浓硫酸.
硫酸是工业生产中最为重要的产品之一,在化学工业的很多领域都要用到浓硫酸.