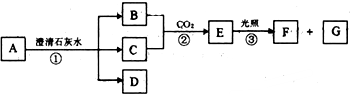
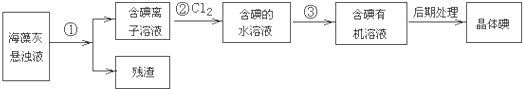
题目内容
在100℃时,将0.100mol的N2O4气体充入1L真空的密闭容器(恒容)中,已知容器中的反应为N2O4(g)?2NO2(g)(正反应为吸热反应).每间隔20s对该容器内的物质进行分析,得到数据如下表,请回答:
试填空:
(1)20s时N2O4的浓度a= ,在0s~20s内N2O4的平均反应速率为 ;表中b c d(填“>”“<”或“=”).
(2)该反应达到平衡时N2O4的转化率为 ,若对该平衡混合气体进行加热,则其平均相对分子质量将 (填“增大”、“减小”或“不变”).
(3)若在相同条件下,往原平衡体系中再通入0.2mol NO2气体,重新达到平衡时容器内的NO2物质的量为 .
A.大于0.12mol,小于0.24mol
B.等于0.24mol
C.大于0.24mol,小于0.32mol
D.等于0.32mol.
| 0 | 20 | 40 | 60 | 80 | |
| c(N2O4)mol?L-1 | 0.100 | a | 0.050 | c | d |
| c(NO2)/mol?L-1 | 0.000 | 0.060 | b | 0.120 | 0.120 |
(1)20s时N2O4的浓度a=
(2)该反应达到平衡时N2O4的转化率为
(3)若在相同条件下,往原平衡体系中再通入0.2mol NO2气体,重新达到平衡时容器内的NO2物质的量为
A.大于0.12mol,小于0.24mol
B.等于0.24mol
C.大于0.24mol,小于0.32mol
D.等于0.32mol.
考点:化学平衡的影响因素
专题:化学平衡专题
分析:(1)根据同一可逆反应、同一时间段内,各物质浓度的变化量之比等于其计量数之比;根据v=
计算反应速率;
根据方程式计算,计算b、c,据此解答,60s后反应达平衡,反应混合物各组分的浓度不变.
(2)由表可知,60s时反应达平衡,根据方程式计算△c(N2O4),根据转化率计算平衡时N2O4的转化率;
N2O4(g)?2NO2(g)(正反应为吸热反应),升高温度,平衡右移,物质的量增大,质量不变,平均相对分子质量减小;
(3)恒容下,再通入0.2mol NO2气体,平衡左移,N2O4的转化率减小.
| △c |
| △t |
根据方程式计算,计算b、c,据此解答,60s后反应达平衡,反应混合物各组分的浓度不变.
(2)由表可知,60s时反应达平衡,根据方程式计算△c(N2O4),根据转化率计算平衡时N2O4的转化率;
N2O4(g)?2NO2(g)(正反应为吸热反应),升高温度,平衡右移,物质的量增大,质量不变,平均相对分子质量减小;
(3)恒容下,再通入0.2mol NO2气体,平衡左移,N2O4的转化率减小.
解答:
解:(1)①根据同一可逆反应、同一时间段内,各物质浓度的变化量之比等于其计量数之比,0-20s时,△c(N2O4):△c(NO2)=(0.100-a):(0.060-0)=1:2,则a=0.070;
v=
=
=0.0015 mol?(L?s)-1;
c3=0.1mol/L-0.06mol/L=0.04mol/L,
由表可知,40s时,c(N2O4)=0.050mol/L,
N2O4?2 NO2,
浓度变化:(0.1-0.05)mol/L 0.10mol/L
所以b=0.10mol/L,所以b>c;
60s后反应达平衡,反应混合物各组分的浓度不变,所以c=d.
故答案为:0.070mol/L;0.0015mol?(L?s)-1;>;=;
(2)由表可知,60s时反应达平衡,c(NO2)=0.120mol/L,
N2O4?2 NO2,
浓度变化:0.06mol/L 0.120mol/L
所以平衡时N2O4的转化率为
×100%=60%,
N2O4(g)?2NO2(g)(正反应为吸热反应),升高温度,平衡右移,物质的量增大,质量不变,平均相对分子质量减小;
故答案为:60%;减小;
(3)恒容下,再通入0.2mol NO2气体,相当于又通入了0.100mol的N2O4气体,平衡左移,N2O4的转化率减小,NO2消耗的物质的量将增大,NO2物质的量为大于原平衡的0.12mol,而小于小于原平衡的2倍,即小于0.24mol.
故答案为:A.
v=
| △c |
| △t |
| (0.100-0.070)mol/L |
| 20S |
c3=0.1mol/L-0.06mol/L=0.04mol/L,
由表可知,40s时,c(N2O4)=0.050mol/L,
N2O4?2 NO2,
浓度变化:(0.1-0.05)mol/L 0.10mol/L
所以b=0.10mol/L,所以b>c;
60s后反应达平衡,反应混合物各组分的浓度不变,所以c=d.
故答案为:0.070mol/L;0.0015mol?(L?s)-1;>;=;
(2)由表可知,60s时反应达平衡,c(NO2)=0.120mol/L,
N2O4?2 NO2,
浓度变化:0.06mol/L 0.120mol/L
所以平衡时N2O4的转化率为
| 0.06mol/L |
| 0.1mol/L |
N2O4(g)?2NO2(g)(正反应为吸热反应),升高温度,平衡右移,物质的量增大,质量不变,平均相对分子质量减小;
故答案为:60%;减小;
(3)恒容下,再通入0.2mol NO2气体,相当于又通入了0.100mol的N2O4气体,平衡左移,N2O4的转化率减小,NO2消耗的物质的量将增大,NO2物质的量为大于原平衡的0.12mol,而小于小于原平衡的2倍,即小于0.24mol.
故答案为:A.
点评:本题考查了等效平衡、化学平衡状态的判断、平衡移动方向的判断等知识点,根据压强对平衡移动的影响判断移动方向,难度中等,注意基础知识的积累掌握.

练习册系列答案
相关题目
下列实验操作正确的是( )
| A、粗盐提纯时,为了加快过滤速率,可用玻璃棒搅拌漏斗中的液体 |
| B、分液操作中,将下层液体放入一烧杯后,再将上层液体继续放入另一烧杯中 |
| C、蒸发KNO3溶液时,当蒸发皿中出现大量晶体时即停止加热,用余热蒸干剩余的水分,获取KNO3晶体 |
| D、蒸馏操作中,温度计水银球部位要插入液面下且不接触蒸馏烧瓶壁 |
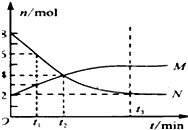 在一定温度下,容器内某一反应中M、N的物质的量随反应时间变化的曲线如图,下列表述中正确的是( )
在一定温度下,容器内某一反应中M、N的物质的量随反应时间变化的曲线如图,下列表述中正确的是( )| A、反应的化学方程式为:N?2M |
| B、t2时,正逆反应速率相等,达到平衡 |
| C、平衡时,N的转化率是75% |
| D、t1分钟内,反应速率:v(M)=2v(N) |
下列四种元素中,第一电离能由大到小顺序正确的是( )
①原子含有未成对电子最多的第二周期元素
②电子排布为1s2的元素
③周期表中电负性最强的元素
④原子最外层电子排布为3s23p4的元素.
①原子含有未成对电子最多的第二周期元素
②电子排布为1s2的元素
③周期表中电负性最强的元素
④原子最外层电子排布为3s23p4的元素.
| A、②③①④ | B、③①④② |
| C、①③④② | D、无法比较 |