题目内容
3.下列关于下图实验装置的说法正确的是( )
| A. | 该装置电流表中没有电流通过 | |
| B. | 铝箔是正极 | |
| C. | 总反应为4Al+3O2+6H2O═4Al(OH)3 | |
| D. | 电子从铝箔流出,经电流表、活性炭、滤纸回到铝箔 |
分析 该装置构成原电池,铝易失电子而作负极,活性炭作正极,负极上失电子发生氧化反应,正极上得电子发生还原反应,电子从负极流向正极.
解答 解:A.该装置符合原电池的构成条件,所以能构成原电池,原电池将化学能转化为电能,有电流通过,故A错误;
B.活性炭上得电子而作正极,故B错误;
C.负极上铝失电子发生氧化反应,正极上氧气得电子发生还原反应,所以发生吸氧腐蚀,电池反应式为:4Al+3O2+6H2O=4Al(OH)3,故C正确;
D.电子从负极铝箔流出,经电流表流向活性炭,故D错误;
故选C.
点评 本题考查原电池原理,明确原电池的构成条件、正负极的判断方法、电子的流向即可解答,注意电子不进入电解质溶液,为易错点.

练习册系列答案
相关题目
14.下列表示对应化学反应离子方程式正确的是( )
| A. | 用KIO3氧化酸性溶液中的KI:5I-+IO3-+3H2O═3I2+6OH- | |
| B. | FeCl3溶液于Cu的反应:Cu+Fe3+═Cu2++Fe2+ | |
| C. | 用氢氧化钠溶液除去铝表面的氧化膜:Al2O3+2OH-═2AlO2-+H2O | |
| D. | 过量氯气通入FeI2溶液中:3Cl2+2I-+4Fe2+═I2+4Fe3++4Cl- |
18.下列物质中,中心原子的杂化方式不是sp3杂化的是( )
| A. | SO2 | B. | CH4 | C. | NH3 | D. | SO42- |
12.下列各组物质中,X是主体物质,Y是其中含有的少量杂质,Z是为除去杂质而加入的试剂,其中能达到除杂目的组别是( )
| X | Y | Z | |
| A | Cl2 | HCl | 饱和的食盐溶液 |
| B | CO2 | HCl | 饱和Na2CO3溶液 |
| C | KCl溶液 | MgCl2 | 适量NaOH溶液 |
| D | FeCl2溶液 | CuCl2 | Fe粉 |
| A. | A | B. | B | C. | C | D. | D |
13.实验室熔化固体烧碱时应选用的坩埚是( )
| A. | 玻璃坩埚 | B. | 石英坩埚 | C. | 铁坩埚 | D. | 瓷坩埚 |
 在已经提取氯化钠、溴、镁等化学物质的富碘卤水中,采用图示的工艺流程生产单质碘:
在已经提取氯化钠、溴、镁等化学物质的富碘卤水中,采用图示的工艺流程生产单质碘:
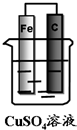 如图装置能否形成原电池?若能,分别写出原电池的电极反应式.
如图装置能否形成原电池?若能,分别写出原电池的电极反应式.  如图,某气体X可能由H2、CO、CH4中的一种或几种组成.将X气体燃烧,把燃烧后生成的气体通过A、B两个洗气瓶.试回答下列问题:
如图,某气体X可能由H2、CO、CH4中的一种或几种组成.将X气体燃烧,把燃烧后生成的气体通过A、B两个洗气瓶.试回答下列问题: