题目内容
14.下列表示对应化学反应离子方程式正确的是( )| A. | 用KIO3氧化酸性溶液中的KI:5I-+IO3-+3H2O═3I2+6OH- | |
| B. | FeCl3溶液于Cu的反应:Cu+Fe3+═Cu2++Fe2+ | |
| C. | 用氢氧化钠溶液除去铝表面的氧化膜:Al2O3+2OH-═2AlO2-+H2O | |
| D. | 过量氯气通入FeI2溶液中:3Cl2+2I-+4Fe2+═I2+4Fe3++4Cl- |
分析 A.酸性条件下,反应产物中不会存在氢氧根离子;
B.离子方程式两边正电荷不相等,违反了电荷守恒;
C.氧化铝与氢氧化钠溶液反应生成偏铝酸钠和水;
D.氯气过量,碘离子和亚铁离子完全反应.
解答 解:A.用KIO3氧化酸性溶液中的KI,正确的离子方程式为:5I-+IO3-+6H+=3I2+3H2O,故A错误;
B.FeCl3溶液于Cu的反应生成氯化亚铁和氯化铜,正确的离子方程式为:Cu+2Fe3+═Cu2++2Fe2+,故B错误;
C.用氢氧化钠溶液除去铝表面的氧化膜,反应的离子方程式为:Al2O3+2OH-═2AlO2-+H2O,故C正确;
D.过量氯气通入FeI2溶液中,亚铁离子和碘离子完全被氧化,正确的离子方程式为:3Cl2+4I-+2Fe2+═2I2+2Fe3++6Cl-,故D错误;
故选C.
点评 本题考查了离子方程式的正误判断,为高考的高频题,属于中等难度的试题,注意掌握离子方程式的书写原则,明确离子方程式正误判断常用方法:检查反应能否发生,检查反应物、生成物是否正确,检查各物质拆分是否正确,如难溶物、弱电解质等需要保留化学式,检查是否符合守恒关系(如:质量守恒和电荷守恒等)、检查是否符合原化学方程式等.

练习册系列答案
相关题目
1.下列操作或装置能达到实验目的是( )
| A. |  检验铁粉与水蒸气反应产生的氢气 | |
| B. |  快速制备和收集一定量的氨气 | |
| C. |  分离互溶但沸点相差较大的液体混合物 | |
| D. | 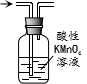 除去甲烷中少量的乙烯得纯净甲烷 |
5.碱性锌锰电池是一种高效的一次电池,外壳为金属锌,中间是石墨极,以MnO2为正极反应物KOH溶液作为电解质溶液,现由碱性锌锰电池回收一些物质.已知Zn2+和Mn2+沉淀的ph范围如下表所示:
请回答下列问题:
(1)该电池的正极反应为MnO2+e-+H+═MnOOH,总反应为Zn+2MnO2+2H+═Zn2++2MnOOH.
(2)该电池中转移0.2mol电子时,消耗MnO2的质量为17.4g.
(3)将该电池的负极材料和MnO2与足量的浓盐酸共热,其中MnO2参与反应的离子方程式为MnO2+4H+(浓)$\frac{\underline{\;\;△\;\;}}{\;}$Mn2++Cl2↑+2H2O;欲使Mn2+和Zn2+分离,需调整pH为6.2≤pH<8.2,可以加入Mn(OH)2调节pH.
(4)再继续调大pH可得到Mn(OH)2,该沉淀在空气中可以迅速被氧化成MnO2,写出此反应的化学方程式2Mn(OH)2+O2=2MnO2+2H2O.
(5)根据Mn2+沉淀完全的pH可以求得Mn(OH)2的Ksp约为10-24.4.
| 离子 | 开始沉淀 | 沉淀完全 |
| Zn2+ | 5.7 | 6.2 |
| Mn2+ | 8.2 | 9.7 |
(1)该电池的正极反应为MnO2+e-+H+═MnOOH,总反应为Zn+2MnO2+2H+═Zn2++2MnOOH.
(2)该电池中转移0.2mol电子时,消耗MnO2的质量为17.4g.
(3)将该电池的负极材料和MnO2与足量的浓盐酸共热,其中MnO2参与反应的离子方程式为MnO2+4H+(浓)$\frac{\underline{\;\;△\;\;}}{\;}$Mn2++Cl2↑+2H2O;欲使Mn2+和Zn2+分离,需调整pH为6.2≤pH<8.2,可以加入Mn(OH)2调节pH.
(4)再继续调大pH可得到Mn(OH)2,该沉淀在空气中可以迅速被氧化成MnO2,写出此反应的化学方程式2Mn(OH)2+O2=2MnO2+2H2O.
(5)根据Mn2+沉淀完全的pH可以求得Mn(OH)2的Ksp约为10-24.4.
2.某有机物的结构简式为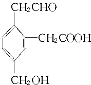 ,该有机化合物属于( )
,该有机化合物属于( )
①芳香烃 ②芳香族化合物 ③醇④羧酸 ⑤酯 ⑥醛 ⑦烃的衍生物⑧不饱和有机物⑨多官能团有机物.
 ,该有机化合物属于( )
,该有机化合物属于( )①芳香烃 ②芳香族化合物 ③醇④羧酸 ⑤酯 ⑥醛 ⑦烃的衍生物⑧不饱和有机物⑨多官能团有机物.
| A. | ②③④ | B. | ①③⑤⑥ | C. | ①③④⑤⑥⑦ | D. | ②③④⑥⑦⑧⑨ |
9.化学能与热能、电能等能相互转化,关于化学能与其他能量相互转化的说法错误的是( )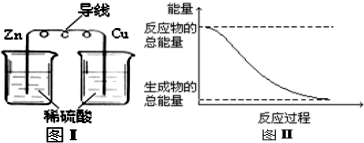

| A. | 化学反应中能量变化的主要原因是化学键的断裂与生成 | |
| B. | 化石燃料是可再生性能源,燃烧时将化学能转变为热能 | |
| C. | 图I所示的装置不能将化学能转变为电能 | |
| D. | 图II所示的反应为放热反应 |
19.已知  ,如果要合成
,如果要合成 所用的原始原料可以是( )
所用的原始原料可以是( )
 ,如果要合成
,如果要合成 所用的原始原料可以是( )
所用的原始原料可以是( )| A. | 2,3-二甲基-1,3-丁二烯和1-丁炔 | B. | 2-甲基-1,3-丁二烯和2-丁炔 | ||
| C. | 2,3-二甲基-1,3-戊二烯和乙炔 | D. | 2-甲基-1,3-丁二烯和丙炔 |
6.油脂的硬化是油脂进行了( )
| A. | 加成反应 | B. | 酯化反应 | C. | 氧化反应 | D. | 皂化反应 |
3.下列关于下图实验装置的说法正确的是( )

| A. | 该装置电流表中没有电流通过 | |
| B. | 铝箔是正极 | |
| C. | 总反应为4Al+3O2+6H2O═4Al(OH)3 | |
| D. | 电子从铝箔流出,经电流表、活性炭、滤纸回到铝箔 |