��Ŀ����
�о������ж�������ŷŶԸ��ƻ�������������ʮ����Ҫ�����壮
��1���ٿ�ѧ�����뽫��������CO2ת��Ϊ�л�������Чʵ��̼ѭ����
a.2CO2+6H2
CH3CH2OH+3H2O
b��CO2+CH4
CH3COOH
c.2CO2+6H2
CH3OCH3+3H2O
d��CO2+3H2
CH3OH+H2O
���Ϸ�Ӧ�в�����������ɫ��ѧ˼�룬��ԭ����������ߵ��� ��
�ڹ�ҵ�ϳ���NH3�ͣ�NH4��2CO3ͨ�����з�Ӧ����CO2���Խ�����������CO2���ŷţ�
a����NH4��2CO3��aq��+H2O��l��+CO2��g��?2NH4HCO3��aq��
b.2NH3��l��+H2O��l��+CO2��g��?��NH4��2CO3��aq��
c��NH3��l��+H2O��l��+CO2��g��?NH4HCO3��ag��
���Ha���Hb����Hc֮��Ĺ�ϵ�ǣ���Ha= ��
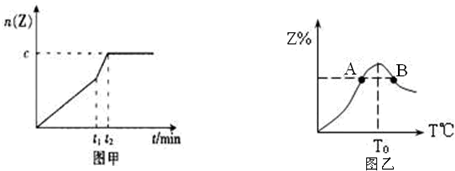
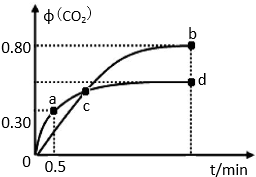
��2������I2O5����CO��Ⱦ�ķ�ӦΪ��5CO��g��+I2O5��s��?5CO2��g��+I2��s����H�� ��ͬ�¶��£���װ������I2O5�����2L�����ܱ�������ͨ��4molCO�����CO2����������գ�CO2����ʱ��t�仯������ͼ��
��ش�
�ٸ÷�Ӧ���� ��Ӧ������ȡ������ȡ�����
�ڴӷ�Ӧ��ʼ��a��ʱ�ķ�Ӧ����Ϊv��CO��= ��b��ʱ��ѧƽ�ⳣ��Kb= ��
������˵������ȷ���� ������ĸ��ţ���
a�������������ܶȲ��䣬������Ӧ�ﵽƽ��״̬
b�������¶��£�c��ʱ��ϵ�л�������ѹǿ���
c������d�����ϵѹǿ��CO��ת���ʲ���
d��b���d��Ļ�ѧƽ�ⳣ����Kb��Kd
��3����ҵ�ϣ���Na2SO3��Һ��Ϊ����Һ���������е�SO2������Һ����SO2�Ĺ����У�����ʱ��Һ�е�c��H+����n��SO32-����n��HSO3-���仯��ϵ���±���
���ϱ��ж�Na2SO3��Һ�� �ԣ�HSO3-�ĵ��볣��Ϊ ��
�ڵ�����Һ������ʱ����Һ������Ũ�ȴ�С��ϵ�� ��
��1���ٿ�ѧ�����뽫��������CO2ת��Ϊ�л�������Чʵ��̼ѭ����
a.2CO2+6H2
| ���� |
| �� |
b��CO2+CH4
| ���� |
| �� |
c.2CO2+6H2
| ���� |
| �� |
d��CO2+3H2
| ���� |
| �� |
���Ϸ�Ӧ�в�����������ɫ��ѧ˼�룬��ԭ����������ߵ���
�ڹ�ҵ�ϳ���NH3�ͣ�NH4��2CO3ͨ�����з�Ӧ����CO2���Խ�����������CO2���ŷţ�
a����NH4��2CO3��aq��+H2O��l��+CO2��g��?2NH4HCO3��aq��
b.2NH3��l��+H2O��l��+CO2��g��?��NH4��2CO3��aq��
c��NH3��l��+H2O��l��+CO2��g��?NH4HCO3��ag��
���Ha���Hb����Hc֮��Ĺ�ϵ�ǣ���Ha=
��2������I2O5����CO��Ⱦ�ķ�ӦΪ��5CO��g��+I2O5��s��?5CO2��g��+I2��s����H�� ��ͬ�¶��£���װ������I2O5�����2L�����ܱ�������ͨ��4molCO�����CO2����������գ�CO2����ʱ��t�仯������ͼ��

��ش�
�ٸ÷�Ӧ����
�ڴӷ�Ӧ��ʼ��a��ʱ�ķ�Ӧ����Ϊv��CO��=
������˵������ȷ����
a�������������ܶȲ��䣬������Ӧ�ﵽƽ��״̬
b�������¶��£�c��ʱ��ϵ�л�������ѹǿ���
c������d�����ϵѹǿ��CO��ת���ʲ���
d��b���d��Ļ�ѧƽ�ⳣ����Kb��Kd
��3����ҵ�ϣ���Na2SO3��Һ��Ϊ����Һ���������е�SO2������Һ����SO2�Ĺ����У�����ʱ��Һ�е�c��H+����n��SO32-����n��HSO3-���仯��ϵ���±���
| n��SO32-����n��HSO3-�� | 91��9 | 1��1 | 9��91 |
| c��H+�� | 6.3��10-9 | 6.3��10-8 | 6.3��10-7 |
�ڵ�����Һ������ʱ����Һ������Ũ�ȴ�С��ϵ��
���㣺ת�������¶ȡ�ѹǿ�ı仯����,�Ȼ�ѧ����ʽ,��ѧƽ�⽨���Ĺ���,��ѧƽ���Ӱ������
ר�⣺
��������1����ԭ����������ߵ��ǻ��Ϸ�Ӧ������ԭ�Ӷ������Ʒ��
�����ø�˹���ɽ��м��㣻
��2������ͼ���֪��d���߷�Ӧ���ʿ죬�¶ȸߣ���CO2���������С���������¶ȣ�ƽ�������ƶ���
�ڸ�����ʼ����a��ʱCO2�����������������������������ʽ���㼴������ӷ�Ӧ��ʼ��a��ʱ�ķ�Ӧ����Ϊv��CO��������b��ʱCO2����������գ�CO2���CO��CO2��ƽ��Ũ�Ƚ������b��ʱ��ѧƽ�ⳣ��Kb��
��a����Ϊ����Ϊ���ݣ�����Ӧǰ�����������仯�����������������ܶ��DZ�����������ʱ������Ӧ�ﵽƽ��״̬��
b��c��Ϊ���㣬���������ʵ����ֱ���ȣ�
c����Ӧǰ������������䣬ѹǿ�仯��ƽ����Ӱ�죻
d��b���d��ʱ������CO2���������˵�����еij̶ȴ���ѧƽ�ⳣ����Kb��Kd��
��3������Na2SO3��Һ����SO2ʱ���������յ����࣬��Һ�ɼ�����Ϊ���ԣ�
HSO3-�ĵ��볣��=
�����˽��м��㣻
������Һ������ʱ������Ϊ�������ƺ����������ƣ�������ˮ��ij̶�������˽����жϣ�
�����ø�˹���ɽ��м��㣻
��2������ͼ���֪��d���߷�Ӧ���ʿ죬�¶ȸߣ���CO2���������С���������¶ȣ�ƽ�������ƶ���
�ڸ�����ʼ����a��ʱCO2�����������������������������ʽ���㼴������ӷ�Ӧ��ʼ��a��ʱ�ķ�Ӧ����Ϊv��CO��������b��ʱCO2����������գ�CO2���CO��CO2��ƽ��Ũ�Ƚ������b��ʱ��ѧƽ�ⳣ��Kb��
��a����Ϊ����Ϊ���ݣ�����Ӧǰ�����������仯�����������������ܶ��DZ�����������ʱ������Ӧ�ﵽƽ��״̬��
b��c��Ϊ���㣬���������ʵ����ֱ���ȣ�
c����Ӧǰ������������䣬ѹǿ�仯��ƽ����Ӱ�죻
d��b���d��ʱ������CO2���������˵�����еij̶ȴ���ѧƽ�ⳣ����Kb��Kd��
��3������Na2SO3��Һ����SO2ʱ���������յ����࣬��Һ�ɼ�����Ϊ���ԣ�
HSO3-�ĵ��볣��=
| c(SO32-)��c(H+) |
| c(HSO3-) |
������Һ������ʱ������Ϊ�������ƺ����������ƣ�������ˮ��ij̶�������˽����жϣ�
���
�⣺��1����b�ǻ��Ϸ�Ӧ������ԭ�Ӷ������Ʒ����ԭ����������ߣ��ʴ�Ϊ��b��
��a����NH4��2CO3��aq��+H2O��l��+CO2��g��?2NH4HCO3��aq��
b.2NH3��l��+H2O��l��+CO2��g��?��NH4��2CO3��aq��
c��NH3��l��+H2O��l��+CO2��g��?NH4HCO3��ag��
c��2-b���NH4��2CO3 ��aq��+H2O ��l��+CO2 ��g��?2NH4HCO3 ��aq����Ha=2��Hc-��Hb��
�ʴ�Ϊ��2��Hc-��Hb��
��2����5CO��g��+I2O5��s��?5CO2��g��+I2��s������ͼ���֪��d���߷�Ӧ���ʿ죬�¶ȸߣ���CO2���������С���������¶ȣ�ƽ�������ƶ����ʸ÷�ӦΪ���ȷ�Ӧ��
�ʴ�Ϊ�����ȣ�
�ڣ���a��ʱ��5CO��g��+I2O5��s��?5CO2��g��+I2��s��
��ʼ��/mol 4 0
ת����/mol x x
a����/mol 4-x x
����a��ʱCO2����������գ�CO2��=
=0.30����x=1.2mol
��ӷ�Ӧ��ʼ��a��ʱ�ķ�Ӧ����Ϊv��CO��=
=1.2mol?L-1?min-1��
b��ʱ��5CO��g��+I2O5��s��?5CO2��g��+I2��s��
��ʼ��/mol 4 0
ת����/mol y y
b����/mol 4-y y
����b��ʱCO2����������գ�CO2��=
=0.80����y=3.2mol��c��CO��=0.4mol?L-1��c��CO2��=1.6mol?L-1
b��ʱ��ѧƽ�ⳣ��Kb=
=
=1024��
�ʴ�Ϊ��1.2mol?L-1?min-1��1024��
��A����Ϊ����Ϊ���ݣ�����Ӧǰ�����������仯�����������������ܶȲ���ʱ��������Ӧ�ﵽƽ��״̬����A��ȷ��
B��c��Ϊ���㣬�������ʵ����ֱ���ȣ����������¶��£���ϵ�л�������ѹǿ���ȣ���b����
C����Ӧǰ������������䣬ѹǿ�仯��ƽ����Ӱ�죬CO��ת���ʲ��䣬��c��ȷ��
d��b���d��ʱ������CO2���������˵�����еij̶ȴ���ѧƽ�ⳣ����Kb��Kd����d����
�ʴ�Ϊ��bd��
��3����c��H+��=6.3��10-9��1��10-7������Һ�Լ��ԣ�
n��SO32-����n��HSO3-��=1��1��c��H+��=6.3��10-8��
��HSO3-�ĵ��볣��=
=6.3��10-8 mol?L-1��
�ʴ�Ϊ���6.3��10-8 mol?L-1��
����Һ�����ԣ�˵��c��H+��=c��OH-����
n��SO32-����n��HSO3-��=1��1ʱ��c��H+��=6.3��10-8������Һ����ʱ��c��HSO3-����c��SO32-����
������Ũ��Ϊc��Na+����c��HSO3-����c��SO32-����c��H+��=c��OH-����
�ʴ�Ϊ��c��Na+����c��HSO3-����c��SO32-����c��H+��=c��OH-����
��a����NH4��2CO3��aq��+H2O��l��+CO2��g��?2NH4HCO3��aq��
b.2NH3��l��+H2O��l��+CO2��g��?��NH4��2CO3��aq��
c��NH3��l��+H2O��l��+CO2��g��?NH4HCO3��ag��
c��2-b���NH4��2CO3 ��aq��+H2O ��l��+CO2 ��g��?2NH4HCO3 ��aq����Ha=2��Hc-��Hb��
�ʴ�Ϊ��2��Hc-��Hb��
��2����5CO��g��+I2O5��s��?5CO2��g��+I2��s������ͼ���֪��d���߷�Ӧ���ʿ죬�¶ȸߣ���CO2���������С���������¶ȣ�ƽ�������ƶ����ʸ÷�ӦΪ���ȷ�Ӧ��
�ʴ�Ϊ�����ȣ�
�ڣ���a��ʱ��5CO��g��+I2O5��s��?5CO2��g��+I2��s��
��ʼ��/mol 4 0
ת����/mol x x
a����/mol 4-x x
����a��ʱCO2����������գ�CO2��=
| x |
| 4 |
��ӷ�Ӧ��ʼ��a��ʱ�ķ�Ӧ����Ϊv��CO��=
| 1.2mol |
| 2L��0.5min |
b��ʱ��5CO��g��+I2O5��s��?5CO2��g��+I2��s��
��ʼ��/mol 4 0
ת����/mol y y
b����/mol 4-y y
����b��ʱCO2����������գ�CO2��=
| y |
| 4 |
b��ʱ��ѧƽ�ⳣ��Kb=
| c(CO2)5 |
| c(CO)5 |
| 1��65 |
| 0��45 |
�ʴ�Ϊ��1.2mol?L-1?min-1��1024��
��A����Ϊ����Ϊ���ݣ�����Ӧǰ�����������仯�����������������ܶȲ���ʱ��������Ӧ�ﵽƽ��״̬����A��ȷ��
B��c��Ϊ���㣬�������ʵ����ֱ���ȣ����������¶��£���ϵ�л�������ѹǿ���ȣ���b����
C����Ӧǰ������������䣬ѹǿ�仯��ƽ����Ӱ�죬CO��ת���ʲ��䣬��c��ȷ��
d��b���d��ʱ������CO2���������˵�����еij̶ȴ���ѧƽ�ⳣ����Kb��Kd����d����
�ʴ�Ϊ��bd��
��3����c��H+��=6.3��10-9��1��10-7������Һ�Լ��ԣ�
n��SO32-����n��HSO3-��=1��1��c��H+��=6.3��10-8��
��HSO3-�ĵ��볣��=
| c(SO32-)��c(H+) |
| c(HSO3-) |
�ʴ�Ϊ���6.3��10-8 mol?L-1��
����Һ�����ԣ�˵��c��H+��=c��OH-����
n��SO32-����n��HSO3-��=1��1ʱ��c��H+��=6.3��10-8������Һ����ʱ��c��HSO3-����c��SO32-����
������Ũ��Ϊc��Na+����c��HSO3-����c��SO32-����c��H+��=c��OH-����
�ʴ�Ϊ��c��Na+����c��HSO3-����c��SO32-����c��H+��=c��OH-����
���������⿼����ɫ��ѧ���ݸ�˹���ɵ�Ӧ�á���ѧ��Ӧ���ʺͻ�ѧƽ�ⳣ������ؼ��㡢��ѧƽ���ƶ�ԭ�������볣��������Ũ�ȴ�С�ıȽϵ�֪ʶ���ۺ��Ժ�ǿ���ѶȺܴ��ݱ������ݷ���������ˮ��Ϊ�����Ĺؼ���

��ϰ��ϵ�д�
�����Ŀ
�������ʵ�ˮ��Һ����NaOH����CH3COOH����NH3����NaHCO3����Cl2�������ܽ�CaCO3���ǣ�������
| A���٢ۢ� | B���٢ܢ� |
| C���ڢ� | D���ڢ� |
�й�AgCl�ij����ܽ�ƽ���˵����ȷ���ǣ�������
| A��AgCl������ˮ����Һ��û��Ag+��Cl- |
| B��AgCl�������ɺ��ܽ�ͬʱ�ڲ��Ͻ��У���������� |
| C����AgCl��Һ�м������ᣬһ�����г������� |
| D������AgCl������Һ�м���NaBr���壬AgCl�������仯 |
��NA��ʾ�����ӵ�������ֵ������������ȷ���ǣ�������
| A��78g Na2O2������CO2��ַ�Ӧʱ����ת����Ϊ2NA |
| B��NA���������ӵ����Ϊ22.4L |
| C��4�桢101kPaʱ��54mL H2O�к��еķ�����Ϊ3NA |
| D��1mol/L Na2SO4��Һ����������Ϊ3NA |
����˵������ȷ���ǣ�������
| A������������ֺͻ�ͭ�����ںϽ� |
| B��ˮ�ࡢ�������մɾ��������ǽ������� |
| C�������ơ�����þ�������������ڼ��������� |
| D����Һ�����塢��Һ�����ڷ�ɢϵ |
 COOH
COOH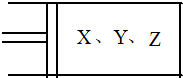 ��ͼ��ʾ����6mol X��3mol Y���������������ɱ�ĵ�ѹ�����У���һ���¶��·������·�Ӧ��2X��g��+Y��g��?2Z��g������Ӧ�ﵽƽ��״̬Aʱ��������������ʵ���Ϊ6.6mol����X��Y��Z����ʼ���ʵ����ֱ���a��b��c��ʾ���ش��������⣺
��ͼ��ʾ����6mol X��3mol Y���������������ɱ�ĵ�ѹ�����У���һ���¶��·������·�Ӧ��2X��g��+Y��g��?2Z��g������Ӧ�ﵽƽ��״̬Aʱ��������������ʵ���Ϊ6.6mol����X��Y��Z����ʼ���ʵ����ֱ���a��b��c��ʾ���ش��������⣺