题目内容
尼泊金酸的结构简式为:HO  COOH
COOH
(1)尼泊金酸的分子式为 .
(2)尼泊金酸不具有的性质是 (填序号).
a.可溶于水
b.通常状况下呈固态
c.发生消去反应
d.遇FeCl 3溶液显紫色
(3)1mol尼泊金酸与下列物质反应时,最多可消耗 (填序号).
a.4mol H 2 b.2mol NaHCO 3c.2mol Br 2 d.2mol Na 2CO 3
(4)将尼泊金酸与足量NaOH溶液混合后反应,生成的有机物结构简式为 .
(5)尼泊金酸有多种同分异构体,写出一种符合以下条件且含有苯环的同分异构体的结构简式:①酯类 ;②醛类 .
 COOH
COOH(1)尼泊金酸的分子式为
(2)尼泊金酸不具有的性质是
a.可溶于水
b.通常状况下呈固态
c.发生消去反应
d.遇FeCl 3溶液显紫色
(3)1mol尼泊金酸与下列物质反应时,最多可消耗
a.4mol H 2 b.2mol NaHCO 3c.2mol Br 2 d.2mol Na 2CO 3
(4)将尼泊金酸与足量NaOH溶液混合后反应,生成的有机物结构简式为
(5)尼泊金酸有多种同分异构体,写出一种符合以下条件且含有苯环的同分异构体的结构简式:①酯类
考点:有机物分子中的官能团及其结构
专题:有机物的化学性质及推断
分析:(1)根据结构简式确定分子式;
(2)尼泊金酸分子中含有酚羟基和羧基,具有酚类和羧酸类物质的性质,酚羟基不能发生消去反应;
(3)尼泊金酸分子中含有酚羟基和羧基,酚羟基和-COOH均可与Na 2CO 3溶液反应,均可生成NaHCO3;
(4)酚羟基和羧基能与氢氧化钠反应;
(5)尼泊金酸含有苯环的同分异构体,注意酯类含有酯基,醛类含有醛基.
(2)尼泊金酸分子中含有酚羟基和羧基,具有酚类和羧酸类物质的性质,酚羟基不能发生消去反应;
(3)尼泊金酸分子中含有酚羟基和羧基,酚羟基和-COOH均可与Na 2CO 3溶液反应,均可生成NaHCO3;
(4)酚羟基和羧基能与氢氧化钠反应;
(5)尼泊金酸含有苯环的同分异构体,注意酯类含有酯基,醛类含有醛基.
解答:
解:(1)根据结构简式可知分子式为:C7H6O3,故答案为:C7H6O3;
(2)尼泊金酸分子中含有酚羟基和羧基,羟基和羧基易溶于水;分子量较大,常温下呈固态;酚羟基遇FeCl 3溶液显紫色;不能发生消去反应,故答案为:c;
(3)a.苯环鞥发生加成反应,1mol尼泊金酸最多与3mol H 2反应;
b.只有羧基能与碳酸氢钠反应,1mol尼泊金酸最多与mol NaHCO 3反应;
c.羟基的邻位能发生取代反应,最多可消耗2mol Br 2;
d.酚羟基和羧基能与碳酸钠反应生成碳酸氢钠,1mol尼泊金酸最多与2mol Na 2CO 3反应,
故答案为:c、d;
(4)酚羟基和羧基能与氢氧化钠反应,生成 ,故答案为:
,故答案为: ;
;
(5)尼泊金酸含有苯环的同分异构体,①酯类符合条件的结构简式为: (邻,间等);②醛类符合条件的结构简式为:
(邻,间等);②醛类符合条件的结构简式为: ,故答案为:
,故答案为: (邻,间等);
(邻,间等); .
.
(2)尼泊金酸分子中含有酚羟基和羧基,羟基和羧基易溶于水;分子量较大,常温下呈固态;酚羟基遇FeCl 3溶液显紫色;不能发生消去反应,故答案为:c;
(3)a.苯环鞥发生加成反应,1mol尼泊金酸最多与3mol H 2反应;
b.只有羧基能与碳酸氢钠反应,1mol尼泊金酸最多与mol NaHCO 3反应;
c.羟基的邻位能发生取代反应,最多可消耗2mol Br 2;
d.酚羟基和羧基能与碳酸钠反应生成碳酸氢钠,1mol尼泊金酸最多与2mol Na 2CO 3反应,
故答案为:c、d;
(4)酚羟基和羧基能与氢氧化钠反应,生成
 ,故答案为:
,故答案为: ;
;(5)尼泊金酸含有苯环的同分异构体,①酯类符合条件的结构简式为:
 (邻,间等);②醛类符合条件的结构简式为:
(邻,间等);②醛类符合条件的结构简式为: ,故答案为:
,故答案为: (邻,间等);
(邻,间等); .
.
点评:本题考查有机物的结构与性质,为高频考点,把握官能团与性质的关系为解答的关键,侧重酚、酯性质的考查,(5)为解答的难点,题目难度不大.

练习册系列答案
相关题目
青铜是我国使用最早的合金.下列关于青铜性质的说法,不正确的是( )
| A、熔点比纯铜低 |
| B、能够导电 |
| C、能够导热 |
| D、硬度比纯铜小 |
下列各组物质中,互为同分异构体的是( )
| A、CH4和C2H6 |
| B、CH2=CH2和CH≡CH |
| C、CH3CH2CH3和CH2=CHCH3 |
| D、CH2=CHCH2CH3和CH3CH=CHCH3 |
将过量CO2气体通入下列溶液中,联系所学知识推测会出现浑浊的是( )
| A、CaCl2溶液 |
| B、饱和Na2CO3溶液 |
| C、澄清石灰水 |
| D、CuSO4溶液 |
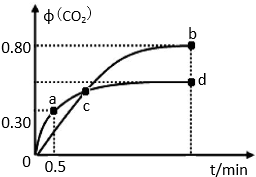
 所示,则下列有关说法正确的是(双选)
所示,则下列有关说法正确的是(双选)
 ,在一定条件下,化合物Ⅲ也能与CO2发生类似于化合物C与CO2反应生成D的反应,生成两种化合物(互为同分异构体),写出其中任意一种化合物的结构简式:
,在一定条件下,化合物Ⅲ也能与CO2发生类似于化合物C与CO2反应生成D的反应,生成两种化合物(互为同分异构体),写出其中任意一种化合物的结构简式: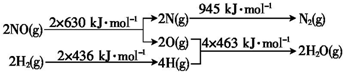 H2还原NO生成氮气和水蒸气的热化学方程式是
H2还原NO生成氮气和水蒸气的热化学方程式是