题目内容
18.实验室用Na2CO3•10H2O晶体配制0.5mol/L的Na2CO3溶液970mL,应选用的玻璃仪器有:烧杯、玻璃棒、量筒、胶头滴管和1000mL容量瓶,称取Na2CO3•10H2O的质量是143.0g.分析 配制0.5mol/L的Na2CO3溶液970mL,选择1000mL容量瓶,结合m=cVM计算,在烧杯中溶解、冷却后转移到容量瓶中定容,以此来解答.
解答 解:配制0.5mol/L的Na2CO3溶液970mL,选择1000mL容量瓶,称取Na2CO3•10H2O的质量是1L×0.5mol/L×286g/mol=143.0g,在烧杯中溶解、冷却后转移到容量瓶中定容,可知需要的仪器为烧杯、玻璃棒、量筒、胶头滴管和1000mL容量瓶,
故答案为:1000mL容量瓶;143.0g.
点评 本题考查配制一定浓度的溶液,为高频考点,把握配制溶液的实验步骤、仪器为解答的关键,侧重分析与实验能力的考查,注意容量瓶的选择,题目难度不大.

练习册系列答案
相关题目
8.尿素是蛋白质代谢的产物,也是重要的化学肥料.工业合成尿素反应如下:
2NH3(g)+CO2(g)═CO(NH2)2(s)+H2O(g)
(1)在一个真空恒容密闭容器中充入CO2和NH3发生上述反应合成尿素,恒定温度下混合气体中的氨气含量如图1所示.A点的正反应速率v正(CO2)>B点的逆反应速率v逆(CO2)(填“>”、“<”或“=”);
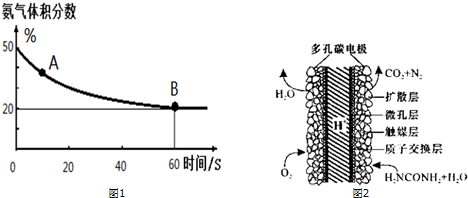
氨气的平衡转化率为75%.
(2)氨基甲酸铵是合成尿素的一种中间产物.将体积比为2:1的NH3和CO2混合气体充入一个容积不变的真空密闭容器中,在恒定温度下使其发生下列反应并达到平衡:
2NH3(g)+CO2(g)═NH2COONH4(s)
将实验测得的不同温度下的平衡数据列于下表:
①关于上述反应的焓变、熵变说法正确的是A.
A.△H<0,△S<0 B.△H>0,△S<0
C.△H>0,△S>0 D.△H<0,△S>0
②关于上述反应的平衡状态下列说法正确的是C
A.分离出少量的氨基甲酸铵,反应物的转化率将增大
B.平衡时降低体系温度,CO2的体积分数下降
C.NH3的转化率始终等于CO2的转化率
D.加入有效的催化剂能够提高氨基甲酸铵的产率
③氨基甲酸铵极易水解成碳酸铵,酸性条件水解更彻底.将氨基甲酸铵粉末逐渐加入1L0.1mol/L的盐酸溶液中直到pH=7(室温下,忽略溶液体积变化),共用去0.052mol氨基甲酸铵,此时溶液中几乎不含碳元素.
此时溶液中c(NH4+)=0.1mol/L;(填具体数值)
NH4+水解平衡常数值为4×10-9.
(3)化学家正在研究尿素动力燃料电池,尿液也能发电!用这种电池直接去除城市废水中的尿素,既能产生净化的水又能发电.尿素燃料电池结构如图2所示,写出该电池的负极反应式:CO(NH2)2+H2O-6e-═N2↑+CO2↑+6H+.
2NH3(g)+CO2(g)═CO(NH2)2(s)+H2O(g)
(1)在一个真空恒容密闭容器中充入CO2和NH3发生上述反应合成尿素,恒定温度下混合气体中的氨气含量如图1所示.A点的正反应速率v正(CO2)>B点的逆反应速率v逆(CO2)(填“>”、“<”或“=”);

氨气的平衡转化率为75%.
(2)氨基甲酸铵是合成尿素的一种中间产物.将体积比为2:1的NH3和CO2混合气体充入一个容积不变的真空密闭容器中,在恒定温度下使其发生下列反应并达到平衡:
2NH3(g)+CO2(g)═NH2COONH4(s)
将实验测得的不同温度下的平衡数据列于下表:
| 温度(℃) | 15.0 | 20.0 | 25.0 | 30.0 | 35.0 |
| 平衡气体总浓度 (10-3mol/L) | 2.4 | 3.4 | 4.8 | 6.8 | 9.4 |
A.△H<0,△S<0 B.△H>0,△S<0
C.△H>0,△S>0 D.△H<0,△S>0
②关于上述反应的平衡状态下列说法正确的是C
A.分离出少量的氨基甲酸铵,反应物的转化率将增大
B.平衡时降低体系温度,CO2的体积分数下降
C.NH3的转化率始终等于CO2的转化率
D.加入有效的催化剂能够提高氨基甲酸铵的产率
③氨基甲酸铵极易水解成碳酸铵,酸性条件水解更彻底.将氨基甲酸铵粉末逐渐加入1L0.1mol/L的盐酸溶液中直到pH=7(室温下,忽略溶液体积变化),共用去0.052mol氨基甲酸铵,此时溶液中几乎不含碳元素.
此时溶液中c(NH4+)=0.1mol/L;(填具体数值)
NH4+水解平衡常数值为4×10-9.
(3)化学家正在研究尿素动力燃料电池,尿液也能发电!用这种电池直接去除城市废水中的尿素,既能产生净化的水又能发电.尿素燃料电池结构如图2所示,写出该电池的负极反应式:CO(NH2)2+H2O-6e-═N2↑+CO2↑+6H+.
9.下列各项表述中正确的是( )
| A. | 氢氧燃料电池就是将氢气在氧气中燃烧,从而获得电流 | |
| B. | 46g的乙醇和28g的乙烯完全燃烧时消耗的O2均为为67.2L(标准状况) | |
| C. | 在氮原子中,质子数为7而中子数一定也为7 | |
| D. | Cl-的结构示意图为 |
13.下列反应的离子方程式中,书写正确的是( )
| A. | 硝酸银溶液跟铜反应 Cu+Ag+═Cu2++Ag | |
| B. | 铁粉跟稀盐酸反应 2Fe+6H+═2Fe3++3H2↑ | |
| C. | 硫酸和氢氧化钡反应:H++SO42-+Ba2++OH-═H2O+BaSO4 | |
| D. | 用小苏打治疗胃酸过多:HCO3-+H+═CO2↑+H2O |
3.形成合金的叙述错误的是( )
| A. | 形成合金后,其熔点要提高 | B. | 合金是混合物 | ||
| C. | 合金具有固定的熔点 | D. | 铁与非金属氯,氧等很难形成合金 |
8.在强酸性、无色透明的溶液中,能够大量存在的离子组是( )
| A. | K+、Mg2+、SO42-、Cl- | B. | Na+、K+、CO32-、Br- | ||
| C. | Ag+、Al3+、SO42-、NO3- | D. | Cu2+、Ca2+、Cl-、NO3- |
