题目内容
 A、B、C、D、E、F、G七种前四周期元素且原子序数依次增大,A的最高正价和最低负价的绝对值相等,B的基态原子有3个不同的能级且各能级中电子数相等,D的基态原子与B的基态原子的未成对电子数目相同,E的基态原子s能级的电子总数与p能级的电子数相等,F的基态原子的3d轨道电子数是4s电子数的4倍,G2+的3d轨道有9个电子,请回答下列问题:
A、B、C、D、E、F、G七种前四周期元素且原子序数依次增大,A的最高正价和最低负价的绝对值相等,B的基态原子有3个不同的能级且各能级中电子数相等,D的基态原子与B的基态原子的未成对电子数目相同,E的基态原子s能级的电子总数与p能级的电子数相等,F的基态原子的3d轨道电子数是4s电子数的4倍,G2+的3d轨道有9个电子,请回答下列问题:(1)F的基态原子电子排布式为
(2)B、C、D的原子的第一电离能由小到大的顺序为
(3)下列关于B2A2分子和A2D2分子的说法正确的是
a.分子中都含有σ键和π键
b.B2A2分子的沸点明显低于A2D2分子
c.都是含极性键和非极性键的非极性分子
d.互为等电子体,分子的空间构型都为直线形
e.中心原子都是sp杂化
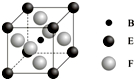
(4)由B、E、F三种元素形成的一种具有超导性的晶体,晶胞如图所示.B位于E和F原子紧密堆积所形成的空隙当中.与一个F原子距离最近的F原子的数目为
(5)向GSO4(aq)中逐滴加入过量氨水,会发生先产生蓝色沉淀后沉淀消失,写出沉淀消失的离子反应方程式:
(6)某电池放电时的总反应为:Fe+F2O3+3H2O=Fe(OH)2+2F(OH)2(注:F2O3和F(OH)2为上面F元素对应的化合物),写出该电池放电时正极反应式
考点:位置结构性质的相互关系应用
专题:
分析:A、B、C、D、E、F、G七种元素的原子序数依次增大.其中B的基态原子有3个不同的能级,且各能级中的电子数相等,原子核外电子排布式为1s22s22p2,故B为碳元素;A的最高正价和最低负价的绝对值相等,原子序数小于碳,故A为H元素;E的基态原子的s能级的电子总数与p能级的电子数相等,原子核外电子排布式为1s22s22p4或1s22s22p63s2,D的基态原子与B的基态原子的未成对电子数目相同,D的原子序数小于E,原子核外电子排布只能为1s22s22p4,则D为O元素,故E为Mg,而C的原子序数介于碳、氧之间,则C为N元素;F的基态原子的3d轨道电子数是4s电子数的4倍,4s电子只能有2个电子层,故原子核外电子排布为1s22s22p63s23p63d84s2,故F为Ni,G2+离子的3d轨道中有9个电子,G原子核外电子数=2+8+8+9+2=29,则G为Cu元素据此解答.
解答:
解:依据分析可知:A为氢、B为碳、C为氮、D为氧、E为镁、F为镍、G为铜,
(1)F为镍,Ni的基态原子的核外电子排布为1s22s22p63s23p63d84s2,
故答案为:[Ar]3d84s2;
(2)C、N、O三种元素,C、N、O同周期,随原子序数增大的第一电离能呈增大趋势,但N元素2p能级容纳3个电子,处于半满稳定状态,能量较低,第一电离能高于同周期相邻元素,故第一电离能由小到大的顺序为C<O<N,故答案为:C<O<N;
(3)a.C2H2分子中含有C≡C三键、C-H键,含有σ键和π键,而H2O2分子为H-O-O-H,只含有σ键,故a错误;
b.C2H2常温下为气态,而H2O2常温下为液态,故b正确;
c.C2H2是直线型对称结构,是非极性分子,而H2O2分子是展开书页形结构,属于极性分子,故c错误;
d.C2H2分子、H2O2分子含有电子总数或价电子总数不相等,不是等电子体,故d错误;
e.C2H2分子中C原子成2个σ键、没有孤对电子,杂化轨道数目为2,采取sp杂化,H2O2分子中O原子成2个σ键、含有2对孤电子对,杂化轨道数目为4,采取sp3杂化,故e错误,
故答案为:b;
(4)以上底面面心F原子研究,与之距离最近的F原子位于晶胞两个侧面及前后面面心上,而晶胞上底面为上层晶胞的下底面,故与之最近的F原子有8个;
由晶胞晶胞可知,晶胞中C原子数目=1、Ni元素数目=6×
=3、Mg原子数目=8×
=1,故该晶体的化学式为MgNi3C;故答案为:8;MgNi3C;
(5)氨水和硫酸铜反应生成氢氧化铜蓝色沉淀,当氨水过量时,氨水和氢氧化铜反应生成可溶性的铜氨络合物,所以难溶物溶解得到深蓝色的透明溶液,涉及的离子方程式为:Cu2++2NH3?H2O=Cu(OH)2↓+2NH4+、Cu(OH)2+4NH3=[Cu(NH3)4]2++2OH-;形成4个配位键,具有对称的空间构型,可能为平面四边形或正四面体,如为正四面体,[Cu(NH3)4]2+中的两个NH3被两个Cl-取代,只有一种结构,所以应为平面四边形,故答案为:Cu(OH)2+4NH3=[Cu(NH3)4]2++2OH-;
(6)电池放电时,正极上得电子发生还原反应,电极反应式为Ni2O3+3H2O+2e-=2Ni(OH)2+2OH-,故答案为:Ni2O3+3H2O+2e-=2Ni(OH)2+2OH-.
(1)F为镍,Ni的基态原子的核外电子排布为1s22s22p63s23p63d84s2,
故答案为:[Ar]3d84s2;
(2)C、N、O三种元素,C、N、O同周期,随原子序数增大的第一电离能呈增大趋势,但N元素2p能级容纳3个电子,处于半满稳定状态,能量较低,第一电离能高于同周期相邻元素,故第一电离能由小到大的顺序为C<O<N,故答案为:C<O<N;
(3)a.C2H2分子中含有C≡C三键、C-H键,含有σ键和π键,而H2O2分子为H-O-O-H,只含有σ键,故a错误;
b.C2H2常温下为气态,而H2O2常温下为液态,故b正确;
c.C2H2是直线型对称结构,是非极性分子,而H2O2分子是展开书页形结构,属于极性分子,故c错误;
d.C2H2分子、H2O2分子含有电子总数或价电子总数不相等,不是等电子体,故d错误;
e.C2H2分子中C原子成2个σ键、没有孤对电子,杂化轨道数目为2,采取sp杂化,H2O2分子中O原子成2个σ键、含有2对孤电子对,杂化轨道数目为4,采取sp3杂化,故e错误,
故答案为:b;
(4)以上底面面心F原子研究,与之距离最近的F原子位于晶胞两个侧面及前后面面心上,而晶胞上底面为上层晶胞的下底面,故与之最近的F原子有8个;
由晶胞晶胞可知,晶胞中C原子数目=1、Ni元素数目=6×
| 1 |
| 2 |
| 1 |
| 8 |
(5)氨水和硫酸铜反应生成氢氧化铜蓝色沉淀,当氨水过量时,氨水和氢氧化铜反应生成可溶性的铜氨络合物,所以难溶物溶解得到深蓝色的透明溶液,涉及的离子方程式为:Cu2++2NH3?H2O=Cu(OH)2↓+2NH4+、Cu(OH)2+4NH3=[Cu(NH3)4]2++2OH-;形成4个配位键,具有对称的空间构型,可能为平面四边形或正四面体,如为正四面体,[Cu(NH3)4]2+中的两个NH3被两个Cl-取代,只有一种结构,所以应为平面四边形,故答案为:Cu(OH)2+4NH3=[Cu(NH3)4]2++2OH-;
(6)电池放电时,正极上得电子发生还原反应,电极反应式为Ni2O3+3H2O+2e-=2Ni(OH)2+2OH-,故答案为:Ni2O3+3H2O+2e-=2Ni(OH)2+2OH-.
点评:本题考查物质结构与性质,涉及核外电子排布、电离能、分子结构与性质、配合物、晶胞结构与计算等,学生要熟练掌握基础知识,并能迁移运用,(4)中晶胞结构与计算,为易错点,需要学生具有一定的空间想象与数学计算能力,难度中等.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
下列溶液中,微粒的物质的量浓度关系正确的是( )
| A、某盐Na2 CO3溶液中:c(OH-)+2c(CO32-)+c(H CO3-)=c(H+)+c(Na+) |
| B、常温时,将PH=1的醋酸和PH=13的Na OH溶液等体积混合后的溶液c(CH3COO-)>c(Na+)>c(H+)>c(OH-) |
| C、NaHCO3溶液中:c(Na+)=2c(CO32-)+c(HCO3-)+c(H2CO3) |
| D、0.1 mol?L-1(NH4)2Fe(SO4)2溶液中:c(NH4+)+c(NH3?H2O)=0.2 mol |
设NA代表阿伏加德罗常数的值.下列说法错误的是( )
| A、30g甲醛(CH2O)与30g葡萄糖均含有NA个碳原子 |
| B、0.1molCl2与过量稀NaOH 溶液作用转移电子数0.2NA |
| C、常温下,1L pH=1的硫酸由水电离出的H+ 约为1×10-13NA |
| D、石墨电极电解CuSO4 溶液,阴极上有4mol电子转移,阳极上有NA个O2 |
下列计算结果正确是( )
| A、向含有1mol AlCl3的溶液中加入足量NaOH溶液就会产生1molAl(OH)3的白色沉淀 | ||
| B、将64g 铜片投入到100ml 18 mol/L的浓硫酸中会产生22.4L的SO2气体 | ||
| C、向1mol的碳酸钾固体中缓缓滴加0.2mol的稀盐酸会产生2.24L的CO2气体 | ||
D、标准状况下,用一充满HCl气体的干燥烧瓶做喷泉实验,当水充满整个烧瓶后(假设溶液不外溢),烧瓶内盐酸的物质的量的浓度为
|
下列有关实验的叙述正确的是( )
| A、检验溶液中SO42-的方法是:先加入BaCl2溶液,再加盐酸 |
| B、从溴水中提纯单质溴的方法是:先用CCl4萃取,分液后再蒸馏 |
| C、证明气体分子中含有“C=C”的方法是:将该气体通入KMnO4酸性溶液 |
| D、除去CO2中少量HCl的方法是:将混合气体通过盛有饱和NaHSO3溶液的洗气瓶 |
下列说法正确的是( )
| A、原子核外电子排布式为1s2的原子与原子核外电子排布式为1s22s2的原子化学性质相似 |
| B、Fe3+的最外层电子排布式为3s23p63d5 |
C、基态铜原子的最外层的电子排布图: |
| D、所有非金属元素都分布在p区 |
自来水常用Cl2消毒,某学生用这种自来水去配制下列物质的溶液,不会产生明显的药品变质问题的是( )
| A、AgNO3 |
| B、FeSO4 |
| C、MgCl2 |
| D、(NH4)2SO3 |
已知2H2(g)+O2(g)→2H2O(g)+483.6kJ.下列说法或表达正确的是( )
| A、在相同的条件下,2mol 氢气与 1 mol 氧气的总能量小于2mol 水蒸气的总能量 | ||
B、H2(g)+
| ||
| C、氢气燃烧是放热反应,所以氢气和氧气反应不需要其他外界条件即可发生 | ||
| D、任何条件下,2L水蒸气分解成2L氢气与1L氧气需吸收483.6kJ热量 |