题目内容
设NA代表阿伏加德罗常数的值.下列说法错误的是( )
| A、30g甲醛(CH2O)与30g葡萄糖均含有NA个碳原子 |
| B、0.1molCl2与过量稀NaOH 溶液作用转移电子数0.2NA |
| C、常温下,1L pH=1的硫酸由水电离出的H+ 约为1×10-13NA |
| D、石墨电极电解CuSO4 溶液,阴极上有4mol电子转移,阳极上有NA个O2 |
考点:阿伏加德罗常数
专题:阿伏加德罗常数和阿伏加德罗定律
分析:A、30g甲醛(CH2O)和葡萄糖(C6H12O6)的混合物中最简式相同,只需计算30gCH2O中含碳原子个数;
B、氯气与碱的反应是歧化反应;
C、在酸溶液中,氢离子绝大部分来自于酸的电离,而氢氧根全部来自于水的电离;
D、根据在电解池中,阴阳极得失电子数相等来计算.
B、氯气与碱的反应是歧化反应;
C、在酸溶液中,氢离子绝大部分来自于酸的电离,而氢氧根全部来自于水的电离;
D、根据在电解池中,阴阳极得失电子数相等来计算.
解答:
解:A、30g甲醛(CH2O)和葡萄糖(C6H12O6)的混合物中最简式相同,只需计算30gCH2O中含碳原子个数=
×NA=NAmol,故A正确;
B、氯气与碱的反应是歧化反应,1mol氯气转移1mol电子,故0.1mol氯气转移0.1mol电子,故B错误;
C、在酸溶液中,氢离子绝大部分来自于酸的电离,而氢氧根全部来自于水的电离,故pH=1的硫酸中c(H+)=0.1mol/L,几乎全部来自于酸;而c(OH-)=10-13mol/L,全部来自于水,而水电离出的c(H+)=c(OH-)=10-13mol/L,故水电离出的H+的物质的量n=CV=10-13mol/L×1L=10-13mol,个数为10-13NA个,故C正确;
D、在电解池中,阴阳极得失电子数相等,当阴极上有4mol电子转移,阳极上会失去4mol电子,根据阳极反应:4OH--4e-=2H2O+O2↑可知,当阳极上失去4mol电子时,生成1mol氧气,故D正确.
故选B.
| 30g |
| 30g/mol |
B、氯气与碱的反应是歧化反应,1mol氯气转移1mol电子,故0.1mol氯气转移0.1mol电子,故B错误;
C、在酸溶液中,氢离子绝大部分来自于酸的电离,而氢氧根全部来自于水的电离,故pH=1的硫酸中c(H+)=0.1mol/L,几乎全部来自于酸;而c(OH-)=10-13mol/L,全部来自于水,而水电离出的c(H+)=c(OH-)=10-13mol/L,故水电离出的H+的物质的量n=CV=10-13mol/L×1L=10-13mol,个数为10-13NA个,故C正确;
D、在电解池中,阴阳极得失电子数相等,当阴极上有4mol电子转移,阳极上会失去4mol电子,根据阳极反应:4OH--4e-=2H2O+O2↑可知,当阳极上失去4mol电子时,生成1mol氧气,故D正确.
故选B.
点评:本题考查了阿伏伽德罗常数的有关计算,掌握公式的使用和物质的结构、状态是解题关键,难度不大.

练习册系列答案
相关题目
某有机物X的分子式为C3H6O2,它在酸性条件下能水解,水解产物只有两种,且这两种产物的相对分子质量相等,该有机物X的结构简式是( )
| A、CH3CH2COOH |
| B、CH3COOCH3 |
| C、HCOOCH2CH3 |
| D、HOCH2CH2CHO |
已知重铬酸钾(K2Cr2O7)是一种强氧化性的物质.在重铬酸钾和KOH的混合液中,重铬酸钾和铬酸钾(K2CrO4)之间存在如下转化关系:K2Cr2O7+2KOH═2K2CrO4+H2O,当反应达到平衡后,加入少量下列固体(或气体)物质,该平衡几乎不发生移动的是( )
| A、NaI固体 |
| B、K2SO4固体 |
| C、NaOH固体 |
| D、HCl气体 |
高铁酸钾(K2FeO4)是一种兼具净水和消毒功能的可溶性盐,可发生如下反应:2K2FeO4+16HCl═4KCl+2FeCl3+8H2O+3Q↑,下列说法正确的是( )
| A、可用湿润的淀粉碘化钾试纸检验产物Q |
| B、K2FeO4在水中的电离方程式为K2FeO4═2K++Fe6++4O2一 |
| C、反应中氧化剂与还原剂的物质的量之比为1:8 |
| D、反应中涉及的6种物质均为电解质 |
NA表示阿伏加德罗常数,下列说法正确的是( )
| A、常温常压下,3.2gO2所含的原子数为0.2NA |
| B、常温下11.2L甲烷气体所含的分子数为0.5NA |
| C、18gD2O所含的电子数为10NA |
| D、1.5molNO2与足量水反应,转移的电子数为1.5NA |
下列离子方程式书写正确的是( )
| A、醋酸溶液与碳酸氢钠溶液反应:H++HCO3-=H2O+CO2↑ |
| B、铜与稀硝酸反应:Cu+4H++2NO3-=Cu2++NO2↑+2H2O |
| C、氯气与烧碱溶液反应:Cl2+2OH-=Cl-+ClO-+H2O |
| D、硫酸溶液与氢氧化钡溶液反应:H++SO42-+OH-+Ba2+=H2O+BaSO4↓ |
下列说法正确的是( )
| A、CuSO4溶液能产生丁达尔效应 |
| B、分散质粒子的直径:浊液>胶体>溶液 |
| C、可以用过滤的方法除去氢氧化铁胶体中的可溶性杂质 |
| D、在饱和氯化铁溶液中滴加氢氧化钠溶液可制得Fe(OH)3胶体 |
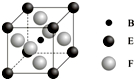 A、B、C、D、E、F、G七种前四周期元素且原子序数依次增大,A的最高正价和最低负价的绝对值相等,B的基态原子有3个不同的能级且各能级中电子数相等,D的基态原子与B的基态原子的未成对电子数目相同,E的基态原子s能级的电子总数与p能级的电子数相等,F的基态原子的3d轨道电子数是4s电子数的4倍,G2+的3d轨道有9个电子,请回答下列问题:
A、B、C、D、E、F、G七种前四周期元素且原子序数依次增大,A的最高正价和最低负价的绝对值相等,B的基态原子有3个不同的能级且各能级中电子数相等,D的基态原子与B的基态原子的未成对电子数目相同,E的基态原子s能级的电子总数与p能级的电子数相等,F的基态原子的3d轨道电子数是4s电子数的4倍,G2+的3d轨道有9个电子,请回答下列问题: