题目内容
按要求填空
(1)分析下列物质的物理性质,判断其晶体类型:
A.碳化铝,黄色晶体,熔点2200℃,熔融态不导电: ;
B.五氟化钒,无色晶体,熔点19.5℃,易溶于乙醇、四氯化碳溶液等有机溶剂中: ;
(2)A.造成温室效应的常见气体的电子式: ;
B.空气中含量最多的气体的结构式: ;
C.淀粉的化学式: ;
(3)从下列六种有机物中选择合适的答案,将其标号填在空格内(填相应字母)
A.蛋白质 B.乙醇 C.乙酸 D.油脂 E.葡萄糖
①食醋可作为增加食品酸味的调味剂,是因为其中含有 ;
②属于天然有机高分子化合物的是 ;
③常用做燃料和医药上消毒剂的是 ;
④花生油、茶籽油、牛油的主要成分是 .
(1)分析下列物质的物理性质,判断其晶体类型:
A.碳化铝,黄色晶体,熔点2200℃,熔融态不导电:
B.五氟化钒,无色晶体,熔点19.5℃,易溶于乙醇、四氯化碳溶液等有机溶剂中:
(2)A.造成温室效应的常见气体的电子式:
B.空气中含量最多的气体的结构式:
C.淀粉的化学式:
(3)从下列六种有机物中选择合适的答案,将其标号填在空格内(填相应字母)
A.蛋白质 B.乙醇 C.乙酸 D.油脂 E.葡萄糖
①食醋可作为增加食品酸味的调味剂,是因为其中含有
②属于天然有机高分子化合物的是
③常用做燃料和医药上消毒剂的是
④花生油、茶籽油、牛油的主要成分是
考点:晶体的类型与物质熔点、硬度、导电性等的关系,生活中的有机化合物
专题:化学键与晶体结构,化学应用
分析:(1)原子晶体的熔点很高,熔融时不导电;分子晶体的熔点较低,易溶于有机溶剂,据此判断;
(2)A.造成温室效应的常见气体的是二氧化碳;
B.空气中含量最多的气体是氮气;
C.淀粉属于高分子是一种多糖;
(3)根据物质的结构、性质和用途分析解答.
(2)A.造成温室效应的常见气体的是二氧化碳;
B.空气中含量最多的气体是氮气;
C.淀粉属于高分子是一种多糖;
(3)根据物质的结构、性质和用途分析解答.
解答:
解:(1)A.原子晶体的熔点很高,熔融时不导电,已知碳化铝,黄色晶体,熔点2200℃,熔融态不导电,则碳化铝为原子晶体;
B.分子晶体的熔点较低,易溶于有机溶剂,已知五氟化钒,无色晶体,熔点19.5℃,易溶于乙醇、四氯化碳溶液等有机溶剂,说明五氟化钒是分子晶体;
故答案为:原子晶体;分子晶体;
(2)A.造成温室效应的常见气体的是二氧化碳,其结构为O=C=O,所以其电子式为 ;
;
B.空气中含量最多的气体是氮气,分子中含有1个三键,其结构式为N≡N;
C.淀粉属于高分子是一种多糖,其化学式为(C6H10O5)n;
故答案为: ;N≡N;(C6H10O5)n;
;N≡N;(C6H10O5)n;
(3)①食醋的主要成分是醋酸,醋酸是一种有机酸可作为增加食品酸味的调味剂;
②蛋白质是一种多肽属于天然有机高分子化合物;
③乙醇燃烧时放出大量热,能使蛋白质变性,能杀死细菌和病毒,常用做燃料和医药上消毒剂;
④花生油、茶籽油、牛油的主要成分是油脂;
故答案为:①C;②A;③B;④D.
B.分子晶体的熔点较低,易溶于有机溶剂,已知五氟化钒,无色晶体,熔点19.5℃,易溶于乙醇、四氯化碳溶液等有机溶剂,说明五氟化钒是分子晶体;
故答案为:原子晶体;分子晶体;
(2)A.造成温室效应的常见气体的是二氧化碳,其结构为O=C=O,所以其电子式为
 ;
;B.空气中含量最多的气体是氮气,分子中含有1个三键,其结构式为N≡N;
C.淀粉属于高分子是一种多糖,其化学式为(C6H10O5)n;
故答案为:
 ;N≡N;(C6H10O5)n;
;N≡N;(C6H10O5)n;(3)①食醋的主要成分是醋酸,醋酸是一种有机酸可作为增加食品酸味的调味剂;
②蛋白质是一种多肽属于天然有机高分子化合物;
③乙醇燃烧时放出大量热,能使蛋白质变性,能杀死细菌和病毒,常用做燃料和医药上消毒剂;
④花生油、茶籽油、牛油的主要成分是油脂;
故答案为:①C;②A;③B;④D.
点评:本题考查了晶体类型的判断,物质电子式、结构式及分子式的书写,常见物质的用途等属于基础知识的考查,题目难度不大.

练习册系列答案
 小学课堂作业系列答案
小学课堂作业系列答案 金博士一点全通系列答案
金博士一点全通系列答案
相关题目
下列有关表述正确的是( )
| A、-OH与OH-组成元素相同,含有的质子数也相同 |
B、NH4Cl的电子式为: |
C、丙烷分子的比例模型示意图: |
D、CO2分子的比例模型示意图: |
下列溶液中有关物质的量浓度关系正确的是( )
| A、Na2CO3溶液中:2c(Na+)=c(CO32-)+c(HCO3-)+c(H2CO3) |
| B、相同条件下,pH=5的 ①NH4Cl溶液、②CH3COOH溶液、③稀盐酸溶液中由水电离出的c(H+):①>②>③ |
| C、NaHCO3溶液中:c(H+)+c(H2CO3)=c(OH-)+c(CO32-) |
| D、0.1mol?L-1的NaHA溶液,其pH=4:c(HA-)>c(H+)>c(H2A)>c(A2-) |
下列过程或现象与盐类水解无关的是( )
| A、硫化钠浓溶液有臭味 |
| B、加热氯化铁溶液颜色变深 |
| C、铁在潮湿的环境下生锈 |
| D、纯碱溶液去油污 |
下列有关实验原理、装置、操作或结论的描述中,不正确的是( )
A、 测量一定时间内生成H2的反应速率 |
B、 用CO2做喷泉实验 |
C、 除去Cl2中的少量HCl |
D、 比较Na2CO3与NaHCO3的热稳定性 |
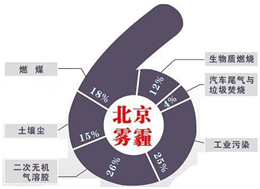 中科院大气研究所研究员张仁健课题组与同行合作,对北京地区PM2.5化学组成及来源的季节变化研究发现,北京PM2.5有6个重要来源,其中,汽车尾气和燃煤分别占4%、18%.
中科院大气研究所研究员张仁健课题组与同行合作,对北京地区PM2.5化学组成及来源的季节变化研究发现,北京PM2.5有6个重要来源,其中,汽车尾气和燃煤分别占4%、18%.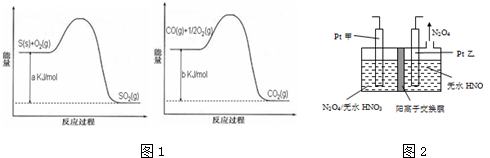
 依据叙述,写出下列反应的热化学方程式.
依据叙述,写出下列反应的热化学方程式.


