题目内容
12.研究表明,在一定温度和压强条件下,2mol H2(g)和1mol O2(g)完全化合成2mol H2O(g)所放出的热量:①与在相同条件下2mol H2O(g)完全分解为2mol H2(g)和1mol O2(g)所吸收的热量在数值上相等;②是相同条件下1mol H2(g)和0.5mol O2(g)完全化合成1mol H2O(g)所放出热量的2倍;③比在相同条件下2mol H2(g)和1mol O2(g)完全化合成2mol H2O(g)所放出的热量少.由此,你可得出哪些结论?分析 由①可知互为逆反应时,焓变的数值相同、符号相反;
由②③可知物质的量与热量成正比,以此来解答.
解答 解:由数据可知,互为逆反应时,焓变的数值相同、符合相反,且物质的量与热量成正比,
答:化学反应中物质的量与热量成正比,互为逆反应时,焓变的数值相同、符合相反.
点评 本题考查反应热与焓变,为高频考点,把握反应中能量变化为解答的关键,侧重分析与应用能力的考查,注意焓变的关系,题目难度不大.

练习册系列答案
相关题目
15.诺氟沙星别名氟哌酸,是治疗肠炎痢疾的常用药.其结构简式如图,下列说法正确的是( )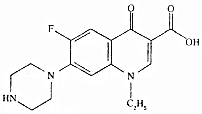

| A. | 该化合物属于苯的同系物 | |
| B. | 分子式为Cl6 H16FN3O3 | |
| C. | 1mol该化合物中含有6NA个双键 | |
| D. | 该化合物能与酸性高锰酸钾、溴水、碳酸氢钠溶液反应 |
3.下列离子方程式书写完全正确的是( )
| A. | 用氯化铁溶液腐蚀铜板:Fe3++Cu=Fe2++Cu2+ | |
| B. | NaHSO4溶液与Ba(OH)2溶液混合至溶液显中性:Ba2++OH-+H++SO42-=BaSO4↓+H2O | |
| C. | 在碳酸氢镁溶液中加入过量氢氧化钠溶液:Mg2++2HCO3-+4OH-=Mg(OH)2↓+2H2O+2CO32- | |
| D. | 向稀醋酸中加入石灰石:CaCO3+2H+=Ca2++CO2↑+H2O |
20.关于下列四个图象的说法中正确的是( )

| A. | 图①表示可逆反应“CO(g)+2H2(g)?CH3OH(g)”的△H<0 | |
| B. | 利用图②所示装置,可以实现在铁制品上镀铜 | |
| C. | 图③表示在实验室中用酸性KMnO4溶液滴定Na2SO3溶液 | |
| D. | 图④表示pH=a的NH3•H2O、NaOH稀释过程,其中线I表示NaOH |
7.在某温度下,将2molA和3molB充入一密闭容器中,发生反应:aA(g)+B(g)?C(g)+D(g),5min后达到平衡,测得K=1.若在温度不变的情况下将容器的体积扩大为原来的1倍,测得A的转化率不发生变化,下列说法正确的是( )
| A. | 改变条件前后,B的转化率均为40% | |
| B. | 改变条件前后,C的反应速率保持不变 | |
| C. | 若保持温度和体积不变,在容器中再充入1molA和1molB,B的转化率不变 | |
| D. | 若保持温度和体积不变,在容器中再充入0.5molB、1molC和1molD,B的转化率增大 |
17.在下列生产生活过程中,涉及氧化还原反应的是( )
| A. | 从海带中提碘 | B. | 用明矾净水 | ||
| C. | 从海水中提取氯化镁 | D. | 用氦气填充飞艇 |
4.检验用硫酸亚铁制得的硫酸铁中是否含有硫酸亚铁,可选用的试剂是( )
| A. | NaOH | B. | KMnO4 | C. | KSCN | D. | 氯水 |
4.短周期主族元素X、Y、Z、W的原子序数依次增大,X元素形成的一种单质是自然界中硬度最大的物质,Y位于周期表中VA族,Z是短周期中金属性最强的元素,W3-与氩原子核外电子排布相同.下列说法正确的是( )
| A. | 原子半径:r(Z)>r(W)>r(Y)>r(X) | |
| B. | Y的简单气态氢化物的热稳定性比W的强 | |
| C. | Z3W中既含有离子键又含有共价键 | |
| D. | X的单质不能与Y的最高价氧化物对应的水化物反应 |

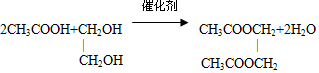 .
.