题目内容
4.检验用硫酸亚铁制得的硫酸铁中是否含有硫酸亚铁,可选用的试剂是( )| A. | NaOH | B. | KMnO4 | C. | KSCN | D. | 氯水 |
分析 亚铁离子具有还原性,可与氯水、高锰酸钾等氧化剂反应,以此解答该题.
解答 解:A.加入氢氧化钠,因含有铁离子,可生成红褐色沉淀,不能检验是否含有亚铁离子,故A错误;
B.亚铁离子具有还原性,可与高锰酸钾等发生氧化还原反应,高锰酸钾溶液褪色,可鉴别,故B正确;
C.亚铁离子与KSCN不反应,不能鉴别,只能鉴别铁离子,故C错误;
D.加入氯水,氯水也铁离子溶液颜色相近,发生反应没有明显的颜色变化,不能鉴别,故D错误.
故选B.
点评 本题考查物质的检验,为高频考点,题目难度不大,本题注意亚铁离子与铁离子性质的区别,检验时必须有明显不同的现象.

练习册系列答案
相关题目
7.下列反应的离子方程式正确的是( )
| A. | 铜跟稀HNO3反应:3Cu+8H++2NO3-═3Cu2++2NO↑+4H2O | |
| B. | 向硫酸铝溶液中加入过量氨水:Al3++3OH-═AlO2-+2H2O | |
| C. | 向Ag(NH3)2NO3溶液中加入盐酸:Ag(NH3)2+2H+═Ag++2NH4+ | |
| D. | NaHSO4溶液和Ba(OH)2溶液混合后溶液呈中性:Ba2++OH-+H++SO42-═BaSO4↓+H2O |
15.下列与化学反应能量变化相关的叙述正确的是( )
| A. | 生成物总能量一定低于反应物总能量 | |
| B. | 放热反应的反应速率总是大于吸热反应的反应速率 | |
| C. | 键能越大,物质越稳定,断键所需的能量就越大 | |
| D. | 同温同压下,H2(g)+Cl2(g)═2HCl(g)在光照和点燃条件下的所放出的热量不同 |
19.在给定的条件下,下列选项所示的物质间转化均能实现的是( )
| A. | NaCL(aq)$\stackrel{CO_{2}}{→}$NaHCO3(s)$\stackrel{△}{→}$NaCO3(s) | |
| B. | FeSz$→_{燃烧}^{O_{2}}$SO2$\stackrel{H_{2}O}{→}$H2SO4 | |
| C. | SiO2$\stackrel{HCl(aq)}{→}$SiCl4$→_{高温}^{H_{2}}$Si | |
| D. | N2$→_{高温、高压、催化剂}^{H_{2}}$NH3$\stackrel{HCl(aq)}{→}$NH4Cl(aq) |
9.下列关于乙二醇和丙三醇的说法中,错误的是( )
| A. | 丙三醇、乙二醇的水溶液的凝固点很低,乙二醇可作内燃机的抗冻剂,丙三醇用于配制化妆品 | |
| B. | 丙三醇的沸点比乙二醇的沸点高 | |
| C. | 这两种多元醇均易溶于乙醇,难溶于水 | |
| D. | 乙二醇和丙三醇都能与Na发生反应 |
16.下列说法中,正确的是( )
| A. | 化合物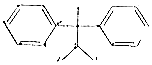 是苯的同系物 是苯的同系物 | |
| B. | 有机物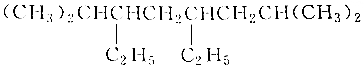 的系统名称是2-甲基-4-乙基-6-异丙基辛烷 的系统名称是2-甲基-4-乙基-6-异丙基辛烷 | |
| C. | C4H8的同分异构体只有3种 | |
| D. | 液化石油气的主要成分是烃,它是一种清洁燃料 |
16.下列指定反应的离子方程式正确的是( )
| A. | 向 H2O中通人 NO2:3NO2+H2O═H++NO3-+2NO | |
| B. | 向Na2SiO3溶液中通入少量SO2:Na2SiO3+SO2+H2O═H2SiO3↓+2Na++SO32- | |
| C. | 用饱和纯減溶液洗涤试管中残留的苯酚:CO32-+2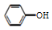 →2 →2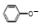 +CO2↑+H2O +CO2↑+H2O | |
| D. | 等体积等物质的量浓度的NH4Fe(SO4)2和Ba(OH)2混合:2Fe3++3SO42-+3Ba2++6OH-═3BaSO4↓+2Fe(OH)3↓ |