题目内容
2mol NH3是 g,含 个分子,含 个原子,在标准状况下所占体积为 L,所含氢原子数和 mol水所含的氢原子数相等.
考点:物质的量的相关计算
专题:计算题
分析:根据m=nM、N=nNA、V=nVm结合分子构成进行计算,氨气和水中氢原子个数相等,则氨气和水的物质的量之比为2:3,据此分析解答.
解答:
解:2mol氨气的质量=2mol×17g/mol=34g,氨气分子个数=2mol×NA/mol=2NA,一个氨气分子中含有4个原子,所以原子个数为8 NA,氨气体积=2mol×22.4L/mol=44.8L,一个氨气分子中含有3个H原子、一个水分子中含有2个H原子,所以氨气和水中氢原子个数相等,则氨气和水的物质的量之比为2:3,氨气的物质的量是2mol,则水的物质的量是3mol,
故答案为:34;2NA;8 NA;44.8;3.
故答案为:34;2NA;8 NA;44.8;3.
点评:本题考查了物质的量的有关计算,熟悉物质的量的基本公式并灵活运用是解本题关键,题目难度不大,注意基础知识的积累.

练习册系列答案
相关题目
在电解水制取H2和O2时,为了增强导电性,常常要加入一些电解质,最好选用( )
| A、NaCl |
| B、HC1 |
| C、NaOH |
| D、CuSO4 |
 Ⅰ同学们已经学习了同位素、同系物、同素异形体、同分异构体,你能区分这些概念吗?下面列出了几组物质,请用物质的组号填写下表.
Ⅰ同学们已经学习了同位素、同系物、同素异形体、同分异构体,你能区分这些概念吗?下面列出了几组物质,请用物质的组号填写下表.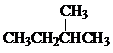 和
和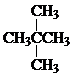
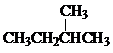 和
和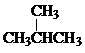
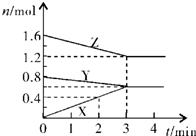
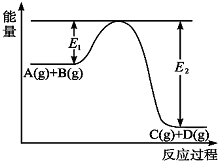 反应A(g)+B(g)?C(g)+D(g)过程中的能量变化如图所示,回答下列问题.
反应A(g)+B(g)?C(g)+D(g)过程中的能量变化如图所示,回答下列问题. 根据反应:mA(g)+nB(g)?pC(g)△H,结合图中所给的信息填空.
根据反应:mA(g)+nB(g)?pC(g)△H,结合图中所给的信息填空.