题目内容
19.硅及其化合物在材料领域中应用广泛.下列叙述不正确的是( )| A. | 晶体硅是良好的半导体材料 | |
| B. | 硅单质可用来制造太阳能电池 | |
| C. | SiO2是制造光导纤维的材料 | |
| D. | 可用带玻璃塞的试剂瓶中盛有NaOH溶液 |
分析 A.晶体硅可作半导体材料;
B.太阳能电池的原料是硅单质;
C.光导纤维的主要成分是二氧化硅;
D.二氧化硅是酸性氧化物.
解答 解:A.晶体硅是良好的半导体材料,故A正确;
B.太阳能电池的原料是硅单质,故B正确;
C.氧化硅是生产光导纤维的主要原料,故C错误;
D.二氧化硅是酸性氧化物,与氢氧化钠反应生成粘合剂硅酸钠,不可用带玻璃塞的试剂瓶中盛有NaOH溶液,故D错误;
故选:D.
点评 本题考查硅和二氧化硅的性质,题目难度不大,注意基础知识的积累.

练习册系列答案
相关题目
7.某消毒液的主要成分为NaClO,还含有一定量的NaOH,下列用来解释事实的方程式中不合理的是(已知:饱和NaClO溶液的pH约为11)( )
| A. | 该消毒液可用NaOH溶液吸收Cl2制备:Cl2+2OH-→ClO-+Cl-+H2O | |
| B. | 该消毒液的pH约为12:ClO-+H2O?HClO+OH- | |
| C. | 该消毒液与洁厕灵(主要成分为HCl)混用,产生有毒Cl2:2H++Cl-+ClO-→Cl2↑+H2O | |
| D. | 该消毒液加白醋生成HClO,可增强漂白作用:H++ClO-→HClO |
14.分类是学习和研究化学物质的一种常用的科学方法,下列说法正确的是( )
| A. | 高锰酸钾中含有氧元素,属于氧化物 | |
| B. | 一氧化碳中含有碳元素,属于有机物 | |
| C. | 纯碱溶液显碱性,属于碱 | |
| D. | 绿矾的化学式为FeSO4•7H2O,属于纯净物 |
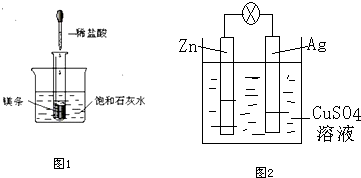
4.下列关于能量转化的认识不正确的是( )
| A. | 原电池工作时,化学能转化为电能 | |
| B. | 手机电池在充电时,是电能转变为化学能 | |
| C. | 煤燃烧时,化学能主要转化为热能 | |
| D. | 人体运动所消耗的能量与化学反应无关 |
11.下列有关乙烯气体和乙醇蒸气的说法正确的是( )
| A. | 二者等物质的量完全燃烧消耗等量的氧气 | |
| B. | 二者分子所有原子都处于同一个平面上 | |
| C. | 二者能相互转化且反应属于可逆反应 | |
| D. | 二者可用酸性高锰酸钾溶液鉴别 |
9.在温度T1和T2时,分别将0.50 mol CH4和1.20 mol NO2充入体积为1L的密闭容器中,发生如下反应:CH4(g)+2NO2(g)?N2(g)+CO2(g)+2H2O(g),测得n(CH4)随时间变化数据如下表:
下列说法正确的是( )
| 时间/min | 0 | 10 | 20 | 40 | 50 | |
| T1 | n(CH4)/mol | 0.50 | 0.35 | 0.25 | 0.10 | 0.10 |
| T2 | n(CH4)/mol | 0.50 | 0.30 | 0.18 | … | 0.15 |
| A. | T2时,NO2的平衡转化率为70.0% | |
| B. | 该反应的△H>0、T1<T2 | |
| C. | 保持其他条件不变,T1时向平衡体系中再充入0.30molCH4和0.80molH2O(g),平衡向正反应方向移动 | |
| D. | 保持其他条件不变,T1时向平衡体系中再充入0.50molCH4和1.20molNO2,与原平衡相比,达新平衡时N2的浓度增大、体积分数减小 |
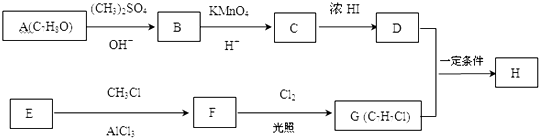
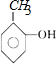 ,由C生成D的化学方程式为
,由C生成D的化学方程式为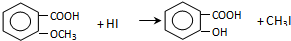 .
.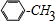 +Cl2$\stackrel{光照}{→}$
+Cl2$\stackrel{光照}{→}$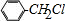 +HCl.反应类型为取代反应
+HCl.反应类型为取代反应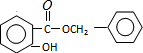 .
. (或
(或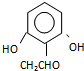 ).
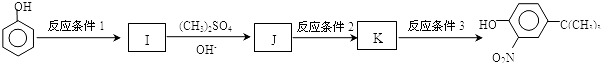
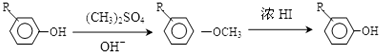
).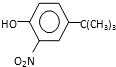 ,反应条件1所用的试剂为(CH3)3CCl/AlCl3,K的结构简式为
,反应条件1所用的试剂为(CH3)3CCl/AlCl3,K的结构简式为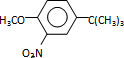 ,反应条件3所用的试剂为浓HI.
,反应条件3所用的试剂为浓HI.