题目内容
11. A图是物质M和N的溶解度曲线.B图中甲、乙试管分别盛 有M、N的饱和溶液,试管底均有未溶解的M、N固体.向烧杯中加入一种物质后,甲中的固体减少,乙中的固体增加,则加入的物质可能是C
A图是物质M和N的溶解度曲线.B图中甲、乙试管分别盛 有M、N的饱和溶液,试管底均有未溶解的M、N固体.向烧杯中加入一种物质后,甲中的固体减少,乙中的固体增加,则加入的物质可能是C A.食盐 B.硝酸铵固体 C.氧化钙 D.NaOH固体或浓硫酸.
分析 由题意可知:A图表示硝酸钾和氢氧化钙的溶解度随温度变化的情况,B图中甲、乙试管分别盛有硝酸钾、氢氧化钙的饱和溶液,试管底部均有未溶解的固体,向烧杯中加入一种物质后,甲试管中固体减少,乙试管中的固体增加.则可推测加入的物质为能使溶液温度增加的物质,故可推测答案.
解答 解:由图示结合题意可知甲的溶解度随温度的升高而增大,乙的溶解度随温度的升高而减小;向烧杯中加入一种物质后,甲中的固体减少,乙中的固体增加,说明是升温造成的,升温后甲由饱和变为不饱和溶液;乙有固体析出,仍为饱和溶液;氧化钙与水反应能使温度升高,氢氧化钠、浓硫酸溶于水都放出热量,
故答案为:C,NaOH固体或浓硫酸.
点评 本题主要结合溶解时的热量变化考查了固体溶解度曲线所表示的意义,题目难度不大,通过本题可以加强学生对所学理解,培养学生应用知识解决问题的能力.

练习册系列答案
相关题目
1.分子式为C7H12O4,其中只含二个-COOCH3基团的同分异构体(不考虑手性异构)共有( )
| A. | 4种 | B. | 5种 | C. | 6种 | D. | 7种 |
2.有机物X的蒸气相对氢气的密度为51,X中氧元素的质量分数为31.7%,则能在碱性溶液中发生反应的X的同分异构体有(不考虑立体异构)( )
| A. | 4种 | B. | 9种 | C. | 13种 | D. | 15种 |
19.标准状况下,某同学向100mLH2S饱和溶液中通入SO2,所得溶液pH变化如图所示,下列分析中,正确的是( )
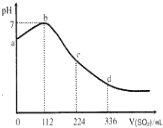

| A. | b 点对应的溶液导电性最强 | |
| B. | 亚硫酸是比氧硫酸更弱的酸 | |
| C. | 原H2S溶液的物质的量浓度为0.05mol•L-1 | |
| D. | ab段反应是:SO2+2H2S═3S↓+2H2O |
6.某元素X的最高价氧化物的水化物的化学式为H2XO4,则其气态氢化物的化学式应为( )
| A. | H2X | B. | H3X | C. | XH4 | D. | HX |
16.乌洛托品在合成、医药、染料等工业中有广泛用途,其结构如图.下列说法正确的是( )
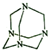

| A. | 分子式为N4C6 | B. | 分子中的氮原子全部是sp2杂化 | ||
| C. | 分子中共形成4个六元环 | D. | 分子间存在氢键 |
3.垃圾无害化处理首先要求将垃圾分类收集.某居民小区垃圾收集点有三个垃圾桶,分别标明“厨余垃圾”、“电池”、“可回收物”.下列物质中不应投入“可回收物”桶内的是( )
| A. | 玻璃碎片 | B. | 破塑料盒 | C. | 纸制包装盒 | D. | 瓜皮果壳 |
20.某气体在标准状况下的密度是1.25克/升,该气体的相对分子质量为( )
| A. | 26 | B. | 28 | C. | 30 | D. | 32 |
1.下列物质属于酸的是( )
| A. | 二氧化硫 | B. | 生石灰 | C. | 三氧化硫 | D. | 硫酸 |