题目内容
16.乌洛托品在合成、医药、染料等工业中有广泛用途,其结构如图.下列说法正确的是( )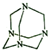
| A. | 分子式为N4C6 | B. | 分子中的氮原子全部是sp2杂化 | ||
| C. | 分子中共形成4个六元环 | D. | 分子间存在氢键 |
分析 A.根据结构简式确定分子式;
B.氮原子成三个键,有一对孤对电子;
C.分子中共形成4个六元环;
D.含有N、O、F的氢化物能形成氢键.
解答 解:A.乌洛托品分子式为C6H12N4,故A错误;
B.氮原子成三个键,有一对孤对电子,为sp3杂化,故B错误;
C.由图知,分子中共形成4个六元环,故C正确;
D.含有N、O、F的氢化物能形成氢键,氮原子上没有氢原子,故D错误.
故选C.
点评 本题考查有机物的结构与性质,为高频考点,把握常见有机物的组成、官能团与性质的关系等为解答的关键,题目难度不大.

练习册系列答案
相关题目
6.下列有机物的命名或化学术语正确的是( )
| A. | 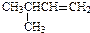 2-甲基-3-丁烯 2-甲基-3-丁烯 | B. | 乙炔的结构简式:CHCH | ||
| C. | 乙醚的分子式:C 2H 6O | D. | 甲基的电子式: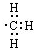 |
7.阿伏加德罗常数约为6.02×1023 mol-1,下列叙述正确的是( )
| A. | 2.24 L CO2中含有的原子数为0.3×6.02×1023 | |
| B. | 0.1 mol F- 中含有的电子数等于0.9×6.02×1023 | |
| C. | 5.6 g铁粉与硝酸反应失去的电子数一定为0.3×6.02×1023 | |
| D. | 电解饱和食盐水若产生2 g氢气,则转移的电子数目为2×6.02×1023 |
4.已知短周期元素的离子aA2+、bB+、cC3-、dD-都具有相同的电子层结构,则下列叙述正确的是( )
| A. | 原子半径 A>B>D>C | B. | 原子序数 d>c>b>a | ||
| C. | 离子半径 C>D>B>A | D. | 元素的电负性 D>C>A>B |
1.I2在KI溶液中存在下列平衡:I2 (aq)+I-(aq)?I3-(aq).测得不同温度下该反应的平衡常数如下表:( )
| t/℃ | 5 | 15 | 25 | 35 | 50 |
| K | 1100 | 841 | 689 | 533 | 409 |
| A. | 反应I2 (aq)+I-(aq)?I3-(aq)的△H>0 | |
| B. | 其他条件不变,升高温度,溶液中c(I3-)减小 | |
| C. | 在上述平衡体系中加入苯,平衡不移动 | |
| D. | 25℃时向溶液中加入少量KI固体,平衡常数K大于689 |
5.下列事实与胶体性质无关的是( )
| A. | 夏日的傍晚常常看到万丈霞光穿云而过,美不胜收 | |
| B. | 食品加工厂利用豆浆中加入盐卤做豆腐 | |
| C. | 三氯化铁溶液中滴入氢氧化钠溶液出现红褐色沉淀 | |
| D. | 某化工厂利用静电除尘技术去除废气中的固体悬浮物 |
6.下列说法正确的是( )
| A. | 在常温常压下,11.2LN2所含有的分子数为0.5NA | |
| B. | 在标准状况下,22.4 L CO和N2的混合物的物质的量为1mol | |
| C. | 在标准状况下,18g H2O的体积为22.4 L | |
| D. | 1mol SO2中原子数为NA个 |
 A图是物质M和N的溶解度曲线.B图中甲、乙试管分别盛 有M、N的饱和溶液,试管底均有未溶解的M、N固体.向烧杯中加入一种物质后,甲中的固体减少,乙中的固体增加,则加入的物质可能是C
A图是物质M和N的溶解度曲线.B图中甲、乙试管分别盛 有M、N的饱和溶液,试管底均有未溶解的M、N固体.向烧杯中加入一种物质后,甲中的固体减少,乙中的固体增加,则加入的物质可能是C