题目内容
6.某元素X的最高价氧化物的水化物的化学式为H2XO4,则其气态氢化物的化学式应为( )| A. | H2X | B. | H3X | C. | XH4 | D. | HX |
分析 元素的最高正价+|最低负价|=8,根据元素的最高价氧化物的水化物的化学式确定最高正价,进而求得最低负价,得出气态氢化物的化学式.
解答 解:元素X的最高价氧化物的水化物的化学式为H2XO4,所以X的最高正价是+6价,元素的最高正价+|最低负价|=8,所以最低负价为-2价,X的气态氢化物的化学式为H2X.
故选:A.
点评 本题考查学生元素周期律的应用知识,注意把握元素的最高正价与负价的关系,题目较简单.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
16.下列叙述中,正确的是( )
| A. | 第三周期元素的离子半径从左到右逐渐减小 | |
| B. | ⅥA族元素的原子,其半径越大,越容易得到电子 | |
| C. | ⅥA族元素的氢化物中,稳定性最好的其还原性最强 | |
| D. | IA族与 VIIA族元素间可形成共价化合物或离子化合物 |
17.下列说法正确的是( )
| A. | SiO2与酸、碱均不反应 | |
| B. | NO2溶于水时发生氧化还原反应 | |
| C. | SO2具有氧化性,可用于漂白纸浆 | |
| D. | Cl2、SO2均能使品红溶液褪色,说明二者均有氧化性 |
14.对于常温下pH均为4的三种溶液:①盐酸,②CH3COOH溶液,③NH4Cl溶液,下列说法中正确的是( )
| A. | 溶液中由水电离出的c(H+):②>③ | |
| B. | 稀释100倍后溶液的pH:①<③ | |
| C. | 中和相同体积的上述溶液消耗NaOH溶液的体积:①<② | |
| D. | ②和③等体积混合后的溶液:c(CH3COO-)+c(Cl-)=c(NH4+) |
18.有关甲、乙、丙、丁四个图示的叙述不正确的是( )


| A. | 甲中负极反应式为Zn-2e-═Zn2+ | |
| B. | 乙中阳极反应式为Ag-e-═Ag+ | |
| C. | 丙中H+向碳棒方向移动 | |
| D. | 丁中电解开始时阳极产生黄绿色气体 |
15.下列各物质中,为同分异构体的是( )
| A. | 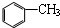 和 和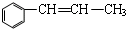 | |
| B. | 正丁烷和异丁烷 | |
| C. | 甲苯和二甲苯 | |
| D. | CH2═CH-CH═CH2和CH3-CH2-CH2-C≡CH |
16.下列有机物的命名正确的是( )
| A. |  2一甲基-3一丁烯 2一甲基-3一丁烯 | B. |  乙苯 乙苯 | C. |  2一甲基丁烷 2一甲基丁烷 | D. |  1一甲基乙醇 1一甲基乙醇 |
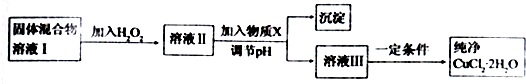
 A图是物质M和N的溶解度曲线.B图中甲、乙试管分别盛 有M、N的饱和溶液,试管底均有未溶解的M、N固体.向烧杯中加入一种物质后,甲中的固体减少,乙中的固体增加,则加入的物质可能是C
A图是物质M和N的溶解度曲线.B图中甲、乙试管分别盛 有M、N的饱和溶液,试管底均有未溶解的M、N固体.向烧杯中加入一种物质后,甲中的固体减少,乙中的固体增加,则加入的物质可能是C