题目内容
11.对于原电池的电极名称,下列叙述有错误的是( )| A. | 负极发生氧化反应 | B. | 正极为电子流入的一极 | ||
| C. | 比较不活泼的金属为负极 | D. | 负极为失去电子的一极 |
分析 原电池中,得电子发生还原反应的电极是正极,失电子发生氧化反应的电极是负极,电流从正极沿导线流向负极,电子与电流流向相反,溶液中阳离子向正极移动,据此进行解答.
解答 解:A.失电子发生氧化反应的电极是负极,所以负极上发生氧化反应,故A正确;
B.负极上失电子,正极上得电子,所以外电路中电子从负极沿导线流向正极,则正极为电子流入的一极,故B正确;
C.原电池中两个电极为活泼性不同的金属时,较不活泼的金属作正极,故C错误;
D.原电池中,负极失去电子发生氧化反应,故D正确;
故选C.
点评 本题考查了原电池原理及其应用,题目难度不大,其判断方法有:电子的流向、电流的流向、电极上得失电子、电极上发生反应类型、电解质溶液中阴阳离子移动方向等,试题侧重考查学生的灵活应用能力.

练习册系列答案
相关题目
1.DDT是人类合成得到的第一种有机农药,它的结构简式如图所示,有关它的说法正确的是( )
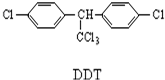

| A. | 它属于芳香烃 | B. | 分子式为C14H8Cl5 | ||
| C. | 1mol该物质能与6mol H2加成 | D. | 分子中最多可能有28个原子共面 |
2.现有部分短周期元素的性质或原子结构如下表:
下列说法正确的是( )
| 元素编号 | 元素性质或原子结构 |
| T | 最外层电子数是次外层电子数的2倍 |
| X | L层有三个未成对电子 |
| Y | L层p电子数比s电子数多两个 |
| Z | 元素的最高正价为+7价 |
| A. | Z离子的结构示意图为: | B. | 分子TY2的键角为180° | ||
| C. | T元素在周期表中的表示为: | D. | XZ3为非极性分子 |
19.3,5-二甲氧基苯酚是重要的有机合成中间体,可用于天然物质白柠檬素的合成.一种以间苯三酚为原料的合成反应如下:

甲醇、乙醚和3,5-二甲氧基苯酚的部分物理性质见表:
反应结束后,先分离出甲醇,再加入乙醚进行萃取.
(1)①分离出甲醇的操作是蒸馏.
②萃取用到的分液漏斗使用前需检查是否漏水并洗净,分液时有机层在分液漏斗的上填(“上”或“下”)层.
(2)分离得到的有机层依次用饱和NaHCO3溶液、饱和食盐水、少量蒸馏水进行洗涤.用饱和NaHCO3 溶液洗涤的目的是除去HCl;用饱和食盐水洗涤的目的是除去少量NaHCO3且减少产物损失.
(3)洗涤完成后,通过以下操作分离、提纯产物,正确的操作顺序是dcab(填字母).
a.蒸馏除去乙醚 b.重结晶 c.过滤除去干燥剂 d.加入无水CaCl2干燥.

甲醇、乙醚和3,5-二甲氧基苯酚的部分物理性质见表:
| 物质 | 沸点/℃ | 熔点/℃ | 密度(20℃)/g•cm-3 | 溶解性 |
| 甲醇 | 64.7 | / | 0.7915 | 易溶于水 |
| 乙醚 | 34.5 | / | 0.7138 | 微溶于水 |
| 3,5-二甲氧基苯酚 | / | 33-36 | / | 易溶于甲醇、乙醚,微溶于水 |
(1)①分离出甲醇的操作是蒸馏.
②萃取用到的分液漏斗使用前需检查是否漏水并洗净,分液时有机层在分液漏斗的上填(“上”或“下”)层.
(2)分离得到的有机层依次用饱和NaHCO3溶液、饱和食盐水、少量蒸馏水进行洗涤.用饱和NaHCO3 溶液洗涤的目的是除去HCl;用饱和食盐水洗涤的目的是除去少量NaHCO3且减少产物损失.
(3)洗涤完成后,通过以下操作分离、提纯产物,正确的操作顺序是dcab(填字母).
a.蒸馏除去乙醚 b.重结晶 c.过滤除去干燥剂 d.加入无水CaCl2干燥.
6.原子结构、元素周期律和元素周期表对于我们化学学习具有理论指导意义,下列有关说法正确的是( )
| A. | 同周期的主族元素从左到右原子半径逐渐减小,它们形成简单的离子半径逐渐增大 | |
| B. | 可以根据主族元素原子的电子层数和最外层电子数确定其在周期表中的位置 | |
| C. | 由氟、氯两元素在周期表中位置关系推知,氟元素非金属性强于氯元素,所以氢氟酸的酸性应强于盐酸 | |
| D. | 在实际生产中,多在元素周期表的过渡元素区寻找新型半导体材料 |
16.已知:
下列有关C2H5F性质的推测中肯定不合理的是( )
①沸点:50.5℃,密度:1.34g•cm-3
②沸点:10.1℃,密度:0.81g•cm-3
③沸点:21.3℃,密度:0.99g•cm-3
④沸点:7.0℃,密度:0.77g•cm-3.
C2H5Cl | C2H5Br | C2H5I | |
密度(g•cm-3) | 0.897 | 1.14 | 1.25 |
沸点(℃) | 12.3 | 38.4 | 42.5 |
①沸点:50.5℃,密度:1.34g•cm-3
②沸点:10.1℃,密度:0.81g•cm-3
③沸点:21.3℃,密度:0.99g•cm-3
④沸点:7.0℃,密度:0.77g•cm-3.
| A. | ①③ | B. | ①② | C. | ②③ | D. | ②④ |
20.取两份质量相等的有机物M,一份与Na2CO3溶液反应最多放出气体V1升,另一份与足量的钠反应放出气体V2升,;若同温同压下V2>V1>0,则M可能是( )
| A. | 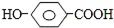 | B. | HO(CH2)2CHO | C. | HOOC-COOH | D. | CH3COOH |
1.关于分子2H218O2的说法正确的是( )
| A. | 该分子的摩尔质量约为40 | B. | 该分子由H2和O2构成 | ||
| C. | 1 mol该分子中含有22 mol中子 | D. | 1 mol该分子中含有20 mol电子 |
 某同学为探究元素周期表中元素性质的递变规律,设计了如下系列实验.
某同学为探究元素周期表中元素性质的递变规律,设计了如下系列实验.