题目内容
14.在一容积为2L的密闭容器中加入2molA和3molB,保持温度为30℃,在催化剂存在的条件下进行下列反应:A(g)+2B(g)?3C(g),达到平衡后生成1.2mol C,此时,平衡混合气中C的体积分数为ω;若将温度升高到70℃后,其他条件均不变,当反应重新达到平衡时,C的物质的量为2.1mol.请回答下列问题,
(1)该反应的平衡常数K随温度升高而增大(填“增大”、“减少”或“不变”),该反应的焓变△H>0(填“>”、“<”或“=”).
(2)30℃时,平衡混合气中C的体积分数ω=24%,A物质的转化率与B物质的转化率之比为3:4.
分析 (1)温度升高C的物质的量增大,结合平衡移动原理分析判断,升温平衡向吸热反应方向进行;
(2)在一容积为2L的密闭容器中加入2molA和3molB,保持温度为30℃,在催化剂存在的条件下进行下列反应:A(g)+2B(g)3C(g),达到平衡后生成1.2mol C,此时,平衡混合气中C的体积分数为ω,依据化学平衡三段式列式计算得到;
A(g)+2B(g)=3C(g),
起始量(mol) 2 3 0
变化量(mol) 0.4 0.8 1.2
平衡量(mol) 1.6 2.2 1.2
解答 解:(1)若将温度升高到70℃后,其他条件均不变,当反应重新达到平衡时,C的物质的量为2.1mol大于30°C生成的C的物质的量,说明反应正向进行,平衡常数增大,升温反应向吸热反应方向进行,说明正向反应是吸热反应,△H>0,
故答案为:增大;>;
(2)在一容积为2L的密闭容器中加入2molA和3molB,保持温度为30℃,在催化剂存在的条件下进行下列反应:A(g)+2B(g)3C(g),达到平衡后生成1.2mol C,此时,平衡混合气中C的体积分数为ω;
A(g)+2B(g)=3C(g),
起始量(mol) 2 3 0
变化量(mol) 0.4 0.8 1.2
平衡量(mol) 1.6 2.2 1.2
平衡混合气中C的体积分数ω=$\frac{1.2mol}{5mol}$×100%=24%;
A物质的转化率与B物质的转化率之比=$\frac{0.4}{2}$:$\frac{0.8}{3}$=3:4;
故答案为:24%;3:4.
点评 本题考查化学平衡影响因素的分析判断,化学平衡的计算应用,等效平衡的分析方法,题目难度中等.

| A. | 粗盐提纯 | B. | 蒸馏法将海水淡化为饮用水 | ||
| C. | 活性炭使红墨水褪色 | D. | 四氯化碳萃取碘水中的碘 |
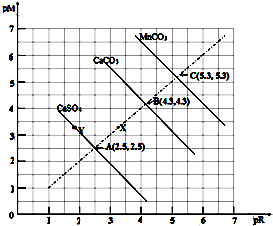
| A. | MnCO3在常温下的Ksp=2.5 x10-11(已知100.4=2.5) | |
| B. | 三种物质在常温下的溶解度大小顺序为MnCO3>CaCO3>CaSO4 | |
| C. | 处于Y点的CaSO4溶液中c(Ca2+)>c(SO42-) | |
| D. | Ca2+、CO32-浓度为X点的溶液可通过蒸发溶剂变为B点的溶液 |
当反应达到平衡后,反应放出的热量为Q1 kJ,物质X的转化率为α;若平衡后再升高温度,混合气体的平均相对分子质量减小,则
(1)化学计量数a的值为1.
(2)下列说法中能说明该反应达到了化学平衡状态的是AC.
A.容器内压强一定 B.容器内气体的密度一定C.容器内Z分子数一定 D.容器内气体的质量一定
(3)温度维持T℃不变,若起始时向容器M中加入的物质的量如下列各项,则反应达到平衡后放出的热量仍为Q1 kJ的是A (稀有气体不参与反应).
A.2mol X、1mol Y、1mol Ar B.a mol Z、1mol W
C.1mol X、0.5mol Y、0.5a mol Z、0.5mol W D.2mol X、1mol Y、1mol Z
(4)温度维持T℃不变,若起始时向容器M中加入4mol X和6mol Y,若达到平衡时容器内的压强减小了10%,则反应中放出的热量为QkJ.
(5)温度维持T℃不变,若在一个和原容器体积相等的恒压容器N 中,加入2mol X和1mol Y发生如上反应并达平衡,则N(选填M或N)容器中的反应先达到平衡状态,容器中X的质量分数M>N(选填>、<、=符号).
(6)已知:该反应的平衡常数随温度的变化如下表:
| 温度/℃ | 200 | 250 | 300 | 350 |
| 平衡常数K | 9.94 | 5.2 | 1 | 0.5 |
| A. | 常温常压下,28 g 14CO和N2的混合物所含的质子数为14NA | |
| B. | 常温下,100mL 1mol•L-1 Na2CO3溶液中阴离子总数大于0.1NA | |
| C. | 将NA个NH3分子溶于1 L水中得到1 mol•L-1的氨水 | |
| D. | 将标况下22.4LC12通入足量NaOH溶液中充分反应转移电子数是2NA |
| A. | KCl | B. | Mg(OH)2 | C. | Na2CO3 | D. | MgSO4 |
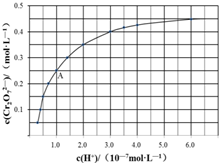 元素铬(Cr)在溶液中主要以Cr3+(蓝紫色)、Cr(OH)4-(绿色)、Cr2O72-(橙红色)、CrO42-(黄色)等形式存在,Cr(OH)3为难溶于水的灰蓝色固体,回答下列问题:
元素铬(Cr)在溶液中主要以Cr3+(蓝紫色)、Cr(OH)4-(绿色)、Cr2O72-(橙红色)、CrO42-(黄色)等形式存在,Cr(OH)3为难溶于水的灰蓝色固体,回答下列问题: