题目内容
下列氧化还原反应中,得失电子情况表示不正确的是( )
A、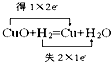 |
B、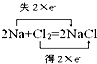 |
C、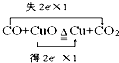 |
D、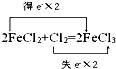 |
考点:氧化还原反应
专题:氧化还原反应专题
分析:氧化还原反应中失电子的元素化合价升高,得电子的元素化合价降低,化合价降低数目=化合价升高数目=转移的电子数目,以此解答该题.
解答:
解:A.铜元素化合价由+2价降低为0价,得到电子,氢元素化合价从0价升高为+1价,失去电子,转移电子为2e-,故A正确;
B.Cl元素化合价由0价降低为-1价,得到电子,钠元素化合价从0价升高为+1价,失去电子,转移电子为2e-,故B正确;
C.C元素化合价由+2价升高为+4价,失去电子,Cu元素化合价由+2价降低为0价,转移电子为2e-,故C正确;
D.反应中氯气为氧化剂,应得到电子,故D错误.
B.Cl元素化合价由0价降低为-1价,得到电子,钠元素化合价从0价升高为+1价,失去电子,转移电子为2e-,故B正确;
C.C元素化合价由+2价升高为+4价,失去电子,Cu元素化合价由+2价降低为0价,转移电子为2e-,故C正确;
D.反应中氯气为氧化剂,应得到电子,故D错误.
点评:本题考查氧化还原反应,为高频考点,侧重于电子转移的考查,注意从元素化合价的角度解答该题,难度不大,

练习册系列答案
相关题目
一定温度下,对可逆反应A(g)+2B(g)?3C(g)的下列叙述中,能说明反应已达到平衡的是( )
| A、A物质与B物质的反应速率之比为1:2 |
| B、单位时间内消耗a mol A,同时消耗3a mol C |
| C、容器内的压强不再变化 |
| D、混合气体的物质的量不再变化 |
在室温下等体积的酸和碱的溶液,混合后pH一定小于7的是( )
| A、pH=3的醋酸和pH=11氢氧化钠溶液 |
| B、pH=2的硫酸和pH=12的氢氧化钠溶液 |
| C、pH=3的盐酸和pH=11的氨水 |
| D、pH=2的硝酸和pH=12的氢氧化钠溶液 |
盐酸能发生下列反应:①Zn+2HCl═ZnCl2+H2↑②2HCl+CuO═CuCl2+H2O ③MnO2+4HCl═MnCl2+Cl2↑+2H2O,因此盐酸具有的性质是( )
| A、只有酸性 |
| B、只有氧化性 |
| C、只有还原性 |
| D、以上三种均具有 |
下列物质中,熔融状态不能导电的电解质是( )
| A、Na2SO4 |
| B、NaOH |
| C、C2H5OH |
| D、H2SO4 |