题目内容
在室温下等体积的酸和碱的溶液,混合后pH一定小于7的是( )
| A、pH=3的醋酸和pH=11氢氧化钠溶液 |
| B、pH=2的硫酸和pH=12的氢氧化钠溶液 |
| C、pH=3的盐酸和pH=11的氨水 |
| D、pH=2的硝酸和pH=12的氢氧化钠溶液 |
考点:pH的简单计算
专题:电离平衡与溶液的pH专题
分析:A.醋酸为弱酸,pH=3的醋酸溶液中氢离子浓度为0.001mol/L,醋酸的浓度远远大于0.001mol/L,两溶液混合后醋酸过量;
B.硫酸和氢氧化钠为强电解质,两溶液混合后恰好反应,溶液为中性;
C.氨水为弱碱,溶液中部分电离出氢氧根离子,两溶液混合后氨水过量,溶液显示碱性;
D.硝酸和氢氧化钠都是强电解质,两溶液混合后溶液显示中性.
B.硫酸和氢氧化钠为强电解质,两溶液混合后恰好反应,溶液为中性;
C.氨水为弱碱,溶液中部分电离出氢氧根离子,两溶液混合后氨水过量,溶液显示碱性;
D.硝酸和氢氧化钠都是强电解质,两溶液混合后溶液显示中性.
解答:
解:A.pH=3的醋酸中氢离子浓度为0.001mol/L,醋酸为弱酸,则醋酸的浓度大于0.001mol/L,而pH=11的氢氧化钠溶液的浓度为0.001mol/L,则二者等体积反应时醋酸过量,溶液呈酸性,混合后pH一定小于7,故A正确;
B.pH=2盐酸中氢离子浓度为0.01mol/L,pH=12的氢氧化钠溶液的浓度为0.01mol/L,两溶液等体积混合后恰好完全反应,溶液呈中性,溶液的pH=7,故B错误;
C.pH=3的盐酸的浓度为0.001mol/L,氨水为弱碱,pH=11的氨水的浓度大于0.001mol/L,两溶液等体积混合后氨水过量,溶液呈碱性,溶液中pH>7,故C错误;
D.pH=2的HNO3溶液的浓度为0.01mol/L,pH=12的NaOH溶液的浓度为0.01mol/L,两溶液等体积混合后恰好反应,溶液呈中性,pH=7,故D错误;
故选A.
B.pH=2盐酸中氢离子浓度为0.01mol/L,pH=12的氢氧化钠溶液的浓度为0.01mol/L,两溶液等体积混合后恰好完全反应,溶液呈中性,溶液的pH=7,故B错误;
C.pH=3的盐酸的浓度为0.001mol/L,氨水为弱碱,pH=11的氨水的浓度大于0.001mol/L,两溶液等体积混合后氨水过量,溶液呈碱性,溶液中pH>7,故C错误;
D.pH=2的HNO3溶液的浓度为0.01mol/L,pH=12的NaOH溶液的浓度为0.01mol/L,两溶液等体积混合后恰好反应,溶液呈中性,pH=7,故D错误;
故选A.
点评:本题考查酸碱混合的定性判断和计算,题目难度中等,注意把握酸碱的强弱以及溶液物质的量浓度的大小比较,明确溶液酸碱性与溶液pH的计算方法.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
下列实验操作正确的是( )
A、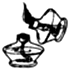 点燃酒精灯 |
B、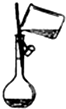 向溶液瓶中转移液体 |
C、 读取液体体积 |
D、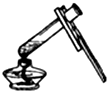 加热液体 |
下列有关说法正确的是( )
| A、塑料垃圾可直接露天焚烧 |
| B、实施“禁塑令”有助于遏制白色污染 |
| C、纤维素、油脂、蛋白质均属于有机高分子 |
| D、聚丙烯结构简式为:-[CH2-CH2-CH2]n- |
常温下,下列各组离子在指定溶液中一定能大量共存的是( )
| A、1.0mol?L-1的KNO3溶液:H+、Fe2+、Cl-、SO42- |
| B、含有大量Fe2+的溶液中:H+、Mg2+、ClO-、NO3- |
| C、c(H+)=10-12mol?L-1的溶液:K+、Ba2+、Cl-、Br- |
| D、能使Al溶解产生H2的溶液中:NH4+、Na+、SiO32-、HCO3- |
设NA表示阿伏加德罗常数的值,下列说法中正确的是( )
| A、1 mol NH4+ 所含质子数为10NA |
| B、CO2的摩尔质量为44 g |
| C、常温常压下,32 g O2和O3的混合气体所含原子数为2NA |
| D、标准状况下,22.4 LHCl溶于水形成1L溶液,所得溶液中溶质的物质的量浓度为22.4 mol/L |
下列各组热化学方程式中,△H1>△H2的是( )
A、C(s)+O2(g)═CO2(g)△H1 C(s)+
| ||
| B、S(g)+O2(g)═SO2(g)△H1 S(s)+O2(g)═SO2(g)△H2 | ||
C、2H2(g)+O2(g)═2H2O(l)△H1 H2(g)+
| ||
| D、CaCO3(s)═CaO(s)+CO2(g)△H1 CaO(s)+H2O(l)═Ca(OH)2(s)△H2 |
下列氧化还原反应中,得失电子情况表示不正确的是( )
A、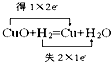 |
B、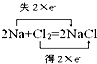 |
C、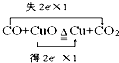 |
D、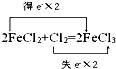 |
下列反应中属于氧化还原反应,伹水既不作氧化剂又不作还原剂的是( )
| A、SO3+H2O=H2SO4 |
| B、Cl2+H2O=HCl+HClO |
| C、2F2+2H2O=4HF+O2 |
| D、2Na+2H2O=2NaOH+H2↑ |
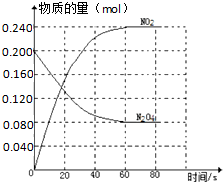 在容积固定为2.00L的密闭容器中,通入一定量的N2O4,发生反应N2O4(g)?2NO2(g)△H>0,100℃时体系中各物质的量(mol)随时间变化如图所示( )
在容积固定为2.00L的密闭容器中,通入一定量的N2O4,发生反应N2O4(g)?2NO2(g)△H>0,100℃时体系中各物质的量(mol)随时间变化如图所示( )| A、100℃时,在0-60s时段反应的平均反应速率v(N2O4)=0.002mol/(L?s) |
| B、100℃时,反应的平衡常数K为0.72mol?L-1 |
| C、100℃时达到平衡后,其它条件不变,仅改变反应温度为T,N2O4以0.001mol/(L?s)的平均速率变化,经10s又达到平衡,则T大于100℃ |
| D、保持反应体系的温度不变(100℃),再向该平衡体系中再加入一定量的N2O4,重新达平衡后,N2O4的体积分数与原平衡相等 |