题目内容
20.NA为阿伏加德罗常数值,下列说法中正确的是( )| A. | 标准状况下,11.2L四氯化碳所含分子数为0.5NA | |
| B. | 1L1mol/l的盐酸溶液中,所含氯化氢分子数为NA | |
| C. | 标准状况下,0.5molCO2所占的体积约为11.2L | |
| D. | 11.2L氧气所含的原子数为NA |
分析 A、标况下四氯化碳为液态;
B、HCl溶于水后完全电离为氢离子和氯离子;
C、体积V=nVm;
D、氧气所处的状态不明确.
解答 解:A、标况下四氯化碳为液态,故不能根据气体摩尔体积来计算其物质的量和分子个数,故A错误;
B、HCl溶于水后完全电离为氢离子和氯离子,故盐酸溶液中无HCl分子,故B错误;
C、体积V=nVm=0.5mol×22.4L/mol=11.2L,故C正确;
D、氧气所处的状态不明确,故氧气的物质的量无法计算,则含有的原子个数无法计算,故D错误.
故选C.
点评 本题考查了阿伏伽德罗常数的有关计算,熟练掌握公式的使用和物质的结构是解题关键,难度不大.

练习册系列答案
相关题目
4.下列说法正确的是( )
| A. | 在酒精灯加热条件下,Na2CO3、NaHCO3固定都能发生分解 | |
| B. | 不可用元素周期律解释热稳定性:Na2CO3>NaHCO3 | |
| C. | 分别加热Na2CO3和NaHCO3固体,试管内壁均有水珠,则两种物质均受热分解 | |
| D. | 1L0.1mol•L-1NaHCO3溶液中HCO3-和CO32-离子数之和为0.1NA |
8.下列溶液中Cl-浓度最大的是( )
| A. | 2 mol•L-1的HCl溶液 | B. | 1 mol•L-1的KCl溶液 | ||
| C. | 0.8 mol•L-1的AlCl3溶液 | D. | 0.5 mol•L-1的FeCl2溶液 |
15.从海水中提取溴有如下反应:5NaBr+NaBrO3+3H2SO4=3Br2+Na2SO4+3H2O,与该反应在氧化还原反应原理上最相似的是( )
| A. | 2NaBr+Cl2=2CaCl+Br2 | |
| B. | AlCl3+3NaAlO2+6H2O=4Al(OH)3↓+3NaCl | |
| C. | 2H2S+SO2=2H2O+3S↓ | |
| D. | 2CO+O2=2CO2 |
5.下列叙述正确的是( )
| A. | 在水溶液和熔融状态下能导电的化合物,叫做电解质 | |
| B. | 在水溶液或熔融状态下能导电的化合物,叫做电解质 | |
| C. | BaSO4是难溶物,所以是非电解质 | |
| D. | 氧化还原反应的本质是化合价升降 |
9.某合作学习小组讨论辨析以下说法正确的是( )
①粗盐和酸雨都是混合物
②硅是光导纤维的主要成分
③冰和干冰既是纯净物又是化合物
④不锈钢和目前流通的硬币都是合金
⑤盐酸和食醋既是化合物又是酸
⑥纯碱和熟石灰都是碱
⑦豆浆、雾、烟都是胶体
⑧利用丁达尔效应可以区分溶液和胶体.
①粗盐和酸雨都是混合物
②硅是光导纤维的主要成分
③冰和干冰既是纯净物又是化合物
④不锈钢和目前流通的硬币都是合金
⑤盐酸和食醋既是化合物又是酸
⑥纯碱和熟石灰都是碱
⑦豆浆、雾、烟都是胶体
⑧利用丁达尔效应可以区分溶液和胶体.
| A. | ③④⑤⑥⑦ | B. | ①②③④⑥ | C. | ①③④⑦⑧ | D. | ①②④⑤⑧ |
10.下列各项表述中正确的是( )
| A. | I-131的原子组成:5378I | B. | HCl电子式: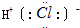 | ||
| C. | Na2S的电子式: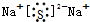 | D. | D2O的摩尔质量为:18g/mol |