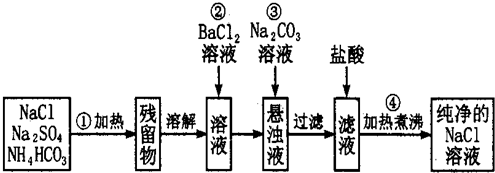
题目内容
4.下列说法正确的是( )| A. | 在酒精灯加热条件下,Na2CO3、NaHCO3固定都能发生分解 | |
| B. | 不可用元素周期律解释热稳定性:Na2CO3>NaHCO3 | |
| C. | 分别加热Na2CO3和NaHCO3固体,试管内壁均有水珠,则两种物质均受热分解 | |
| D. | 1L0.1mol•L-1NaHCO3溶液中HCO3-和CO32-离子数之和为0.1NA |
分析 A.Na2CO3不能发生分解;
B.Na2CO3、NaHCO3的性质与金属性、非金属性的递变无关;
C.Na2CO3不能发生分解;
D.NaHCO3溶液中含存在H2CO3.
解答 解:A.Na2CO3较稳定,不能发生分解,故A错误;
B.碳酸氢钠加热分解生成碳酸钠,可知热稳定性:Na2CO3>NaHCO3,不能用元素周期律解释,故B正确;
C.Na2CO3可能含有水或含有结晶水合物而导致试管内壁有水珠,但碳酸钠不发生分解,故C错误;
D.NaHCO3溶液中含存在H2CO3,1L0.1mol•L-1NaHCO3溶液中H2CO3、HCO3-和CO32-离子数之和为0.1NA,故D错误.
故选B.
点评 本题考查Na2CO3和NaHCO3性质,为高频考点,侧重于学生的分析能力的考查,题目难度不大,注意把握Na2CO3和NaHCO3性质的异同,注重基础知识的积累.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
14.某学生做元素性质递变实验时自己设计了一套方案,并记录了有关实验现象如下表(实验方案与实验现象没对应)
请你帮助该同学完成实验报告:
(1)实验的目的验证第三周期金属元素的金属性的递变规律;
(2)实验内容:与实验方案1-5对应的实验现象依次为E、A、C、B、D(填:字母编号);实验现象(A)为:钠浮在水面上,熔化化成小球,四处游动,发出嘶嘶响声,溶液变红;
(3)实验结论同周期从左到右元素的金属性逐渐减弱.
| 实验现象 |
| (A) |
| (B)反应不十分强烈,产生的气体可在空气中燃烧 |
| (C)剧烈反应,产生可燃性气体 |
| (D)生成白色胶状沉淀,然后沉淀消失 |
| (E)产生气体,可在空气中燃烧,溶液变成浅红色 |
| 实验方案 |
| 1.用砂纸打磨后的镁带加适量水加热,再向反应后溶液中滴加酚酞 |
| 2.钠与滴有酚酞的试液的冷水反应 |
| 3.镁带与2mol/L的盐酸反应 |
| 4.铝条与2mol/L的盐酸反应 |
| 5.向氯化铝溶液中滴加氢氧化钠溶液至过量 |
(1)实验的目的验证第三周期金属元素的金属性的递变规律;
(2)实验内容:与实验方案1-5对应的实验现象依次为E、A、C、B、D(填:字母编号);实验现象(A)为:钠浮在水面上,熔化化成小球,四处游动,发出嘶嘶响声,溶液变红;
(3)实验结论同周期从左到右元素的金属性逐渐减弱.
19.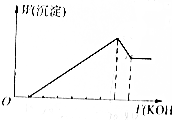 把镁铝合金用稀H2SO4溶液完全溶解后,在所得溶液中加入KOH溶液的体积与生成沉淀的质量关系如图所示,则合金中镁与铝的质量比是( )
把镁铝合金用稀H2SO4溶液完全溶解后,在所得溶液中加入KOH溶液的体积与生成沉淀的质量关系如图所示,则合金中镁与铝的质量比是( )
 把镁铝合金用稀H2SO4溶液完全溶解后,在所得溶液中加入KOH溶液的体积与生成沉淀的质量关系如图所示,则合金中镁与铝的质量比是( )
把镁铝合金用稀H2SO4溶液完全溶解后,在所得溶液中加入KOH溶液的体积与生成沉淀的质量关系如图所示,则合金中镁与铝的质量比是( )| A. | 1:1 | B. | 8:9 | C. | 4:3 | D. | 4:9 |
19.在标准状况下将19.2g铜粉投入一定量浓HNO3中随着铜粉的溶解,反应生成的气体颜色逐渐变浅,当铜粉完全溶解后共收集到由NO2和NO组成的混和气体8.96L,则混和气体中NO的体积为( )
| A. | 2240mL | B. | 1008mL | C. | 3360mL | D. | 448mL |
20.NA为阿伏加德罗常数值,下列说法中正确的是( )
| A. | 标准状况下,11.2L四氯化碳所含分子数为0.5NA | |
| B. | 1L1mol/l的盐酸溶液中,所含氯化氢分子数为NA | |
| C. | 标准状况下,0.5molCO2所占的体积约为11.2L | |
| D. | 11.2L氧气所含的原子数为NA |