题目内容
常温常压下,10mL某气态烃在50mLO2中充分燃烧生成CO2和H2O,恢复到原来状态时剩余35mL气体,则此烃可能是( )
| A、C2H6 |
| B、C3H4 |
| C、C3H8 |
| D、C4H6 |
考点:有关有机物分子式确定的计算
专题:烃及其衍生物的燃烧规律
分析:常温常压下水为液态,设烃的分子式为CxHy,根据烃的燃烧通式CxHy+(x+
)O2→xCO2+
H2O,利用差量法计算出氢原子的数目,再根据完全燃烧即氧气足量进行判断.
| y |
| 4 |
| y |
| 2 |
解答:
解:常温常压下,水为液态,设烃的分子式为CxHy,
则CxHy+(x+
)O2→xCO2+
H2O△V
1 (x+
) x 1+
10mL (10+50-35)mL
解得y=6,
选项AD符合,其中10mLC2H6消耗氧气的体积为:10mL×(2+
)=35mL,能充分燃烧;
而10mLC4H6完全燃烧消耗的氧气的体积为:10mL×(4+
)=55mL,氧气不足,不能完全燃烧,所以只有A正确,
故选A.
则CxHy+(x+
| y |
| 4 |
| y |
| 2 |
1 (x+
| y |
| 4 |
| y |
| 4 |
10mL (10+50-35)mL
解得y=6,
选项AD符合,其中10mLC2H6消耗氧气的体积为:10mL×(2+
| 6 |
| 4 |
而10mLC4H6完全燃烧消耗的氧气的体积为:10mL×(4+
| 6 |
| 4 |
故选A.
点评:本题考查有机物燃烧的计算,题目难度中等,把握有机物燃烧的通式及差量法计算为解答的关键,注意常温下水为液体,选项D为易错点,注意判断能否完全燃烧.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
设NA表示阿伏加德罗常数的值,下列叙述正确的是( )
| A、粗铜(含铁、镍、银等杂质)的电解精炼中,外电路转移电子数为2NA个时,阳极减少的质量大于64g |
| B、0.168g铁粉加入100mL0.1mol/L稀硝酸充分反应后,溶液中含有0.015mol/L亚铁离子(假设溶液体积不变) |
| C、往密闭容器中通入3.0gH2和14gN2,充分反应后可得到NH3分子数为NA |
| D、298K、101kPa下,33.6L的SO2中含有的分子数为1.5NA |
已知25℃时有关弱酸的电离常数:
25℃下,下列有关说法正确的是( )
| 弱酸 | CH3COOH | HCN | H2CO3 |
| 电离常数 | 1.8×10-5 | 4.9×10-10 | K1=4.3×10-7 K2=5.6×10-11 |
| A、浓度为0.10 mol?L-1的HCN溶液中c(OH-)=10-13 mol?L-1 |
| B、物质的量浓度相同的稀酸溶液中Kw:CH3COOH>H2CO3>HCN |
| C、物质的量浓度相同的三种钠盐溶液的pH:NaHCO3>NaCN>CH3COONa |
| D、浓度均为a mol?L-1的HCN溶液与NaOH溶液等体积混合充分反应后的溶液中(忽略体积的变化):c(H+)<c(OH-)<c(CN-)<0.5a mol?L-1 |
乙醇分子中各化学键如图所示对乙醇在各种反应中应断裂的键说明不正确的是( )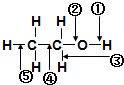

| A、和金属钠作用时,键①断裂 |
| B、和浓硫酸共热至170℃时,键②和⑤断裂 |
| C、和浓硫酸共热至140℃时,键②和③断裂 |
| D、在铜催化下和氧气反应时,键①和③断裂 |
下列有关离子大量共存的说法正确的是( )
| A、H+、Fe2+、SO42-、NO3-因发生氧化还原反应而不能大量共存 |
| B、水电离产生c(H+)=1×10-12mol/L的溶液中,可能有Mg2+、Na+、Cl-、HCO3-大量共存 |
| C、澄清透明的无色溶液中,可能有ClO-、MnO4-、Al3+、SO42-大量共存 |
| D、在含大量Fe3+的溶液中,可能有NH4+、Na+、Cl-、SCN-大量共存 |
100℃时向pH=6的蒸馏水中加入NaHSO4晶体,保持温度不变,测得溶液的pH=2,下列叙述正确的是( )
| A、此时水的离子积KW=1.0×10-14 |
| B、水电离出的c(H+)=1.0×10-10mol/L |
| C、水的电离度程不随温度升高而变化 |
| D、100℃时,蒸馏水呈酸性 |
设NA代表阿伏加德罗常数的数值,下列说法中正确的是( )
| A、标准状况时,22.4L四氯化碳所含有的分子数为NA |
| B、34g H2O2中含有的非极性共价键数为 NA |
| C、碱性锌锰电池中,当有1.3g的锌消耗,则转移的电子数为0.002NA |
| D、将16gO2与64gSO2在一定的条件下充分反应生成的SO3分子数为NA |
常温能被浓硝酸钝化的黑色金属是 ( )
| A、Mg | B、Al | C、Fe | D、Cu |
下列叙述中错误的是( )
| A、元素的性质呈周期性变化的根本原因是元素原子的核外电子排布呈周期性变化 |
| B、主族元素在周期表中的位置取决于该元素原子的电子层数和最外层电子数 |
| C、除零族元素外,短周期元素的最高正化合价在数值上都等于该元素所属的族序数 |
| D、副族元素中没有非金属元素 |