题目内容
3.下列物质能和NaHCO3溶液反应,既无气体逸出,也无沉淀生成的是( )| A. | 石灰石 | B. | 熟石灰 | C. | 烧碱 | D. | 硫酸 |
分析 NaHCO3+NaOH=Na2CO3+H2O中无气体、沉淀生成,以此来解答.
解答 解:A.石灰石和NaHCO3溶液不反应,故A不选;
B.熟石灰与NaHCO3溶液反应生成碳酸钙沉淀,故B不选;
C.烧碱与NaHCO3溶液反应生成碳酸钠和水,既无气体逸出,也无沉淀生成,故C选;
D.硫酸与NaHCO3溶液反应为H2SO4+2NaHCO3=Na2SO4+2CO2↑+2H2O,有气体生成,故D不选;
故选C.
点评 本题考查物质的性质及反应,为高频考点,把握物质的性质、发生的反应等为解答的关键,侧重分析与应用能力的考查,注意复分解反应的判断,题目难度不大.

练习册系列答案
相关题目
13. 常温下,向20mL 0.2mol/L H2A溶液中滴加0.2mol/L NaOH溶液.有关微粒的物质的量变化如图(其中Ⅰ代表H2A,Ⅱ代表HA-,Ⅲ代表A2-)所示.根据图示判断,下列说法正确的是( )
常温下,向20mL 0.2mol/L H2A溶液中滴加0.2mol/L NaOH溶液.有关微粒的物质的量变化如图(其中Ⅰ代表H2A,Ⅱ代表HA-,Ⅲ代表A2-)所示.根据图示判断,下列说法正确的是( )
 常温下,向20mL 0.2mol/L H2A溶液中滴加0.2mol/L NaOH溶液.有关微粒的物质的量变化如图(其中Ⅰ代表H2A,Ⅱ代表HA-,Ⅲ代表A2-)所示.根据图示判断,下列说法正确的是( )
常温下,向20mL 0.2mol/L H2A溶液中滴加0.2mol/L NaOH溶液.有关微粒的物质的量变化如图(其中Ⅰ代表H2A,Ⅱ代表HA-,Ⅲ代表A2-)所示.根据图示判断,下列说法正确的是( )| A. | 当V(NaOH)=20 mL时,溶液中离子浓度大小关系:c(Na+)>c(HA-)>c(A2-)>c(H+)>c(OH-) | |
| B. | 等浓度的NaOH溶液与H2A溶液按2:1混合后,其溶液中水的电离程度比纯水大 | |
| C. | NaHA溶液中:c(OH-)=c(H+)+c(HA-)+2c(H2A) | |
| D. | 向上述加入20 mL NaOH溶液后所得溶液中再加入水的过程中,pH可能减少 |
14.下列化学用语的书写正确的是( )
| A. | CO2的比例模型: | B. | 氮气的电子式: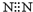 | ||
| C. | S原子结构示意图: | D. | 8个中子的碳原子的符号:12C |
11.在含NaCl、KCl、Na2SO4、K2SO4四种物质的混合液中,已知Na+、Cl- 和K+ 的物质的量浓度分别为0.80mol/L、0.70mol/L和0.40mol/L,则SO42- 的物质的量浓度为( )
| A. | 0.25 mol/L | B. | 0.30 mol/L | C. | 0.40 mol/L | D. | 0.50 mol/L |
18.25℃时,体积和物质的量浓度都相同的氢氧化钠溶液和氨水,分别与同浓度的盐酸相混合,直至溶液的pH都为7,则下列叙述正确的是( )
①消耗盐酸的体积氢氧化钠比氨水多
②消耗盐酸的体积氨水比氢氧化钠多
③两种溶液所消耗盐酸的体积相同
④所得溶液中,c(OH-)=c(H+)
①消耗盐酸的体积氢氧化钠比氨水多
②消耗盐酸的体积氨水比氢氧化钠多
③两种溶液所消耗盐酸的体积相同
④所得溶液中,c(OH-)=c(H+)
| A. | ①④ | B. | ③ | C. | ③④ | D. | ②④ |
8.现有300mL的某浓度的盐酸溶液,其中含溶质54.75g,现欲配制1mol/L的盐酸溶液,需原溶液和蒸馏水的体积比为(假设液体体积可以加和)( )
| A. | 1:4 | B. | 1:5 | C. | 2:1 | D. | 2:3 |
12.下列关于烷烃的说法中,正确的是( )
| A. | 通式为CnH2n | |
| B. | 可以使酸性高锰酸钾溶液褪色 | |
| C. | 在光照下可与氯气发生加成反应 | |
| D. | 随分子中碳原子数的增加,烷烃的熔沸点升高 |