题目内容
含铜化合物是工业生产和日常生活中常用的物质.请根据题意回答下列问题:
(1)已知Cu2+、Fe3+以氢氧化物形式开始沉淀和完全沉淀时溶液的pH如下表:
为除去CuCl2溶液中含有的少量FeCl3杂质,可加入 (填一种物质的化学式),调节溶液的pH,使溶液中的Fe3+转化为Fe(OH)3沉淀而除去
(2)在空气中直接加热CuCl2?2H2O晶体得不到纯的无水CuCl2,原因是 .由CuCl2?2H2O晶体得到纯的无水的CuCl2合理方法是 .
(3)已知氧化性:Cu2+>I2,Ksp(CuCl)=1.7×10-7mol2?L-2,Ksp(CuI)=1.3×10-12mol2?L-2,则CuCl2溶液与KI溶液反应的离子方程式为 .
(1)已知Cu2+、Fe3+以氢氧化物形式开始沉淀和完全沉淀时溶液的pH如下表:
| 物质 | 开始沉淀 | 完全沉淀 |
| Cu2+ | 4.7 | 6.7 |
| Fe3+ | 1.9 | 3.2 |
(2)在空气中直接加热CuCl2?2H2O晶体得不到纯的无水CuCl2,原因是
(3)已知氧化性:Cu2+>I2,Ksp(CuCl)=1.7×10-7mol2?L-2,Ksp(CuI)=1.3×10-12mol2?L-2,则CuCl2溶液与KI溶液反应的离子方程式为
考点:难溶电解质的溶解平衡及沉淀转化的本质,物质分离和提纯的方法和基本操作综合应用
专题:
分析:(1)加入物质和酸反应调节溶液的pH,使溶液中的Fe3+转化为Fe(OH)3沉淀而除去,但不引入新的杂质;
(2)氯化铜中铜离子水解生成氢氧化铜,得不到纯净的氯化铜;应在氯化氢气流中加热失去结晶水;
(3)CuI溶度积远远小于CuCl,反应生成CuI沉淀,铜离子被还原,碘离子被氧化生成I2.
(2)氯化铜中铜离子水解生成氢氧化铜,得不到纯净的氯化铜;应在氯化氢气流中加热失去结晶水;
(3)CuI溶度积远远小于CuCl,反应生成CuI沉淀,铜离子被还原,碘离子被氧化生成I2.
解答:
解:(1)为除去CuCl2溶液中含有的少量FeCl3杂质,调节溶液的pH,加入CuO 或Cu(OH)2或CuCO3或Cu2(OH)2CO3,能调节溶液PH但不引入新的杂质,使溶液中的Fe3+转化为Fe(OH)3沉淀而除去;
故答案为:CuO 或Cu(OH)2或CuCO3或Cu2(OH)2CO3;
(2)在空气中直接加热CuCl2?2H2O晶体得不到纯的无水CuCl2,原因是在空气中直接加热CuCl2?2H2O晶体得不到纯的无水CuCl2,由CuCl2?2H2O晶体得到纯的无水的CuCl2合理方法是在干燥的HCl气流中加热脱水;
故答案为:加热CuCl2?2H2O晶体时Cu2+会发生水解而得不到纯净的CuCl2,在干燥的HCl气流中加热脱水;
(3)CuI溶度积远远小于CuCl,反应生成CuI沉淀,铜离子被还原,碘离子被氧化生成I2,CuCl2溶液与KI溶液反应的离子方程式为:2Cu2++4I-=2CuI↓+I2;
故答案为:2Cu2++4I-=2CuI↓+I2.
故答案为:CuO 或Cu(OH)2或CuCO3或Cu2(OH)2CO3;
(2)在空气中直接加热CuCl2?2H2O晶体得不到纯的无水CuCl2,原因是在空气中直接加热CuCl2?2H2O晶体得不到纯的无水CuCl2,由CuCl2?2H2O晶体得到纯的无水的CuCl2合理方法是在干燥的HCl气流中加热脱水;
故答案为:加热CuCl2?2H2O晶体时Cu2+会发生水解而得不到纯净的CuCl2,在干燥的HCl气流中加热脱水;
(3)CuI溶度积远远小于CuCl,反应生成CuI沉淀,铜离子被还原,碘离子被氧化生成I2,CuCl2溶液与KI溶液反应的离子方程式为:2Cu2++4I-=2CuI↓+I2;
故答案为:2Cu2++4I-=2CuI↓+I2.
点评:本题考查了混合物分离的实验方法,实验操作和注意问题,盐类水解分析应用,掌握基础是解题关键,题目难度中等.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
下列反应的离子方程式中正确的是( )
| A、钠与水反应:2Na+2H2O=2Na++2OH-+H2↑ |
| B、氢氧化钡溶液和硫酸铵溶液反应:Ba2++SO42-=BaSO4↓ |
| C、硫化钠溶于水呈碱性:S2-+2H2O?H2S+2OH- |
| D、向溴化亚铁溶液中通入少量氯气:Cl2+2Br-=2Cl-+Br2 |
若NA表示阿伏伽德罗常数,下列说法正确的是( )
| A、在同温同压时,相同体积的任何气体所含的原子数目相同 |
| B、将49gH2SO4溶于1L水中,所得溶液的物质的量浓度为0.5mol?L-1 |
| C、标准状况下,11.2L水所含的分子数为0.5NA |
| D、18g NH4+含有的电子数为10NA |
下列检验方法和结论都正确的是( )
| A、加入AgNO3溶液有白色沉淀生成,证明原溶液中一定有大量Cl- |
| B、加入硝酸后的溶液中,滴加BaCl2溶液,有白色沉淀生成,证明原溶液中一定有大量SO42- |
| C、加入盐酸后,放出能使澄清石灰水变浑浊的无色气体,证明原溶液中一定含有大量CO32- |
| D、加入无色酚酞试液后,溶液显红色,证明原溶液中一定含有大量OH- |


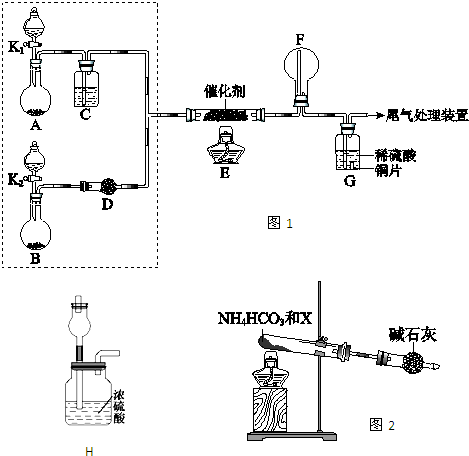
 (1)写出实验室制取氨气的化学方程式:
(1)写出实验室制取氨气的化学方程式: