题目内容
若NA表示阿伏伽德罗常数,下列说法正确的是( )
| A、在同温同压时,相同体积的任何气体所含的原子数目相同 |
| B、将49gH2SO4溶于1L水中,所得溶液的物质的量浓度为0.5mol?L-1 |
| C、标准状况下,11.2L水所含的分子数为0.5NA |
| D、18g NH4+含有的电子数为10NA |
考点:阿伏加德罗常数
专题:
分析:A.分子可以是单原子分子,也可以双原子分子;
B.49g硫酸的物质的量为0.5mol,0.5mol硫酸溶于1L水中,所得溶液体积大于1L;
C.标况下水的状态不是气体,不能使用标况下的气体摩尔体积计算水的物质的量;
D.铵根离子中含有10个电子,18g铵根离子的物质的量为1mol,含有10mol电子.
B.49g硫酸的物质的量为0.5mol,0.5mol硫酸溶于1L水中,所得溶液体积大于1L;
C.标况下水的状态不是气体,不能使用标况下的气体摩尔体积计算水的物质的量;
D.铵根离子中含有10个电子,18g铵根离子的物质的量为1mol,含有10mol电子.
解答:
解:A.气体分子可以是单原子分子,也可以双原子分子,在同温同压时,相同体积的任何气体所含的原子数目不一定相同,故A错误;
B.硫酸溶于1L水中,所得溶液体积不是1L,所得溶液的物质的量浓度小于0.5mol?L-1,故B错误;
C.标准状况水不是气体,不能使用标况下的气体摩尔体积计算11.2L水的物质的量,故C错误;
D.18g铵根离子的物质的量为1mol,1mol NH4+含有10mol电子,含有的电子数为10NA,故D正确;
故选D.
B.硫酸溶于1L水中,所得溶液体积不是1L,所得溶液的物质的量浓度小于0.5mol?L-1,故B错误;
C.标准状况水不是气体,不能使用标况下的气体摩尔体积计算11.2L水的物质的量,故C错误;
D.18g铵根离子的物质的量为1mol,1mol NH4+含有10mol电子,含有的电子数为10NA,故D正确;
故选D.
点评:本题考查阿伏加德罗常数的应用,题目难度中等,注意掌握好以物质的量为中心的各化学量与阿伏加德罗常数的关系,明确标况下气体摩尔体积的使用条件:标准状况下、物质状态必须为气体,试题培养了学生综合应用所学知识的能力.

练习册系列答案
相关题目
下列哪一组溶液的反应可用H++OH-=H2O 表示( )
| A、硫酸和氢氧化钡 |
| B、硫酸和烧碱 |
| C、硫酸和氢氧化铜 |
| D、硫酸和氨水 |
下面是常用来快速制备氨气的装置和试剂,其中不合理的是( )
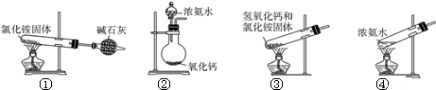

| A、一种 | B、二种 | C、三种 | D、四种 |
侯氏制碱法制备的工业产物主要是( )
| A、碳酸钠 | B、氢氧化钠 |
| C、碳酸氢钠 | D、氯化铵 |
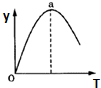 工业制氢气的一个重要反应是:CO(g)+H2O(g)?CO2(g)+H2(g)
工业制氢气的一个重要反应是:CO(g)+H2O(g)?CO2(g)+H2(g)