题目内容
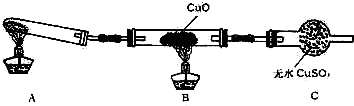
某小组同学欲实验验证NH3的化学性质,探究催化氧化反应,按如图1所示装置进行实验.A、B装置可选药品:浓氨水、H2O2、蒸馏水、NaOH固体、MnO2,C、D为干燥装置.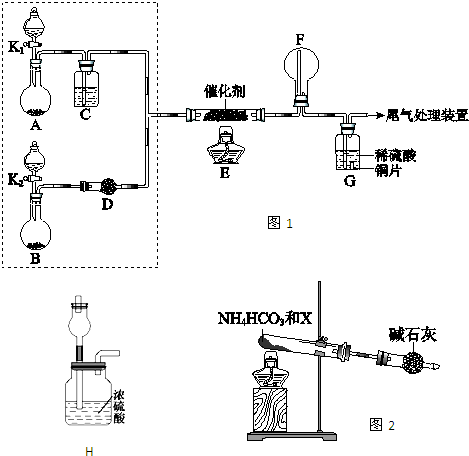
(1)装置A、B中产生气体的化学式分别是A: ;B: .
(2)实验开始后发现分液漏斗中液体不能顺利流下,应对实验装置如何改进来解决该问题. .
(3)甲乙两同学分别按上述装置进行实验.一段时间后,装置G中溶液都变成蓝色.甲观察到装置F中有红棕色气体,红棕色气体的成分是 .乙观察到装置F中只有白烟生成,白烟的成分是(写化学式) .G中可以观察到 现象.
(4)为帮助乙实现在装置F中也观察到红棕色气体,可在原实验的基础上进行改进.除了调节K1和K2控制A、B装置中的产气量外,还可以在装置E、F间增加一个H装置,理由是 .该装置采用空的干燥管,目的是 .
(5)为实现该反应,也可用如图2所示的装置替换上述装置中虚线框部分,该气体发生装置涉及多个化学反应,写出可能的化学方程式.如:NH4HCO3
NH3↑+CO2↑+H2O↑. .
(6)运输氨时,不能使用铜及其合金制造的管道阀门.因为,在潮湿的环境中,金属铜在有NH3存在时能被空气中的O2氧化,生成Cu(NH3)42+,该反应的离子方程式为 .

(1)装置A、B中产生气体的化学式分别是A:
(2)实验开始后发现分液漏斗中液体不能顺利流下,应对实验装置如何改进来解决该问题.
(3)甲乙两同学分别按上述装置进行实验.一段时间后,装置G中溶液都变成蓝色.甲观察到装置F中有红棕色气体,红棕色气体的成分是
(4)为帮助乙实现在装置F中也观察到红棕色气体,可在原实验的基础上进行改进.除了调节K1和K2控制A、B装置中的产气量外,还可以在装置E、F间增加一个H装置,理由是
(5)为实现该反应,也可用如图2所示的装置替换上述装置中虚线框部分,该气体发生装置涉及多个化学反应,写出可能的化学方程式.如:NH4HCO3
| △ |
(6)运输氨时,不能使用铜及其合金制造的管道阀门.因为,在潮湿的环境中,金属铜在有NH3存在时能被空气中的O2氧化,生成Cu(NH3)42+,该反应的离子方程式为
考点:氨的制取和性质
专题:实验题
分析:(1)根据实验目的可知,A、B装置制备的是氨气和氧气,再根据干燥装置特点判断A、B气体的名称;
(2)使分液漏斗与烧瓶内压强相等,则分液漏斗中液体能够顺利流下;
(3)氨气与氧气在催化剂作用下反应生成一氧化氮和水,一氧化氮与氧气反应生成红棕色的二氧化氮;二氧化氮与水反应生成硝酸,硝酸与氨气反应生成硝酸铵;二氧化氮与水反应生成的硝酸能够与铜发生反应生成硝酸铜、一氧化氮气体;
(4)根据浓硫酸具有酸性、吸水性分析装置H的作用;空的干燥管可以防止倒吸;
(5)虚线框部分需要制取氧气和氨气,碳酸氢铵分解生成氨气、二氧化碳和水,再用过氧化钠与二氧化碳、水反应可以生成氧气,据此写出反应的化学方程式;
(6)铜在有NH3存在时能被空气中的O2氧化,生成Cu(NH3)42+,以此书写离子反应.
(2)使分液漏斗与烧瓶内压强相等,则分液漏斗中液体能够顺利流下;
(3)氨气与氧气在催化剂作用下反应生成一氧化氮和水,一氧化氮与氧气反应生成红棕色的二氧化氮;二氧化氮与水反应生成硝酸,硝酸与氨气反应生成硝酸铵;二氧化氮与水反应生成的硝酸能够与铜发生反应生成硝酸铜、一氧化氮气体;
(4)根据浓硫酸具有酸性、吸水性分析装置H的作用;空的干燥管可以防止倒吸;
(5)虚线框部分需要制取氧气和氨气,碳酸氢铵分解生成氨气、二氧化碳和水,再用过氧化钠与二氧化碳、水反应可以生成氧气,据此写出反应的化学方程式;
(6)铜在有NH3存在时能被空气中的O2氧化,生成Cu(NH3)42+,以此书写离子反应.
解答:
解:(1)欲实验验证NH3的化学性质,则装置A、B中制取的是氧气和氨气,根据干燥装置C、D可知,装置C为浓硫酸,所以装置A中制取的是O2、装置B中制取的是NH3,
故答案为:O2;NH3;
(2)用导管将分液漏斗上口与烧瓶口相连或改用恒压滴液漏斗,使分液漏斗与烧瓶内压强相等,分液漏斗中液体则能够顺利流下,
故答案为:用导管将分液漏斗上口与烧瓶口相连或改用恒压滴液漏斗;
(3)NH3与过量O2在催化剂、加热条件下发生反应生成一氧化氮和水,反应方程为:4NH3+5O2
4NO+6H2O,NO与未反应的氧气反应生成二氧化氮,则装置F中红棕色气体为二氧化氮;二氧化氮与水反应生成硝酸,硝酸与氨气反应生成硝酸铵,所以乙观察到有装置F中有白烟生成;
装置G中二氧化氮与水反应生成硝酸,硝酸与铜反应生成硝酸铜和一氧化氮气体,则观察到的现象为:铜片溶解,表面有气泡,溶液变成蓝色,
故答案为:NO2;NH4NO3;铜片溶解,表面有气泡,溶液变成蓝色;
(4)装置H盛有浓硫酸,浓硫酸可以吸收氨气和水,可以避免二氧化氮与氨气和水反应;
氨气极易溶于水,需要使用防止倒吸装置,而空的干燥管具有防止倒吸的作用,
故答案为:除去混合气体中的水蒸气和未反应的氨气; 防止倒吸;
(5)图示装置中的虚线框部分需要制取氧气和氨气,图2中碳酸氢铵加热分解生成氨气、二氧化碳和水,反应方程式为:NH4HCO3
NH3↑+CO2↑+H2O↑,还缺少氧气,联系过氧化钠与二氧化碳、水反应生成氧气的知识,试剂X为过氧化钠,反应的化学方程式为:2CO2+2Na2O2=2Na2CO3+O2、2H2O+2Na2O2=4NaOH+O2,
故答案为:2CO2+2Na2O2=2Na2CO3+O2、2H2O+2Na2O2=4NaOH+O2;
(6)铜在有NH3存在时能被空气中的O2氧化,生成Cu(NH3)42+,该离子反应为:2Cu+8NH3+O2+2H2O═2Cu(NH3)42++4OH-,
故答案为:2Cu+8NH3+O2+2H2O═2Cu(NH3)42++4OH-.
故答案为:O2;NH3;
(2)用导管将分液漏斗上口与烧瓶口相连或改用恒压滴液漏斗,使分液漏斗与烧瓶内压强相等,分液漏斗中液体则能够顺利流下,
故答案为:用导管将分液漏斗上口与烧瓶口相连或改用恒压滴液漏斗;
(3)NH3与过量O2在催化剂、加热条件下发生反应生成一氧化氮和水,反应方程为:4NH3+5O2
| ||
| △ |
装置G中二氧化氮与水反应生成硝酸,硝酸与铜反应生成硝酸铜和一氧化氮气体,则观察到的现象为:铜片溶解,表面有气泡,溶液变成蓝色,
故答案为:NO2;NH4NO3;铜片溶解,表面有气泡,溶液变成蓝色;
(4)装置H盛有浓硫酸,浓硫酸可以吸收氨气和水,可以避免二氧化氮与氨气和水反应;
氨气极易溶于水,需要使用防止倒吸装置,而空的干燥管具有防止倒吸的作用,
故答案为:除去混合气体中的水蒸气和未反应的氨气; 防止倒吸;
(5)图示装置中的虚线框部分需要制取氧气和氨气,图2中碳酸氢铵加热分解生成氨气、二氧化碳和水,反应方程式为:NH4HCO3
| △ |
故答案为:2CO2+2Na2O2=2Na2CO3+O2、2H2O+2Na2O2=4NaOH+O2;
(6)铜在有NH3存在时能被空气中的O2氧化,生成Cu(NH3)42+,该离子反应为:2Cu+8NH3+O2+2H2O═2Cu(NH3)42++4OH-,
故答案为:2Cu+8NH3+O2+2H2O═2Cu(NH3)42++4OH-.
点评:本题考查了氨气制备及化学性质,题目难度中等,注意掌握氨气的制备原理及具有的化学性质,根据题干信息明确实验目的及反应原理为解答关键,试题有利于培养学生的分析、理解能力及化学实验能力.

练习册系列答案
相关题目
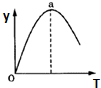
某化学科研小组研究在其他条件不变时,改变某一条件对A2(g)+3B2(g)?2AB3(g)化学平衡状态的影响,得到如下图所示的变化规律(图中T表示温度,n表示物质的量),根据如图可得出的判断结论正确的是( )
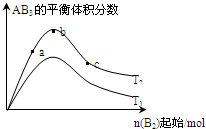

| A、反应速率a>b>c |
| B、若T2>T1,则正反应一定是吸热反应 |
| C、达到平衡时,AB3的物质的量大小为:b>c>a |
| D、达到平衡时A2的转化率大小为:b>a>c |
 .
.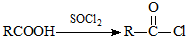

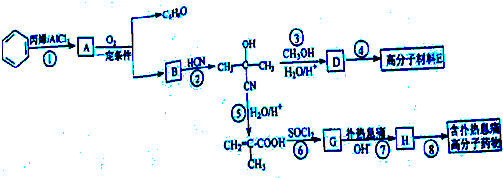
 工业制氢气的一个重要反应是:CO(g)+H2O(g)?CO2(g)+H2(g)
工业制氢气的一个重要反应是:CO(g)+H2O(g)?CO2(g)+H2(g)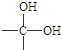 →
→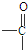 +H2O
+H2O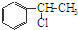 、
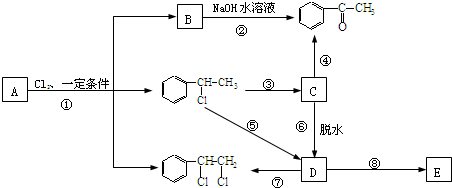
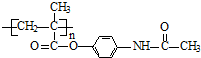
、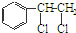 等都是A和Cl2发生反应生成的产物,E是一种高分子化合物,透光性能好,常用作一些灯饰外壳.过程中一些小分子都已经略去.
等都是A和Cl2发生反应生成的产物,E是一种高分子化合物,透光性能好,常用作一些灯饰外壳.过程中一些小分子都已经略去.