题目内容
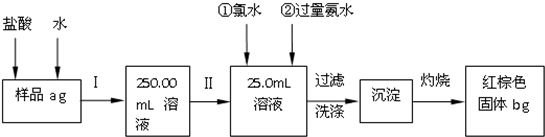
7.固态化合物A由两种短周期元素组成,可与水发生复分解反应,甲组同学用下图装置(夹持装置略)对其进行探究实验.
(1)仪器B的名称是分液漏斗.
(2)实验中,Ⅱ中的试纸变蓝,Ⅳ中黑色粉末逐渐变为红色并有气体M生成,则Ⅳ发生反应的化学方程式为3CuO+2NH3$\frac{\underline{\;\;△\;\;}}{\;}$3Cu+3H2O+N2↑;Ⅲ中的试剂为碱石灰.
(3)乙组同学进行同样实验,但装置连接顺序为Ⅰ--Ⅲ--Ⅳ--Ⅱ--Ⅴ,此时Ⅱ中现象为试纸变蓝,原因是CuO与氨气反应生成的水和未反应的氨气形成氨水,使试纸变蓝.
(4)经上述反应,2.5g 化合物A理论上可得0.56L(标准状况)M;则A的化学式为Mg3N2.
分析 实验中,Ⅱ中的试纸变蓝,可知A与水反应生成氨气,Ⅳ中黑色粉末逐渐变为红色并有气体M生成,IV中发生3CuO+2NH3$\frac{\underline{\;\;△\;\;}}{\;}$3Cu+3H2O+N2↑,V为排水法收集气体,则M为N2;装置连接顺序为Ⅰ--Ⅲ--Ⅳ--Ⅱ--Ⅴ,则干燥的氨气不能使干燥红色石蕊试纸变蓝;该化合物的化学式为M3Nx,M的相对原子质量为R,利用关系式M3Nx~$\frac{x}{2}$N2,确定R与x的关系,x是M的化合价,只能取正整数,讨论确定M的相对原子质量,进而确定元素,以此来解答.
解答 解:(1)仪器B的名称是分液漏斗,故答案为:分液漏斗;
(2)Ⅱ中的试纸变蓝,说明生成了NH3,Ⅳ中黑色粉末逐渐变为红色并有M生成,生成Cu,M为气体单质,为氮气,同时生成水,IV在发生反应为3CuO+2NH3$\frac{\underline{\;\;△\;\;}}{\;}$3Cu+3H2O+N2↑,Ⅲ中的试剂为碱石灰,可干燥氨气,故答案为:3CuO+2NH3$\frac{\underline{\;\;△\;\;}}{\;}$3Cu+3H2O+N2↑;碱石灰;
(3)装置连接顺序为Ⅰ--Ⅲ--Ⅳ--Ⅱ--Ⅴ,因为3CuO+2NH3 $\frac{\underline{\;\;△\;\;}}{\;}$N2+3Cu+3H2O,该反应有水生成,且氨气肯定不能完全反应,剩余的氨气和水反应NH3•H2O,显碱性,使红色石蕊试纸变蓝,
故答案为:试纸变蓝;CuO与氨气反应生成的水和未反应的氨气形成氨水,使试纸变蓝;
(4)设该化合物的化学式为M3Nx,M的相对原子质量为R,则:
M3Nx~$\frac{x}{2}$N2
3R+14x 11.2 x L
2.5g 0.56 L
2.5×11.2x=(3R+14x)×0.56
整理得R=12x,因x是M的化合价,只能取正整数,R为12、24或36,x=2时R为24,此元素只能为Mg符合,化合物A是Mg3N2,
故答案为:Mg3N2.
点评 本题考查物质组成和含量的测定实验,为高频考点,把握实验装置的作用、发生的反应及物质的性质为解答的关键,(4)中计算确定物质组成为解答的难点,题目难度中等.


| A. | X的分子式为C12H16O3 | |
| B. | 可用酸性高锰酸钾溶液区分苯和X | |
| C. | X在一定条件下能发生水解、酯化、加成等反应 | |
| D. | 在Ni作催化剂的条件下,1 mol X最多只能与1 mol H2加成 |
| A. | 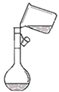 定容 | B. | 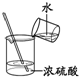 稀释浓硫酸 | C. | 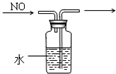 排水法收集NO | D. | 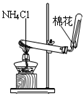 实验室制氨气 |
| A. | 苯和丙苯 | B. | 乙苯和间二甲苯 | C. | 丁二烯和丁烯 | D. | 萘和苯 |
 $\stackrel{一定条件下}{→}$
$\stackrel{一定条件下}{→}$ .
. +2NaOH$→_{△}^{乙醇}$
+2NaOH$→_{△}^{乙醇}$ +2NaBr+2H2O.
+2NaBr+2H2O.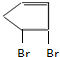 、
、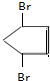 .
.