题目内容
17.标准状况下,有H2和CO的混合气体共8.96L,测得其总质量为6.0g,试计算:(1)求混合气体的平均相对分子质量;
(2)该混合气体中H2和CO的质量与体积分别为多少?(须写出详细计算过程)
分析 (1)根据n=$\frac{V}{{V}_{m}}$计算出标况下8.96L混合气体的物质的量,再根据M=$\frac{m}{n}$计算出平均摩尔质量,从而得出混合气体的平均相对分子质量;
(2)根据混合气体的总物质的量、总质量列式计算出氢气、一氧化碳的物质的量,再根据m=nM、V=nVm分别计算出二者的质量和体积.
解答 解:(1)标况下氢气和一氧化碳的总物质的量为:n(H2)+n(CO)=$\frac{8.96L}{22.4L/mol}$=0.4mol,
则混合气体的平均摩尔质量为:$\frac{6.0g}{0.4mol}$=15g/mol,
所以混合气体的平均相对分子质量为16,
答:混合气体的平均相对分子质量为16;
(2)混合气体的总物质的量为0.4mol,根据质量可得:n(H2)×2g/mol+(0.4mol-n(H2))×28g/mol=6.0g,
解得:n(H2)=0.2mol,则n(CO)=0.4mol-0.2mol=0.2mol,
混合气体中氢气的质量为:m(H2)=0.2mol×2g/mol=0.4g,一氧化碳的质量为:m(CO)=0.2mol×28g/mol=5.6g,
标况下一氧化碳和氢气的体积为:V(CO)=V(H2)=0.2mol×22.4L/mol=4.48L,
答:此混合气体中H2和CO的质量分别为m(H2)=0.4g,m(CO)=5.6g;体积为V(CO)=V(H2)=4.48L.
点评 本题考查了混合物反应的计算,题目难度中等,明确物质的量与摩尔质量、气体摩尔体积的关系为解答关键,试题侧重考查学生的分析、理解能力及化学计算能力.

练习册系列答案
相关题目
8.X、Y、Z、W是原子序数依次增大的短周期元素,且互不同族,其中只有两种为金属;X原子的最外层电子数与次外层电子数相等;X与W、Y与Z这两对原子的最外层电子数之和均为9.单质Y和W都可与浓的NaOH溶液反应.下列说法不正确的是( )
| A. | 原子半径:Y>Z>W | |
| B. | ZW2电子式为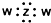 | |
| C. | 片状Y在空气中点燃时现象不剧烈 | |
| D. | 已知XW2熔点为-107℃、沸点为12.5℃,熔融时不导电,可说明固态XW2为共价化合物 |
5.下列说法正确的是( )
| A. | 海水经过加碱、加酸、浓缩结晶、过滤干燥、电解制得金属镁 | |
| B. | 除去铁粉中混有的少量铝粉,可加入过量的氢氧化钠溶液,完全反应后过滤 | |
| C. | 在稀硫酸中加入铜粉,铜粉不溶解,再加入Cu(NO3)2固体,铜粉仍不溶解 | |
| D. | 金属镁着火时,可以用二氧化碳灭火器来灭火 |
12.下列说法正确的是( )
| A. | 任何化学反应,只要是放热反应,理论上都能设计成原电池 | |
| B. | 周期表中所有元素都是从自然界中发现的 | |
| C. | 需要加热才能发生的反应一定是吸热反应 | |
| D. | 原子结合成分子过程中一定释放出能量 |
2.某炔烃与H2充分加成后的产物为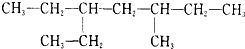 ,此炔烃可能的结构有( )
,此炔烃可能的结构有( )
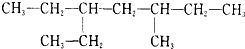 ,此炔烃可能的结构有( )
,此炔烃可能的结构有( )| A. | 1种 | B. | 2种 | C. | 3种 | D. | 4种 |
9.下列说法正确的是( )
①Na2CO3-制玻璃; ②SiO2-太阳能电池;③AgI-人工降雨;④Fe2O3-红色油漆或涂料;
⑤Al2O3-焊接钢轨;⑥NaClO-消毒剂; ⑦NaCl-制纯碱;⑧明矾-用于水的消毒、杀菌.
①Na2CO3-制玻璃; ②SiO2-太阳能电池;③AgI-人工降雨;④Fe2O3-红色油漆或涂料;
⑤Al2O3-焊接钢轨;⑥NaClO-消毒剂; ⑦NaCl-制纯碱;⑧明矾-用于水的消毒、杀菌.
| A. | ①②③⑥⑧ | B. | ②③⑤⑥⑦ | C. | ②③④⑥⑧ | D. | ①③④⑥⑦ |
6.下列说法中,不正确的是( )
| A. | 若反应时形成新化学键释放的能量大于断裂旧化学键所吸收的能量,则该化学反应是释放能量的反应 | |
| B. | 若反应物的总能量大于生成物的总能量,则该化学反应为释放能量的反应 | |
| C. | 化学反应中能量变化的大小与反应物的质量多少无关 | |
| D. | 化学反应必然伴随着能量的变化 |