题目内容
12.下列实验操作中,正确的是( )| A. | 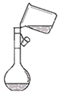 定容 | B. | 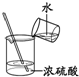 稀释浓硫酸 | C. | 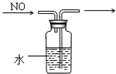 排水法收集NO | D. |  实验室制氨气 |
分析 A.转移液体需要玻璃棒引流,定容时加水至刻度线1~2cm处改用胶头滴管;
B.稀释浓硫酸,将密度大的液体注入密度小的液体中;
C.NO不溶于水,导管短进长出可收集NO;
D.氯化铵分解后,在试管口又化合生成氯化铵.
解答 解:A.转移液体需要玻璃棒引流,定容时加水至刻度线1~2cm处改用胶头滴管,则图中定容操作不合理,故A错误;
B.稀释浓硫酸,将密度大的液体注入密度小的液体中,则应将浓硫酸注入水中,顺序不合理,故B错误;
C.NO不溶于水,导管短进长出可收集NO,图中收集方法合理,故C正确;
D.氯化铵分解后,在试管口又化合生成氯化铵,则不能利用氯化铵制备氨气,故D错误;
故选C.
点评 本题考查化学实验方案的评价,为高频考点,涉及实验基本操作、气体的收集及制备等,把握实验基本技能及实验原理为解答的关键,侧重分析与实验能力的考查,题目难度不大.

练习册系列答案
 开心蛙状元作业系列答案
开心蛙状元作业系列答案 课时掌控随堂练习系列答案
课时掌控随堂练习系列答案 一课一练一本通系列答案
一课一练一本通系列答案 浙江之星学业水平测试系列答案
浙江之星学业水平测试系列答案
相关题目
2.某炔烃与H2充分加成后的产物为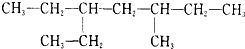 ,此炔烃可能的结构有( )
,此炔烃可能的结构有( )
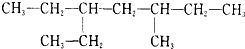 ,此炔烃可能的结构有( )
,此炔烃可能的结构有( )| A. | 1种 | B. | 2种 | C. | 3种 | D. | 4种 |
3.某同学探究同周期主族元素性质递变规律时,自己设计了一套实验方案,并记录了有关实验现象(见下表,表中的“实验方案”与“实验现象”前后不一定是对应关系).
请你帮助该同学整理并完成实验报告.
(1)实验目的:探究同一周期主族元素性质的递变规律.
(2)实验用品:试剂:金属钠,镁条,铝条,稀盐酸,新制氯水,新制Na2S溶液等.仪器:①烧杯,②试管,③胶头滴管,试管夹,镊子,小刀,玻璃片,砂纸,酒精灯等.
(3)实验内容:(填写与实验步骤对应的实验现象的编号和离子方程式)
(4)若用最高价氧化物的水化物的碱性相对强弱来验证Mg、Al失电子能力的相对强弱,请你设计实验(实验用品自选,不要求写化学方程式):向溶液中滴加NaOH溶液至过量,得白色沉淀,不溶解;向溶液中滴加NaOH溶液至过量,产生白色胶状沉淀,继而沉淀消失;.
(5)实验结论:同周期元素随原子序数增大,元素金属性逐渐减弱,非金属性逐渐增强.
| 实验步骤 | 实验现象 |
| 1.将镁条用砂纸打磨后,放入沸水中;再向溶液中滴加酚酞溶液 | A.浮在水面上,熔成小球,做不定向运动,随之消失,溶液变成红色. |
| 2.向新制得的Na2S溶液中滴加少量新制的氯水 | B.有气体产生,溶液变成浅红色 |
| 3.将一小块金属钠放入滴有酚酞溶液的冷水中 | C.剧烈反应,迅速产生大量无色气体. |
| 4.将镁条投入稀盐酸中 | D.反应不十分剧烈,产生无色气体 |
| 5.将铝条投入稀盐酸中 | E.生成淡黄色沉淀 |
(1)实验目的:探究同一周期主族元素性质的递变规律.
(2)实验用品:试剂:金属钠,镁条,铝条,稀盐酸,新制氯水,新制Na2S溶液等.仪器:①烧杯,②试管,③胶头滴管,试管夹,镊子,小刀,玻璃片,砂纸,酒精灯等.
(3)实验内容:(填写与实验步骤对应的实验现象的编号和离子方程式)
| 实验内容 | 实验现象 | 离子方程式 |
| 1 | ||
| 2 | ||
| 3 | ||
| 4 | ||
| 5 |
(5)实验结论:同周期元素随原子序数增大,元素金属性逐渐减弱,非金属性逐渐增强.
4.配制100ml 0.1mol/L Na2CO3溶液,下列操作正确的是( )
| A. | 称取1.06 g 无水碳酸钠,加入100ml容量瓶中,加水溶解、定容 | |
| B. | 称取1.06 g 无水碳酸钠,加入100ml蒸馏水,搅拌、溶解 | |
| C. | 转移Na2CO3溶液时,未用玻璃棒个引流,直接倒入容量瓶中 | |
| D. | 定容后,塞好瓶塞,反复倒转,摇匀 |
1.0.5molCl2中含有( )
| A. | 0.5个Cl2 | B. | 1个Cl原子 | ||
| C. | 3.01×1023个Cl原子 | D. | 6.02×1023个Cl原子 |
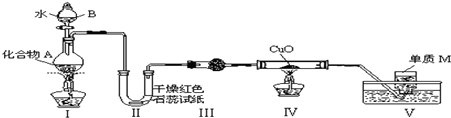
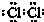 .
.
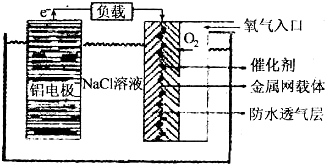
 .
.